
- •Глава 1. Введение
- •1.1. Термодинамика и ее метод
- •1.2. Параметры состояния
- •1.3. Понятие о термодинамическом процессе
- •1.4. Идеальный газ. Законы идеального газа
- •1.5. Понятие о смесях. Смеси идеальных газов
- •1.6. Понятие о теплоемкости
- •Глава 2. Первый закон термодинамики
- •2.1. Теплота. Опыт Джоуля. Эквивалентность теплоты и работы
- •2.2. Закон сохранения и превращения энергии
- •2.3. Внутренняя энергия и внешняя работа
- •2.4. Уравнение первого закона термодинамики
- •2.5. Энтальпия
- •2.6. Уравнение первого закона термодинамики для потока
- •Глава 3. Второй закон термодинамики
- •3.1. Циклы. Понятие термического КПД. Источники теплоты
- •3.2. Обратимые и необратимые процессы
- •3.3. Формулировки второго закона термодинамики
- •3.4. Цикл Карно. Теорема Карно
- •3.5. Термодинамическая шкала температур
- •3.6. Энтропия
- •3.7. Изменение энтропии в необратимых процессах
- •3.8. Объединенное уравнение первого и второго законов термодинамики
- •3.9. Энтропия и термодинамическая вероятность
- •3.10. Обратимость и производство работы
- •Глава 4. Дифференциальные уравнения термодинамики
- •4.1. Основные математические методы
- •4.2. Уравнения Максвелла
- •4.3. Частные производные внутренней энергии и энтальпии
- •4.4. Теплоемкости
- •Глава 5. Равновесие термодинамических систем и фазовые переходы
- •5.1. Гомогенные и гетерогенные термодинамические системы
- •5.2. Термодинамическое равновесие
- •5.3. Условия устойчивости и равновесия в изолированной однородной системе
- •5.4. Условия фазового равновесия
- •5.5. Фазовые переходы
- •5.7. Устойчивость фаз
- •5.8. Фазовые переходы при неодинаковых давлениях
- •Глава 6. Термодинамические свойства веществ
- •6.1. Термические и калорические свойства твердых тел
- •6.2. Термические и калорические свойства жидкостей
- •6.3. Опыт Эндрюса. Критическая точка. Уравнение Ван-дер-Ваальса
- •6.4. Термические и калорические свойства реальных газов. Уравнения состояния реальных газов
- •6.5. Термодинамические свойства веществ на линии фазовых переходов. Двухфазные системы
- •6.6. Свойства вещества в критической точке
- •6.7. Методы расчета энтропии вещества
- •6.8. Термодинамические диаграммы состояния вещества
- •6.9. Термодинамические свойства вещества в метастабильном состоянии
- •Глава 7. Основные термодинамические процессы
- •7.1. Изохорный процесс
- •7.2. Изобарный процесс
- •7.3. Изотермический процесс
- •7.4. Адиабатный процесс
- •7.5. Политропные процессы
- •7.7. Адиабатное расширение реального газа в вакуум (процесс Джоуля)
- •7.8. Процессы смешения
- •7.9. Процессы сжатия в компрессоре
- •Глава 8. Процессы течения газов и жидкостей
- •8.1. Основные уравнения процессов течения
- •8.2. Скорость звука
- •8.3. Истечение из суживающихся сопл
- •8.4. Переход через скорость звука. Сопло Лаваля
- •8.5. Адиабатное течение с трением
- •8.6. Общие закономерности течения. Закон обращения воздействий
- •8.7. Температура адиабатного торможения
- •9.1. О методах анализа эффективности циклов
- •9.2. Методы сравнения термических КПД обратимых циклов
- •9.3. Метод коэффициентов полезного действия в анализе необратимых циклов
- •Глава 10. Теплосиловые газовые циклы
- •10.1. Циклы поршневых двигателей внутреннего сгорания
- •10.2. Циклы газотурбинных установок
- •10.3. Циклы реактивных двигателей
- •Глава 11. Теплосиловые паровые циклы
- •11.1. Цикл Карно
- •11.2. Цикл Ренкина
- •11.3. Анализ цикла Ренкина с учетом потерь от необратимости
- •11.4. Цикл с промежуточным перегревом пара
- •11.5. Регенеративный цикл
- •11.6. Бинарные циклы
- •11.7. Циклы парогазовых установок
- •11.8. Теплофикационные циклы
- •Глава 12. Теплосиловые циклы прямого преобразования теплоты в электроэнергию
- •12.1. Цикл термоэлектрической установки
- •12.2. Цикл термоэлектронного преобразователя
- •12.3. Цикл МГД-установки
- •Глава 13. Холодильные циклы
- •13.1. Обратные тепловые циклы и процессы. Холодильные установки
- •13.2. Цикл воздушной холодильной установки
- •13.3. Цикл парокомпрессионной холодильной установки
- •13.4. Цикл пароэжекторной холодильной установки
- •13.5. Понятие о цикле абсорбционной холодильной установки
- •13.6. Цикл термоэлектрической холодильной установки
- •13.7. Принцип работы теплового насоса
- •13.8. Методы сжижения газов
- •Глава 14. Влажный воздух
- •14.1. Основные понятия
- •14.2. Н, d-диаграмма влажного воздуха
- •Глава 15. Основы химической термодинамики
- •15.1. Термохимия. Закон Гесса. Уравнение Кирхгофа
- •15.2. Химическое равновесие и второй закон термодинамики
- •15.3. Константа равновесия и степень диссоциации
- •15.4. Тепловой закон Нернста

8.7. Температура адиабатного торможения
геометрического сопла. Иными словами, изменением расхода в трубе постоянного сечения можно создать те же условия течения, что и в геометрическом сопле (сопле переменного сечения) при G = const.
Этот вывод нетрудно получить и аналитическим путем. Из уравнения (8.43) следует, что при переменном расходе
dv = v |
dΣ |
dw |
dG |
|
. |
(8.94) |
------ |
+ ------ |
– ------- |
|
|||
|
Σ |
w |
G |
|
|
Подставляя в уравнение (8.82) это соотношение вместо соотношения (8.84), получаем из (2.83) для qвнеш = 0, qтр = 0, lтехн = 0, dz = 0 и Σ = const:
(M |
2 |
dw |
dG |
(8.95) |
|
– 1)------ |
= – ------- . |
||
|
|
w |
G |
|
Отсюда следует, что при М < 1 скорость потока растет при увеличении расхода (dw > 0 при dG > 0), а при М > 1 для увеличения скорости надо уменьшать расход (dw > 0 при dG < 0).
Как видно из изложенного, знак воздействия, которое нужно оказать на поток для его ускорения (подвод или отвод теплоты, работы, вещества и т.д.), меняется при переходе через скорость звука в критическом сечении сопла. Так, в тепловом сопле на его дозвуковом участке dqвнеш > 0 (подвод теплоты), а на
сверхзвуковом участке dqвнеш < 0 (отвод теплоты). Уравнение (8.88а), позволя-
ющее установить знак воздействия в зависимости от М, носит название з а к о н а о б р а щ е н и я в о з д е й с т в и й 1).
Уравнения, аналогичные уравнению (8.88а) для скорости движения потока, могут быть получены также для давления, температуры и удельного объема в потоке газа (жидкости).
8.7. Температура адиабатного торможения
Заканчивая рассмотрение адиабатных процессов течения, остановимся на понятии т е м п е р а т у р ы а д и а б а т н о г о т о р м о ж е н и я .
Напомним, что, как следует из уравнения (8.8), для двух произвольных точек обратимого адиабатного течения имеет место равенство
h1 |
w12 |
= h2 |
w22 |
, |
(8.96) |
+ ----- |
+ ----- |
||||
|
2 |
|
2 |
|
|
или, что то же самое, для всего потока
|
w2 |
|
|
h + |
----- |
= const . |
(8.96a) |
2 |
Если газ в потоке можно рассматривать как идеальный, а его теплоемкость считать постоянной, не зависящей от температуры, то, поскольку энтальпия такого газа (отсчитываемая от 0 K) равна h = cpT, уравнение (8.96) может быть
записано в следующем виде:
w2 |
(8.97) |
Т + -------- = const. |
|
2cp |
|
Из уравнения (8.97) видно, что если обратимый адиабатный поток идеального газа с постоянной теплоемкостью, имеющий температуру Т, полностью
1) Это уравнение и следствия из него получены Л.А. Вулисом.
293

Г л а в а 8. ПРОЦЕССЫ ТЕЧЕНИЯ ГАЗОВ И ЖИДКОСТЕЙ
заторможен (w = 0), то температура заторможенного потока (ее называют температурой адиабатного торможения Tа.т )
Tа.т |
w2 |
|
= Т + -------- . |
(8.98) |
|
|
2cp |
|
Из (8.98) видно, что всегда Та.т > Т. Поскольку для идеального газа [см. (7.55)] k = cp / cv и в соответствии с уравнением Майера (2.67)
ср – cv = R,
то
|
cp |
Rk |
|
|
|
(8.99) |
|
= ----------- |
|
|
|
||
|
|
k – 1 |
|
|
|
|
и уравнение (8.98) может быть записано в виде |
|
|
|
|||
Tа.т |
|
k – 1 |
w |
2 |
. |
(8.100) |
= T + ------------ |
|
|||||
|
|
2kR |
|
|
|
|
Наконец, с учетом того, что для идеального газа в соответствии с уравнением (8.25)
a = 
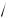 kRT ,
kRT ,
выражение (8.100) для температуры адиабатного торможения может быть преобразовано следующим образом:
T |
|
= T |
|
k – |
1 |
M |
2 |
. |
(8.101) |
а.т |
|
1 + ------------ |
|
||||||
|
|
2 |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Понятие о температуре адиабатного торможения широко используется в различных аэрогазодинамических расчетах. Всякий измерительный прибор, помещенный в поток, покажет температуру, близкую к температуре адиабатного торможения.
294
Глава 9. Общие методы анализа эффективности циклов тепловых
установок
9.1.О методах анализа эффективности циклов
9.2.Методы сравнения термических КПД обратимых циклов
9.3.Метод коэффициентов полезного действия в анализе необратимых циклов
9.4.Эксергетический метод анализа эффективности тепловых установок

Г л а в а д е в я т а я
ОБЩИЕ МЕТОДЫ АНАЛИЗА ЭФФЕКТИВНОСТИ ЦИКЛОВ ТЕПЛОВЫХ УСТАНОВОК
9.1. О методах анализа эффективности циклов
Общие принципы построения циклов тепловых двигателей и некоторые общие закономерности для этих циклов были сформулированы в гл. 3.
Располагая закономерностями различных термодинамических процессов, мы можем приступить к подробному рассмотрению циклов и принципиальных схем реальных тепловых установок. Условимся в дальнейшем тепловые установки, в которых осуществляется прямой цикл (т.е. цикл, в котором производится работа, отдаваемая внешнему потребителю), называть теплосиловыми установками, а установки, работающие по обратному циклу (т.е. циклу, для осуществления которого затрачивается работа, подводимая извне), — холодильными установками.
Циклы теплосиловых установок обычно подразделяют на три основные группы: газовые; паровые; прямого преобразования теплоты в электроэнергию.
Эти группы циклов подробно рассмотрены в гл. 10—12.
Такая классификация циклов определяется следующими причинами. Общим для всех теплосиловых газовых циклов является то, что в течение всего цикла рабочее тело находится в одном и том же агрегатном состоянии — в виде газа. При этом рабочее тело находится в состоянии, далеком от линии насыщения, и благодаря сравнительно невысоким давлениям в сочетании с весьма высокими (по сравнению с критической) температурами его можно с точностью, вполне достаточной для качественного анализа, рассматривать как идеальный газ.
Отличительной чертой второй большой группы циклов теплосиловых установок (паровых циклов) является использование таких рабочих тел, агрегатное состояние которых в цикле меняется: в одной части цикла рабочее тело находится в жидком состоянии, в другой части — в виде двухфазной смеси (влажного пара), в третьей — в виде перегретого пара. Обычно перегретый пар находится в состояниях, настолько близких к области насыщения, что к нему не применимы законы идеального газа.
Третья группа объединяет стоящие несколько особняком от первых двух групп циклы теплосиловых установок, в которых осуществляется так называемое прямое преобразование теплоты в электроэнергию.
Методы оценки эффективности циклов холодильных установок в принципе те же, что и теплосиловых установок. В этой главе рассматриваются методы анализа циклов теплосиловых установок; особенности оценки эффективности циклов холодильных установок анализируются в гл. 12.
Для оценки эффективности теплосиловой установки следует ответить на две основные группы вопросов:
1)Насколько велик КПД обратимого цикла теплосиловой установки, от каких факторов он зависит и что следует предпринять для его увеличения?
2)Насколько велики необратимые потери в реальном цикле установки, как распределяются эти потери по отдельным элементам цикла и, следовательно, на усовершенствование какой части цикла теплосиловой установки надо обратить внимание с целью уменьшения степени необратимости цикла (и, следовательно, увеличения КПД цикла)?
295

Гл а в а 9. ОБЩИЕ МЕТОДЫ АНАЛИЗА ЭФФЕКТИВНОСТИ ЦИКЛОВ
Всоответствии с этим в дальнейшем анализ циклов теплосиловых и холодильных установок будет проводиться, как правило, в два этапа — вначале анализ обратимого цикла, а затем — реального цикла с учетом основных источников необратимости.
Условимся в дальнейшем термин « т е р м и ч е с к и й К П Д » (ηт ) употреблять только для обозначения КПД обратимого цикла, а КПД реального необратимого цикла будем называть в н у т р е н н и м К П Д цикла ηцi .
Термин «внутренний» показывает, что речь идет о КПД собственно цикла: этот КПД характеризует степень совершенства процессов, совершаемых рабочим телом, но не отражает степени совершенства тех или иных узлов установки (они характеризуются так называемыми эффективными КПД, понятие о которых вводится в дальнейшем).
В соответствии с этим
|
ηт |
l |
цобр |
q1 |
– q2обр |
q2обр |
|
||||
|
= -------- |
q1 |
= |
--------------------- |
|
- = 1 – |
-------- |
; |
(9.1) |
||
|
|
|
|
|
|
|
q1 |
q1 |
|
||
ц |
l |
цдейств |
q |
1 |
– q2действ |
q |
2действ |
|
|||
ηi |
= --------------- |
|
q1 |
- |
= ----------------------------- |
|
|
= 1 – --------------- |
, |
(9.2) |
|
|
|
|
|
|
|
|
q1 |
|
q1 |
|
|
где индексы «обр» и «действ» относятся соответственно к обратимому и реальному необратимому (действительному) циклам.
Степень совершенства обратимых циклов полностью характеризуется термическим КПД в сравнении с термическим КПД цикла Карно, осуществляемого в том же интервале температур. Некоторые наиболее употребительные методы анализа таких циклов описаны в следующем параграфе. Эффективность реальных циклов можно оценивать по значению внутреннего КПД, определяемого
соотношением (9.2). Однако сама по себе величина ηцi еще не говорит о том,
какова степень необратимости цикла. Поэтому при анализе реальных необратимых циклов часто используется понятие об относительном КПД цикла, опреде-
|
|
|
|
|
|
|
ц |
= |
l |
цдейств |
ляемом следующим образом. Уравнение (9.2) для внутреннего КПД ηi |
---------------- |
|||||||||
|
|
|
|
|
|
|
|
|
|
q1 |
может быть записано в виде: |
|
|
|
|
|
|
|
|
|
|
|
ц |
|
l цдейств |
lцобр |
|
|
|
|||
|
ηi |
|
= |
--------------- |
-------- ; |
|
|
|
||
|
|
|
|
обр |
|
q1 |
|
|
|
|
|
|
|
|
lц |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
обозначая |
|
|
|
|
|
|
|
|
|
|
|
|
|
ц |
l цдейств |
|
|
|
(9.3) |
||
|
|
ηоi |
= --------------- |
|
|
|
||||
|
|
|
|
lцобр |
|
|
|
|
|
|
и учитывая (9.1), получаем: |
|
|
|
|
|
|
|
|
|
|
|
|
|
ηц |
= ηц |
η |
т |
. |
|
|
(9.4) |
|
|
|
i |
оi |
|
|
|
|
|
|
Величина ηц |
носит название в н у т р е н н е г о о т н о с и т е л ь н о г о |
К П Д |
||||||||
оi |
|
|
|
|
|
|
|
|
|
|
ц и к л а . Она показывает, насколько действительный цикл менее совершенен, чем обратимый цикл (т.е. какую долю ηт составляет внутренний КПД действи-
тельного цикла)1).
1)Для того чтобы подчеркнуть отличие ηi от η0i , величину ηi иногда называют также в н у т р е н н и м
аб с о л ю т н ы м К П Д ц и к л а .
296
