
хирургия 5 курс / книги / Savel'ev V.S. (red.) 80 lekcij po hirurgii (Litterra, 2008)(ru)(T)(K)(910s)(ISBN 9785982161190)
.pdfПрофилактика стресс-повреждений желудочно-кишечного тракта у больных в критических состояниях
Группу контроля составили пациенты с аналогичными данными, но получавшие в качестве профилактики СОПЖ в/в форму Нг-блокаторов (ацилок). В группе пациентов, получавших эзомепразол, признаков развития СОПЖ выявлено не было. В контрольной группе пациентов, получавших Нг-6локаторы, было зафиксировано 4 слу чая развития стресс-повреждений верхнего отдела ЖКТ (острые язвы, гастро-дуоденальные кровотечения). Полученные результаты, а также литературные данные, позволяют сделать вывод, что наиболее приемлемыми препаратами для профилактики СОПЖ представляются ингибиторы протонной помпы. У пациентов в крити ческих состояниях с высоким риском развития СОПЖ наиболее эффективным ИПП является эзомепразол в дозе 40 мг парентерально.
Протокол профилактики стресс-повреждения верхнего
отдела ЖКТ у больных
в критических состояниях
Решение вопроса о выборе средств и продолжитель ности профилактики синдрома острого повреждения верхнего отдела ЖКТ базируется на комплексном ана лизе клинической ситуации.
1.Оценка факторов риска и их значимости. Для больных, находящихся в ОИТ, в качестве этиопатогенетических факторов развития острого пов реждения верхнего отдела ЖКТ особое значение имеют ОДН, коагулопатия, артериальная гипотензия любого генеза, сепсис, особенно тяжелый. Наличие любого из этих нарушений является категорическим показанием к немедленному назначению средств профилактики стресс-пов реждений.
2.Возраст больного. Учитывая возрастные измене ния сердечно-сосудистой системы, возраст стар ше 65 лет может служить противопоказанием для
применения блокаторов Н2-рецепторов, которые обладают отрицательным инотропным и хронотропным действием.
3.Наличие сопутствующих заболеваний или органных расстройств, влияющих на фармакодинамику и фармакокинетику применяемых лекарственных средств. Эцефалопатия любого генеза является относительным противопоказа нием для применения блокаторов ^-рецепто ров, поскольку эти препараты могут влиять на
ментальный статус. Сопутствующая печеночная и
почечная недостаточность служат дополнитель ными факторами развития стресс-поражений ЖКТ и, следовательно, являются показаниями к анти секреторной профилактике стресс-повреждений.
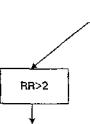
Учитывая изложенное, следует признать, что оптимальным фармакологическим средством профи лактики в настоящее время представляется приме нение внутривенных ингибиторов протонной помпы. Продолжительность профилактического использования этих препаратов зависит от длительности действия фак тора риска. При стресс-язвах необходимо их назначе ние в течение всего времени действия факторов риска их развития; при гастро-дуоденальных кровотечени ях — в течение 3-х суток после гемостаза (в этот пери од происходит > 80% рецидивов). Дозировка препара тов зависит от «повреждающей значимости» фактора риска. В частности, при дыхательной недостаточности, коагулопатии, тяжелом сепсисе доза внутривенного омепразола должна быть не менее 40 мг 2 раза в сутки, эзомепразола не менее 40 мг 1 раз в сутки. При наличии этиопатогенетических факторов меньшей значимости (RR < 2) доза омепразола может быть уменьшена до
40мг 1 раз в сутки, эзомепрзола до 20 мг.
Для профилактики стресс-язв следует использовать
болюсное введение внутривенного омепразола (40 мг в течение 10 минут) или эзомепразола (40 мг в течение 10—30 минут в виде инфузии). Для предотвращения рецидива или для лечения кровотечения — непрерыв ное внутривенное введение 80 мг омепразола в течение 15 мин, затем 8 мг/ч в течение 72 ч, в дальнейшем 20 мг per os до эндоскопического заживления. Эзомепразол назначают в дозе 40 мг в течение 3-х минут болюсно, затем 40 мг в течение 10—30 минут в виде инфузии не менее 72 часов, по мере регрессирования факторов риска развития СОПЖ. 20 мг per os/сутки (рис. 1).
Профилактика желудочно-кишечных кровотечений дает значительный экономический эффект. При развив шемся кровотечении на одного больного дополнитель но требуется в среднем 6,6 гематологических исследо ваний, 10,8 флаконов компонентов крови, проведение эндоскопических процедур и, возможно, выполнение хирургического вмешательства. Все это увеличивает срок пребывания больных в ОИТ в среднем до 11,4 суток и более, а общая противоязвенная терапия составляет 23,6 суток (Cook DJ. и соавт., 1991).
Протокол лечения больных с развившимся крово течением должен включать применение ингибиторов протонной помпы, т.к. блокаторы Нг-рецепторов при кровотечении не эффективны. Наш клинический опыт свидетельствует об эффективности и целесообразности использования этого протокола в лечебной практике.
34 80 лекции по кнрур, »ц
881
Общие вопросы хирургии
Оценка факторов риска и их повреждающей значимости |
Повреждающий фактор |
(RR) |
|
(величина RR) |
|||
|
|
||
Возраст больного |
ОДН |
15,6 |
|
Наличие хронических и/или острых органных расстройств |
|
|
|
Коагулопатия |
4,3 |
||
|
|||
|
|
|
|
|
Гипотензия |
3,7 |
|
|
|
|
|
|
Сепсис |
2,0 |
|
|
|
|
|
|
Печеночная недостаточность |
1,6 |
|
|
|
|
|
|
Почечная недостаточность |
1,6 |
|
|
|
|
|
|
Энтеральное питание |
1,0 |
|
|
|
|
|
|
Глюкокортикоиды |
1,5 |
|
|
|
|
м
Ингибиторы протонной помпы
|
RFK2 |
омепразол 40 мг х 2 раза/сут |
омепразол 40 мг х 1 раз/сут |
или эзомепразол 40 мг х 1 раз/сут |
или эзомепразол 20 мг х 1 раз/сут |
:. 1. Протокол профилактики синдрома острого повреждения желудка (СОПЖ)
Протокол лечения кровотечений из верхних отделов ЖКТ (Lanas А. и соавт., 1995):
•Защита дыхательных путей:
—мониторинг дыхания;
—обеспечение проходимости дыхательных путей (при необходимости интубация трахеи).
•Поддержание гемодинамики:
—адекватный венозный доступ;
—инфузионная терапия;
—гемотрансфузия (при НЬ ниже 70 г/л);
—препараты плазмы, тромбоциты (по показа ниям),
ИПП внутривенно (Н2-блокаторы не эффективны):
—назогастральная интубация и лаваж желудка;
—клинико-лабораторный мониторинг;
—эндоскопическое обследование/лечение.
Стресс-повреждения верхнего отдела ЖКТ играют важную роль в патогенезе и исходах у больных с крити ческими состояниями. Клиническая настороженность и выявление факторов риска развития синдрома острого повреждения желудка позволяют своевременно начать профилактические мероприятия в отношении этих нередко фатальных расстройств. Профилактика должна носить комплексный характер, направленный на подде ржание и оптимизацию всех факторов, обеспечивающих структурную и функциональную целостность ЖКТ.
Литература
г1 Адо А.Д., Ado M.A., Пыцкий В.И. и др. (ред.). Патологическая физиология. М.: Триада-Х, 2000.
1.Бертрам Г. Катцунг. Базисная и клиническая фармаколо гия. Т. 2. Пер. с англ. М. — СПб., Бином — Невский Диалект. 1998.
882
Профилактика стресс-повреждений желудочно-кишечного тракта у больных в критических состояниях
'
6
7
и аков В.А. Ингибиторы протонного насоса: их свойства и 12. |
Fennerty M.B. Pathophysiology of the upper gastrointestinal |
|
пименение в гастроэнтерологии. М., ИКЦ «Академкнига», |
tract in the critically ill patient: Rationale for therapeutic |
|
2001 304 с. |
|
benefits of acid suppression / Crit. Care Med. 2002, v. 30(6), |
Лапина Т.Л. Клиническая фармакология и терапия. Том 11, |
p. 351—355. |
|
№2,2002. |
13. |
Geus W.P. Are there indications for intravenous acid-inhibition |
Литвицкий П.Ф. Патофизиология. М.: ГЭОТАР-Мед, 2002, т. 1,in the prevention and treatment of upper GI bleeding? /
752 с, т. 2,808 с. |
Scand. 3. Gastroenterol. 2000. Suppl. 232, p. 10—20. |
14. |
Lanas A., Artal A., Bias 3., et al. Effect of parenteral omep |
Хитрова Н.К., Саркисова Д.С., Пальцева М.А. Руководство |
razole and ranitidine on gastric pH and the outcome of |
по общей патологии человека. М.: Медицина, 1999, 728 с. |
bleeding peptic ulcer. J. Clin. Gastroenterot. 1995, v. 21(2), p. |
Andersson Т., Rohss К., Hassan-Alin M., Bredberg f. Pharma |
103—106. |
cokinetics and dose-response relationship of esomeprasole. 15. |
Lasky M.R., Metzler MM., Phillips 3.0. A prospective study of |
Gastroenterology, 2000, 118, A1210. |
omeprazole suspension to prevent clinically significant gast |
rointestinal bleeding from stress ulcers in mechanically ven tilated trauma patients / 3. Trauma. 1998, v. 44(3), p. 527— 533.
16. Raynard В., Nitenberg G. Is prevention of upper digestive system hemorrhage in intensive care necessary? Schweiz. Med. Wochenschr. 1999, v. 129(43), p. 1605—1612.
11.Cook D.J., Guyatt G., Marshall J., et al. A comparison of suc
ralfate and ranitidine for the prevention of upper gastrointestinal 18. Tryba M. Sucralfate versus antacids or H^antagonists for
bleeding in patients requiring mechanical ventilation: Canadian |
stress ulcer prophylaxis: A meta-analysis on efficacy and |
Crit. Care Trials Group. N. Engl. 3. Med. 1998, v. 338, p. 791—797. |
pneumonia rate/Crit. Care Med. 1991, v. 19, p. 942—949. |
883
ПАРАЗИТАРНЫЕ ЗАБОЛЕВАНИЯ
ВПРАКТИКЕ ХИРУРГА
Б.И. Альперович
Среди паразитарных заболеваний печени в практике хирурга чаще всего встречаются и имеют наибольшее значение эхинококкоз, альвеококкоз и описторхоз. По массовости инвазии, тяжести поражения печени и дру гих органов, частоте осложнений и неблагоприятному прогнозу они являются преобладающими.
Эхинококкоз
Заболевание зависит от попадания в организм и развития в нем личиночной стадии ленточного червя
Echinococcus granulosus. Это плоский червь длиной 2,7—5,4 мм из рода Echinococcinae, типа Plathelmintes.
Червь состоит из головки с 4 присосками и крючьями, которыми он прикрепляется к слизистой кишечника окончательного хозяина, и двух-трех члеников. Червь довольно примитивно устроен, питается за счет пита тельных веществ хозяина, имеет выраженную поло вую систему. Третий членик почти полностью занят маткой, содержащей 400—800 яиц паразита. Каждое яйцо имеет плотную хитиновую оболочку, содержащую личинку-зародыш, устойчивую к внешним воздействи ям. С момента заражения окончательного хозяина червь достигает половой зрелости через 60—100 дней и начи нает выделять яйца в окружающую среду.
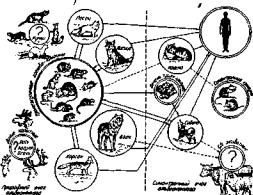
Цикл развития. Половозрелый червь живет в орга низме окончательного хозяина-собаки, где локализу ется в тонком кишечнике, прикрепляясь к слизистой. Количество червей может достигать нескольких тысяч. Яйца эхинококка естественным путем выходят во вне шнюю среду. Там они прикрепляются к шерсти собаки и рассеиваются, попадая на стебли растений и в воду стоячих водоемов. Промежуточными хозяевами эхино кокка являются домашние животные— овцы, коровы, свиньи, верблюды. Человек— промежуточный хозяин эхинококка, заражается случайно и является для пара зита биологическим «тупиком».
В организме промежуточного хозяина яйцо после попадания в желудок лишается хитиновой оболоч ки, которая растворяется желудочным соком, личинка освобождается и, пробуравливая стенку желудка или кишечника, попадает в кровь, которой заносится в капилляры печени. Там она задерживается в 75—80%.
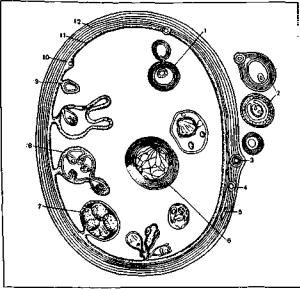
Если она минует капилляры печени, с током крови попа дает в капилляры легких, где локализуется в 10—15% случаев. Из большого круга кровообращения она может заноситься в любые органы и ткани. При заражении животных в организме их развивается пузырчатая ста дия паразита. После гибели животного или его забоя больные органы, пораженные эхинококком, поедают ся собаками, и цикл развития паразита завершается
(рис. 1).
Рис. 1. Цикл развития эхинококка
После заражения человека личинка, попавшая в печень, начинает активно делиться и превращается в комочек ткани, а через месяц в пузырек, достигая через 5 месяцев величины 55 мм. Рост ее в печени практичес ки неограничен. В печени человека пузыри эхинококка могут достигать величины до 10—20 и даже 30 литров.
Патологическая анатомия. В печени личинка эхи нококка довольно быстро превращается в пузырек-
884
Паразитарные заболевания в практике хирурга
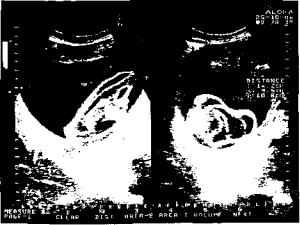
гидаткду, которая имеет определенное строение. Киста в печени наполнена прозрачной жидкостью, содержа щей янтарную кислоту. Стенка ее состоит из трех слоев. Внутренний слой эхинококковой кисты выстлан куби ческим эпителием (ростковым). Из него внутрь кисты отпочковываются дочерние пузыри паразита, которые в свою очередь отшнуровывают внутрь пузырей вну чатные и т.д. Кнаружи от росткового слоя располага ется хитиновая оболочка, внешне очень похожая на белок вареного яйца. Это продукт жизнедеятельности паразита. Кнаружи от этой оболочки лежит фиброзная капсула — плотная соединительнотканная оболочка, которая является продуктом жизнедеятельности хозя ина и служит барьером, которым он пытается отграни читься от паразитарной кисты (рис. 2). В эхинококковой жидкости материнского пузыря имеется «эхинококко вый песок»— большое количество головок-сколексов паразита. В 1 кубическом сантиметре «эхинококко вого песка» может содержаться до нескольких тысяч сколексов эхинококка. Они могут служить причиной рецидива заболевания после операций и основой для обсеменения брюшной полости при прорывах кист или попадании в брюшную полость во время оперативных вмешательств.
Рис. 2. Схема строения эхинококковой кисты в печени
Распространение. Эхинококкоз распространен, в основном, в странах с развитым животноводством. В ряде из них поражение людей достигло таких раз меров, что заболевание приобрело социальный харак тер. Наибольшее количество больных регистрируется в
Аргентине, Чили и Бразилии. В Аргентине регистрируется 7,5 случаев на 10 000 населения в год, в Австралии — 1,7, в Новой Зеландии — 1,1. Далее идет Северная Африка (Тунис). В Европе это— Италия, Греция, Югославия, Болгария, Исландия. В Болгарии заболеваемость состав ляет 1,1 на 100 000 населения в год.
На территории СНГ эхинококкоз встречается в Крыму, на Кавказе (Армения, Азербайджан), в Средней Азии (Казахстан, Киргизия, Узбекистан). В России эхи нококкоз распространен в среднем и нижнем течении Волги, в Западной Сибири, Якутии (Саха) и на Чукотке. В восьмидесятые годы заболеваемость в Якутии дости гала 11 на 100 000 населения в год.
Классификация и клинические проявления.
Эхинококковая киста, растущая в печени человека, ока зывает на организм хозяина механическое и биологичес кое воздействие. Механическое заключается в раздвига нии и сдавлении важных образований печени: сосудов ворот органа, желчных протоков и соседних органов. Биологическое действие состоит в сенсибилизации орга низма продуктами распада паразита и всасывании чуже родного белка. Кроме этого, в организме хозяина имеет место интоксикация из-за всасывания в кровь продуктов жизнедеятельности паразита. Все эти факторы определя ют клинические проявления заболевания.
Впрактической работе хирурга выгоднее пользовать ся классификацией, предложенной А.В. Мельниковым, который различает три стадии развития эхинокок ка: бессимптомную, выраженных изменений и стадию осложнений. Процесс протекает длительно, годами.
Впервой, бессимптомной стадии, когда киста еще малых размеров, у больных наблюдаются только сим птомы аллергизации организма, характерные вообще для глистной инвазии — крапивница, зуд кончика носа, появление папул на теле, сопровождающееся сильным зудом. Эти симптомы особенно выражены у детей.
Встадии выраженных изменений больные жалу ются на тяжесть и тупые боли в правом подреберье, диспепсические расстройства, увеличение печени. При объективном исследовании у них можно определить гепатомегалию, иногда локальное увеличение печени округлой формы, плотно-эластической консистенции, слегка болезненное при пальпации. Иногда при толч кообразных движениях рука исследующего ощущает дрожание, «шум дрожания гидатид», но этот симптом встречается редко.
Встадии осложнений происходит ряд изменений в кисте и окружающих органах, которые могут оказаться роковыми для больного. Среди осложнений эхинококка встречаются обызвествление кисты, ее нагноение и асептический некроз, механическая желтуха, порталь-
885
Общие вопросы хирургии
ная гипертензия; прорывы кисты в бронхиальное дере во, в брюшную или плевральную полость либо в полость перикарда. Частота осложнений обычно составляет 10—15%.
Эхинококковая киста вследствие гибели пара зита может частично или полностью подвергнуться обызвествлению. Тогда в печени располагается плот ный, каменистой плотности узел шаровидной формы. В 25—30% наблюдений наблюдается асептический некроз паразитарной кисты. При этом материнская киста может погибнуть, а часть дочерних кист остаться живыми. При инфицировании такой погибшей кисты происходит ее нагноение и клиническая картина этого осложнения напоминает проявления абсцесса печени: боли в правом подреберье, высокая температура, уве личение печени, воспалительная реакция со стороны крови. Когда киста достигает значительных размеров или при ее центральном расположении происходит сдавление элементов ворот печени, тогда у больного развивается портальная гипертензия с асцитом, пище водными и ректальными кровотечениями, расширением вен брюшной стенки («голова медузы»). При сдавлении желчных протоков развивается механическая желту ха с интенсивным окрашиванием кожных покровов и слизистых в желтый цвет, обесцвечиванием кала и потемнением мочи с соответствующими изменениями биохимических показателей крови (повышение уровня билирубина в сыворотке крови, появление уробилина в моче и отсутствие стеркобилина в каловых массах).
При прорыве кисты в плевральную полость раз вивается эхинококковый плеврит, в полость перикар да — перикардит, в брюшную полость— перитонит. Прорыв эхинококковой кисты в полости тела сопровож дается анафилактическим шоком, угрожающим непос редственно жизни пациента. Особенно он бывает выра женным при прорывах кист в брюшную полость. Если после этого больной остается жив (вследствие терапии или защитных сил организма), то ему все же угрожает опасность из-за того, что из каждого дочернего пузыря или сколекса, попавших в различные отделы брюшной полости, начинают развиваться вторичные кисты. Во время вмешательств по поводу этого осложнения при ходится удалять из брюшной полости несколько десят ков эхинококковых кист, часто вместе с пораженными ими органами (селезенка, кишечник, матка и т.д.).
Сравнительно редко (в 5—7% наблюдений) вследс твие развития реактивного плеврита легкое срастается с диафрагмой и при прорыве эхинококковой кисты вверх ее элементы попадают не в плевральную полость, а в просвет бронхов. Тогда у больного развивается желчно-бронхиальный свищ. Клинически такой прорыв
проявляется приступом сильнейшего кашля с выделе нием большого количества светлой мокроты и пленок от разорвавшейся хитиновой оболочки. После приступа и ликвидации симптомов аллергического шока паци ент начинает выделять большое количество мокроты желчного характера или чистую желчь. Количество желчной мокроты увеличивается после приемов пищи и в положении больного лежа. Такие больные могут спать только в положении сидя из-за того, что лежа захлебы ваются большим количеством желчной мокроты.
Перечисленные осложнения угрожают здоровью и жизни больного.
Лабораторные данные. При эхинококкозе в анали зах крови наблюдаются характерные изменения. Живая киста часто сопровождается эозинофилией, которая может достигать высоких степеней. Как и при всех оча говых поражениях печени, меняются белковые фрак ции — увеличивается количество альбуминов сыворот ки крови и уменьшается количество гамма-глобулинов. При механической желтухе возрастает уровень прямого билирубина сыворотки, а при печеночной недостаточ ности возрастают трансаминазы (АЛТ и ACT).
На особом месте при эхинококкозе стоят иммуно логические реакции. В 1911 году Tomaso Casoni ввел туберкулиновым шприцем больному 0,1 мл эхинокок ковой жидкости внутрикожно. В другое предплечье был введен физиологический раствор. На стороне вве дения эхинококковой жидкости появилась краснота и папула. Реакция получила имя автора. Жидкость для реакции берется из эхинококкового пузыря и использу ется после пропускания через фильтр Зейтца. Реакция положительна в 90% случаев эхинококкоза. Но она неспецифична и бывает положительной при других глистных инвазиях и туберкулезе. Для повышения спе цифичности реакции Казони предложено разводить эхинококковый антиген в 200 раз. Разработан также ряд иммунологических реакций (связывания компле мента, гемагглютинации и др.), однако с введением в
клиническую практику современных диагностических инструментальных исследований эти реакции потеряли свое былое диагностическое значение.
Диагностика эхинококкоза печени. Она достаточ но проста при знании врача о возможности заболева- « ния, тщательно собранном эпиданамнезе и использо вании специальных методов исследования. Во время сбора анамнеза выясняют наличие у больного собак и контактов ;с ними (общая постель, игры детей и пр.). Характер деятельности пациента также играет роль — чаще заболевают люди, имеющие по роду деятель ности контакты с животными (пастухи, ветеринарные работники, работники мясокомбинатов, охотники). При
886 |
т, |
|
Паразитарные заболевания в практике хирурга
t
•Л |
|
•\; |
клиническом обследовании выясняют у больного нали- |
-% |
чие аллергических реакций, гепатомегалии, желтухи, |
*асцита и других проявлений болезни.
*Специальные методы исследования дают возможность
к' |
верифицировать диагноз. Среди них безусловное пре |
|
имущество имеет ультразвуковое исследование. Метод |
^ |
достаточно точный, неинвазивный и информативный. |
4Исследование позволяет получить четкие данные о топог рафии патологического очага в печени, характере его и
!имеющихся изменениях. При этом видна киста в печени.
Нередко удается выявить наличие дочерних пузырей и к отслоенную хитиновую оболочку паразита {рис. 3). Этот I метод позволяет точно установить топографию кисты и i взаимоотношения кисты с элементами ворот печени и
,нижней полой веной, что имеет значение при планирова нии предстоящего хирургического вмешательства.
Рис. 3. УЗИ при эхинококкозе. Хорошо видна хитиновая оболочка паразита
Когда киста выходит на поверхность печени, при лапароскопии она представляется в виде белесоватой округлой опухоли в толще органа, похожей на биллиардный шар. Диагноз можно поставить визуально.
При радиоизотопном исследовании больному вводят бенгал-роз, меченный радиоактивным йодом. Дефект накопления радиофармпрепарата в печени соответс твует расположению кисты.
Изучение печеночного кровотока с помощью реогепатографии или допплеровского исследования позво ляет обнаружить отсутствие кровотока в зоне парази тарной кисты и усиление кровотока вокруг нее за счет оттесненных сосудов печени.
Рентгеновское исследование имеет особое значение в диагностике эхинококкоза. На обзорной рентгено грамме в зоне паразитарной кисты видна округлая тень,
иногда с полоской обызвествления по контуру тени. При дренирующейся кисте виден уровень жидкости в зоне затемнения. Контрастирование системы воротной вены позволяет выявить наличие кисты в печени. При этом кровеносные сосуды огибают ее по периферии, поскольку при росте ее киста сдвигает сосуды. Они огибают кисту наподобие кисти руки, держащей мяч. Артериография также позволяет выявить наличие кисты без сосудов в тени ее. При компьютерной томографии и спиральной компьютерной томографии на срезах в зоне печени определяется округлая тень, и можно выявить дочерние пузыри паразита. Метод позволяет обнару жить наличие округлого образования в печени, но не дает возможности точно определить характер его.
Сочетание клинико-лабораторного исследования со специальными методами, среди которых безусловное преимущество имеют ультразвуковое исследование и ангиография, дает возможность точно установить диа гноз эхинококкоза и правильно построить план пред стоящего лечения.
Лечение. Многочисленные попытки лечения эхи нококкоза лекарственными средствами пока не дали убедительных результатов. В 1951 году Cuervo Garsia сообщил о положительных результатах лечения забо левания с помощью препаратов пальмитиновой кис лоты. В СССР получен аналогичный препарат ТЭПАЛЬ (тимоловый эфир пальмитиновой кислоты). Но и он не дал убедительных результатов. В последние годы появились сообщения, свидетельствующие об эффек тивном применении мебендазола и его производных, но дороговизна препаратов и отсутствие значительного положительного эффекта делают пока хирургическое лечение эхинококкоза приоритетным.
История хирургического лечения эхинококкоза достаточно обширна. В 1874 году Folkman впервые про извел открытую двухмоментную эхинококкотомию. Во время лапаротомии он подшил края кисты к брюшной стенке, а во время второй операции вскрыл и опорож нил ее. В 1871 году Lindeman осуществил эту операцию
водин момент. В 1894 году одновременно А.А. Бобров
иPosadas произвели одномоментную закрытую эхино коккотомию. Во время операции киста паразита была вскрыта, опорожнена и после обработки полости ее формалином ушита, так же как рана брюшной стенки.
В1926 году СИ. Спасокукоцкий осуществил закрытую эхинококкотомию при нагноившемся эхинококке.
В1988 году Lawson впервые удалил кисту вместе с фиброзной капсулой, т.е. осуществил эхинококкэктомию. В 1887 году Loretta впервые произвел резекцию печени вместе с эхинококковой кистой. Подобная опе рация осуществлена Н.В. Склифосовским в 1918 году.
887
Общие вопросы хирургии
На современном уровне развития хирургии при эхинококкозе производятся следующие вмешательства. Все они имеют цель — удалить из печени паразитарную кисту. Это осуществляется различными путями. При одиночных кистах без дочерних пузырей в случаях расположения кисты на периферии печени допустимо
пункционное вмешательство, во время которого при пункции киста опорожняется и в полость ее вводится склерозант (Гальперин Э.И.). Методика малоинвазивна и эффективна. Но при этом следует учитывать возмож ности развития анафилактического шока при попада нии содержимого кисты в брюшную полость.
Наиболее распространенная операция — закрытая эхинококкотомия. Она практически осуществляется так же, как ранее ее производил А.А. Бобров. После лапаротомии вскрывается фиброзная капсула, и па разитарная киста удаляется вместе с содержимым и дочерними кистами (рис. 4). После этого стенки полос ти кисты обрабатывают формалином и ушивают кисет ными или узловыми швами для ликвидации большой полости. Во время операции некоторые хирурги реко мендуют иссекать выходящие на поверхность печени участки кисты (Вишневский А.А.). Операция доста точно проста и эффективна. Недостатком ее является сравнительно большой процент рецидивов заболева ния (от 10 до 45%). Это происходит либо из-за остав ления во время вмешательства сколексов паразита в полости кисты, либо из-за того, что при осложненном эхинококкозе в трещины фиброзной капсулы внедря ются сколексы эхинококка, которые и служат причи ной рецидива болезни. С целью избежать подобной ситуации ряд хирургов предлагают во время операции обрабатывать стенки фиброзной капсулы дезинфици
рующими веществами. Б.И. Альперович для этой цели использовал сверхнизкие температуры, разрушающие фиброзную капсулу.
Для предупреждения рецидивов эхинококкоза В.А. КубышкиниВ.А. Вишневский предложили шире при менять операцию удаления паразитарной кисты вместе с фиброзной капсулой (перицистэктомия). Современные средства гемостаза позволяют осуществлять это вмеша тельство при минимальной кровопотере.
Самой радикальной операцией при эхинококко зе является резекция печени, когда паразитарная киста удаляется в пределах здоровой ткани. Это вме шательство, безусловно, радикально, но достаточно травматично и не всегда доступно широкому кругу хирургов. Поэтому наша клиника считает показаниями к резекции печени при эхинококкозе краевое распо ложение кист, множественные кисты, занимающие доли или половины органа и рецидивный эхинококкоз. Использование при этих вмешательствах криотехники облегчает работу хирурга и увеличивает радикализм вмешательства.
При нагноившемся эхинококке, когда хирург не уве рен в полноценности удаления дочерних кист, прибегают к открытой эхинококкотомии, когда после опорожнения кисты и частичного иссечения стенок ее края фиброзной капсулы подшивают к брюшной стенке и в дальнейшем рана заживает вторичным натяжением (рис. 5).
Рис. Л. Закрытая эхинококкотомия. Удаление хитиновой |
|
оболочки кисты |
Рис. 5. Открытия эхинококкотомия . Схема операции |
|
888
Паразитарные заболевания о практике хирурга
Средняя летальность после оперативного лечения |
случаев. Собаки же заболевают альвеококкозом только |
эхинококкоза, по данным разных авторов, колеблется |
в 17,8%. После заражения песец начинает выделять яйца |
от 10 до 23%. Она особенно высока при множественном |
альвеококка на 22-й день, лисица — на 22—42-й дни. |
эхинококкозе и при операциях по поводу осложнений |
Яйца альвеококка попадают во внешнюю среду, где пое |
болезни. |
даются промежуточными хозяевами. Ими служат мыше |
Профилактика эхинококкоза складывается из |
видные грызуны из рода Microtinae. Это полевые мыши, |
государственных и личных мер. Государственная про |
суслики, крысы, лемминги, песчанки, нутрии и речные |
филактика проводится в странах с высокой заболева |
бобры. Человек является промежуточным хозяином аль |
емостью в государственном масштабе. Она дала сущес |
веококка. Он заражается случайно и представляет для |
твенное снижение заболеваемости в России, Греции, |
червя биологический «тупик». После заражения проме |
Исландии, Италии. Сущность мероприятий заключается |
жуточного хозяина в его организме развивается пузыр |
в том, что декретируется запрет на подворный забой |
чатая стадия червя. Окончательные хозяева заражаются, |
скота (овец, свиней, коров). Он должен осуществляться |
поедая промежуточных. |
под контролем ветеринарной службы, задачей которой |
Заражение человека происходит при обработке и |
является выбраковка внутренностей животных, пора |
выделке шкур убитых лисиц, песцов, волков, при сборе |
женных эхинококком. Пораженные внутренние орга |
ягод, грибов, питье воды из стоячих водоемов, обсеме |
ны должны сжигаться или обрабатываться негашеной |
ненных яйцами альвеококка {рис. 6). |
известью, чтобы их не могли съесть собаки. Служебные |
|
собаки должны подвергаться дегельминтизации дваж |
|
ды в год. Индивидуальная профилактика заключается в |
|
соблюдении правил личной гигиены. Особую осторож |
|
ность должны проявлять животноводы, пастухи и люди, |
|
работающие с собаками. |
|
Альвеококкоз
Заболевание, зависящее от попадания в организм и развития в нем личиночной стадии ленточного червя
Echinococcus multilocularis Leukart 1868. Если эхинококкоз известен человечеству со времен глубокой древ ности, то альвеококкоз стал предметом изучения толь ко в середине XIX века, когда Buhl, Luschka и Zeller
описали |
«коллоидный рак» печени или «карциному |
в фазе |
обратного развития». Только Rudolf Wirchov |
в 1856 году установил паразитарную природу этого заболевания. В середине XX века Rausch, Schiller, Vogel и Н.П.Лукашенко досконально изучили паразита, его цикл развития и особенности поражения человека. Альвеококк— плоский червь длиной 2—4 мм. Так же как эхинококк он состоит из головки с четырьмя при сосками и двух-трех члеников, последний из которых содержит матки с 200—400 яйцами. Каждое яйцо имеет плотную хитиновую оболочку, стойкую к внешним воз действиям. Червь также относится к роду Echinococcinae,
типу Plathelmintes.
Цикл развития. Червь обитает в тонком кишечнике окончательных хозяев — диких животных из семейства псовых: волков, рыжих и черно-бурых лисиц, песцов, кор саков. По данным Н.М. Губанова (1960) и М.Г. Сафронова (1962,1964), песцы поражаются альвеококком в 59—71%, красные лисицы— в 4,5—18%, черно-бурые— в 18%
О Промежуточна? lOMtto омЛюкиш |
•? ** А я м г Дяфмг |
Рис. 6. Цикл развития альвеококка (по Н.П. Лукашенко)
Патологическая анатомия. После попадания в желу док человека яйца альвеококка его оболочка растворя ется желудочным соком и личинка освобождается. Она проникает через стенку желудка или кишечника в кровь и током ее заносится в печень. Поскольку размеры личинки альвеококка намного превосходят диаметр печеночных капилляров, то она практически всегда задерживается в капиллярах печени. При альвеококкозе пузырек паразита имеет размеры от 2 до 5 мм. Размножается он почковани ем, но в отличие от эхинококка отшнуровывание пузырь ков происходит не вовнутрь материнского пузырька, а вовне его. Группа пузырьков альвеококка представляет собой «паразитарную опухоль». В результате взаимо действия с тканями хозяина она находится в строме из плотной соединительной ткани. Паразитарная «опухоль» представляет собой плотнейший конгломерат, не имею-
889
Общие вопросы хирургии
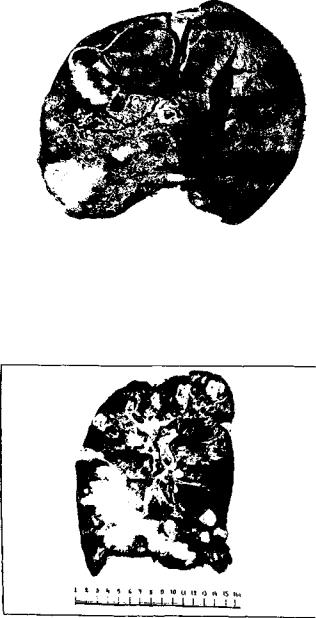
щий себе равных по плотности (Дедерер Ю.М.). Паразит выделяет фермент гиалуронидазу, растворяющий окру жающие ткани. Поэтому растущая по периферии парази тарная «опухоль» альвеококка обладает инфильтративным ростом, подобно злокачественной опухоли (рис. 7). Она прорастает в элементы ворот печени и соседние орга ны (диафрагму, легкое, перикард, желудок, надпочечник, почку, поджелудочную железу). Б.И. Альперович описал прорастание узла альвеококка в сердечную мышцу, пери кард и аорту.
Рис. 7. Узел альвеококка в печени
Прорастание паразита в кровеносные и лимфати ческие сосуды приводит к тому, что отдельные пузырь ки альвеококка отрываются и током крови и лимфы заносятся в регионарные лимфатические узлы, легкие (рис. 8) и головной мозг. Там они вновь начинают расти
Рис. Н. Метастазы альиеококка в легкие
и размножаться, образуя своеобразные метастазы. Все эти особенности роста альвеококка (способность давать рецидивы, прорастать в окружающие органы и давать метастазы) делают альвеококкоз заболеванием, похожим на злокачественные опухоли печени, с тем отличием, что паразитарная «опухоль» растет значи тельно медленнее злокачественной.
Поскольку паразитарная «опухоль» альвеококка питается за счет питательных веществ хозяина путем диффузии, то по периферии узла происходит бурный рост паразита, а в центре его за счет недостатка пита ния часть пузырьков погибает и подвергается распаду. В центре паразитарного узла образуется полость — паразитарная каверна, достигающая порой значитель ных размеров. Известны случаи прорыва полостей распада в брюшную, грудную и плевральную полости, а также в полость перикарда и в бронхиальное дерево. Все заканчивается гибелью больного от осложнений.
Распространение. Заболевание имеет четкий оча говый характер, и распространение его 8 мире доста точно ограниченно. Альвеококкоз встречается в Тироле и Баварии (ФРГ), на юге Франции в области Юрских гор, на Аляске, на острове Ребун и севере Японии (остров Хоккайдо), в Закавказье (Армения, Азербайджан), в Кир гизии (область Кочкорской котловины). В России заболе вание зарегистрировано в Башкирии, Кировской области, Западной Сибири, Якутии (Саха), на Чукотке, Камчатке. Наибольшее количество больных (до 1000 человек) отме чено в Якутии, где в семидесятые годы XX века оно дости гало 11 на 1000 населения в год (Габышев П.П.).
Классификация альвеококкоза предложена Б.И. Альперовичем (1967). Альвеококкоз печени имеет три стадии: бессимптомную, неосложненного течения и стадию осложнений. Среди осложнений различают про растание в соседние органы, портальную гипертензию, механическую желтуху, желчно-бронхиальные свищи, метастазы в легкие и головной мозг, прорывы полостей распада в соседние полости (брюшную, плевральную, полость перикарда) и атипичные формы-маски (прорас тание в желудок и др.).
Клинические проявления альвеококкоза зависят от стадии процесса и тех патоморфологических изме нений, которые при этом происходят. В бессимптомной стадии паразитарный узел в печени имеет малые раз меры и ничем себя не проявляет, за исключением незначительных проявлений сенсибилизации организ ма. Это крапивница, кожный зуд. В крови в это время может быть эозинофилия. Узел, чаще располагающийся в IV сегменте печени, может быть выявлен при тщатель ной пальпации во время профилактического осмотра и при ультразвуковом исследовании.
890
