
хирургия 5 курс / книги / Savel'ev V.S. (red.) 80 lekcij po hirurgii (Litterra, 2008)(ru)(T)(K)(910s)(ISBN 9785982161190)
.pdfДИАГНОСТИКА И ЛЕЧЕНИЕ ЯЗВЕННЫХ ГАСТРОДУОДЕНАЛЬНЫХ КРОВОТЕЧЕНИЙ
Э.В. Луцевич, И.Н. Белов, Э.Н. Праздников
Экскурс в историю язвенной болезни желудка и двенадцатиперстной кишки едва ли следует начинать с трудов Гиппократа, несмотря на то что уже в них можно найти свидетельства о наличии такой болезни и ее осложнений. Основоположником учения о язве желудка справедливо считается Cruvellhier, обобщивший свой опыт по этой проблеме в трудах 1829—1835 гг. С тех пор долгие годы едва ли не главным, патогномоничным симптомом язвы желудка считалось желудочное крово течение. Разумеется, ни о каком хирургическом лечении болезни или ее осложнений в ту доасептическую пору речи не велось, и абсолютная монополия на консерва тивное, нехирургическое лечение больных с желудоч но-кишечным кровотечением сохранялась фактически до 90-х годов XIX века.
Первые попытки оперативного лечения больных с желудочно-кишечными кровотечениями в те годы обыч но заканчивались неудачей при всех видах хирургичес ких вмешательств (иссечение язвы, резекция желудка или пилорэктомия, перевязка основных сосудов желуд ка, прижигание или выскабливание язвы, гастроэнтеростомия, гастростомия, тампонада и др.). Поэтому неудивительно, что почти каждый случай благоприятно го исхода операции публиковался в литературе и под вергался обсуждению (Федоров СП., 1903; Юцевич О.А., 1906; Соловов П.Д., 1908; Van Kleef, 1882; Roux, 1893; Connel, 1904, и др.). Тем не менее тактика консерва тивного лечения желудочно-кишечных кровотечений продолжала господствовать, пока с коротким интерва лом одно за другим не появились сообщения Finsterer и Gordon—Taylor (1933—1935) об активном хирурги ческом подходе к лечению кровотечений, Meulengracht (1934) о кормлении больных как лечебном методе в период острого кровотечения и Hampton (1937) о ран нем рентгеноконтрастном исследовании верхнего отде ла пищеварительного тракта как эффективном методе диагностики причин желудочного кровотечения.
Существовавшая долгие годы догма исключительно консервативного лечения именно в эти годы начала разрушаться: лечить больных с желудочно-кишечными кровотечениями стали в хирургических стационарах, а хирурги все чаще стали прибегать к оперативному лече нию таких больных. Наиболее ярким сторонником актив
ной хирургической тактики, и не только в нашей стране, был СХ. Юдин. Но и в его многочисленных работах мно гократно повторялась мысль о трудностях диагностики желудочных кровотечений, а слова, что «в момент остро го кровотечения мы не имеем никаких прочных опорных пунктов для положительной диагностики язвы, кроме анамнеза», стали классикой на многие годы.
Сблизить позиции не только терапевтов и хирургов, но и разных хирургических школ, придерживавшихся иногда диаметрально противоположных точек зрения, могла лишь более точная диагностика. Она стала реаль ностью в 60—70-х годах прошлого века, благодаря широкому распространению современной эндоскопии.
Более 30 лет назад нами совместно с академиком В.И. Стручковым впервые в стране было сообщено об опыте фиброскопии при желудочно-кишечных крово течениях. Сразу стало очевидно (Савельев B.C.), что значение эндоскопического исследования при таких обстоятельствах преувеличить невозможно. Было установлено, что чем раньше от начала кровотечения выполняется исследование, тем выше его диагнос тическая эффективность. Стало ясно, что осматри вать пищеварительный тракт необходимо на возможно большем протяжении. Более того, сразу определилась возможность использования эндоскопов для местного воздействия на источник кровотечения. Уже тогда мы пришли к выводу, что сроки хирургического вмешатель ства при кровотечении в пищеварительный тракт долж ны определяться не эффективностью или безуспешнос тью консервативных лечебных мероприятий в течение 24—48 ч, как это было принято ранее, а данными эндоскопического исследования (продолжающееся во время исследования кровотечение, интенсивность его, диаметр кровоточащего или тромбированного сосуда, характеристика собственно источника кровотечения). Тем не менее потребовались десятилетия, чтобы эти истины стали общим достоянием.
Накопленный за 52 года опыт лечения 4829 больных лег в основу настоящего сообщения. В течение первых 20 лет (1949—1969 гг.), когда эндоскопический метод исследования практически не применялся, лечили 1973 больных. В течение последующих 32 лет (1969— 2001 гг.), когда эзофагогастродуоденоскопия стала
481
Абдоминальная хирургия
основным и практически единственным эффективным методом диагностики, лечили 2856 больных с желудоч но-кишечными кровотечениями различной этиологии. Что отличает эти 2 периода? К чему все мы пришли в решении сложнейшей проблемы?
1. Конечно же, успехи диагностики. Достаточно сказать, что число случаев кровотечений неустановлен ной этиологии сократилось почти в 20 раз. Из практики исчезли «слепые» резекции желудка при не установ ленном до операции источнике кровотечения. Ранее многие хирурги склонны были рассматривать всякое тяжелой степени кровотечение язвенным, в действи тельности же на их долю приходится не более 40% слу чаев. На второе место по частоте вышли кровотечения из острых язв и эрозий слизистой оболочки преиму щественно органов верхнего отдела пищеварительного тракта, составляющие до 10% всех кровотечений.
2. Изменилась возрастная структура пациентов с кровотечениями. Сегодня каждый третий больной — старше 60 и даже 70 лет. Особенно велика эта возрастная группа среди пациентов с острыми поражениями слизис той оболочки, обусловленными неконтролируемым при емом как стероидных, так и нестероидных противовос палительных медикаментозных средств при возрастных поражениях опорно-двигательного аппарата.
3.Ухудшились сроки госпитализации больных с желудочно-кишечными кровотечениями в первую оче редь за счет поздней обращаемости, во вторую — за счет диагностических врачебных ошибок на догоспи тальном этапе. Позже 24 ч с момента появления первых признаков кровотечения госпитализируются более 50% больных. Все без исключения случаи с невыявленной причиной кровотечения связаны с исследованием в условиях наступившего гемостаза.
4.К большому сожалению, хирурги добровольно уступили инициативу в диагностике и даже в решении тактических вопросов лечения врачам-эндоскопистам. Все чаще встречаются случаи, когда больные не полу чают лечение до тех пор, пока им не будет выполнено эндоскопическое исследование. Упускается драгоцен ное время для коррекции волемических нарушений. Забывается, что непременным условием успешности эндоскопии, особенно при тяжелом кровотечении, слу жит инфузионная терапия, проводимая одновременно
сисследованием. Хирурги зачастую даже не считают нужным присутствовать при исследовании, получая информацию только из протокола, заполненного эндос копистом, часто не имеющим хирургической подготовки
иопыта клинициста.
5.Технические возможности для визуализации источника кровотечения и методов воздействия на него
заметно расширились в последние годы. Это и исполь зование ширококанальных операционных торцевых панэндоскопов, операционных дуоденоскопов, видео эндоскопов, видеокапсул, применение эндоскопической ультрасонографии и допплеровской ультрасонографии, сочетанное применение гастро- и лапароскопии (биэндоскопические исследования).
6. Опыт показывает, что среди существующих многочисленных эндоскопических методик местного воздействия на источник кровотечения гемостаз при интенсивном кровотечении, пусть даже временный, обычно обеспечивается всего лишь двумя-тремя мето дами: диатермокоагуляцией с применением гидротермозонда, лазерной или аргоноплазменной коагуляцией и наложением клипс.
При массивном артериальном кровотечении из
язвы применяющиеся методики остановки кровоте чения с помощью эндоскопа в большинстве случаев неэффективны. Единственно правильной в тактичес ком отношении в лечении таких больных является экс тренная хирургическая операция.
7.Среди факторов прогноза рецидива кровотече ния эндоскопические данные являются определя ющими. Накопленный за многие годы коллективный опыт свидетельствует, что у больных, у которых дно язвы после кровотечения чистое, рецидив кровотече ния возможен в 5—7% случаев, а послеоперационная летальность при этом не превышает 2%. Когда язва полностью или частично заполнена свертком крови, рецидива кровотечения можно ожидать у 20% больных,
алетальность после экстренных операций достигает 5—7%. Когда же в дне язвы виден крупный тромбированный сосуд, рецидив кровотечения наступает у 40% больных, а послеоперационная летальность превышает 10%. Наконец, при продолжающемся струйном крово течении или подтекании крови из-под свертка крови, которое удается остановить при эзофагогастродуоденоскопии, рецидив кровотечения развивается у 50% боль ных, а послеоперационная летальность превышает 15%.
8.Несмотря на практически решенные вопросы диа гностики причин кровотечения, результаты лечения боль ных остаются неудовлетворительными. Надежды, возла гавшиеся на эндоскопию как метод достижения оконча тельного гемостаза, оправдываются не в полной мере.
Из изложенного следует, что наряду с огромными переменами, отличающими 2 периода последнего пяти десятилетия, остается нерешенной основная суть про блемы — улучшение результатов лечения, уменьшение общей и послеоперационной летальности.
Временами создается впечатление, что общие дости жения эндоскопии и желудочной хирургии оборачм-
482
Диагностика и лечение язвенных гастродуадекпт,иых крпппгт'чричЛ
ваются негативом в кардинальном решении всей про блемы. Действительно, на протяжении уже многих лет в литературе, с нашей точки зрения, преувеличивают ся возможности лечебной эндоскопии в обеспечении гемостаза при осложненной кровотечением язвенной болезни желудка или двенадцатиперстной кишки. Выросло уже не одно поколение хирургов именно такой ориентации.
Утверждая это, мы имеем в виду только массивные артериальные кровотечения из больших каллезных язв желудка или двенадцатиперстной кишки, составляющие примерно 5% всех язвенных кровотечений. О такой же частоте неудач эндоскопической установки кровотече ний сообщают практически все отечественные и зару бежные авторы. При менее выраженном кровотечении лечебная эндоскопия часто действительно оказывается эффективной, обеспечивая при неустойчивом гемоста зе и риске рецидива кровотечения возможность прове дения соответствующей предоперационной подготовки больного и успешного выполнения радикального хирур гического вмешательства.
Вместе с тем настойчивые попытки остановить
кровотечение, используя эндоскопические методи ки, приводят в конечном итоге к запоздалым в связи с глубокими изменениями гомеостаза оперативным вмешательствам, упущению благоприятных сроков их выполнения и высокой летальности, достигаю щей среди таких больных 70%.
Есть основания полагать, что успехи плановой хирургии (аппаратный шов и др.) способствовали фор мированию ложной точки зрения об относительной тех нической простоте и экстренных операций при язвен ных желудочно-кишечных кровотечениях. В результа те выполнение таких операций часто осуществляется недостаточно подготовленными хирургами, не всегда способными объективно оценить общее состояние боль ного и прогноз, успешно разрешить как тактические, так
итехнические проблемы.
С.С.Юдин, придавая опыту хирурга первостепенное значение, писал: «Кто будет делать предстоящую опера цию? Вопрос, который не стоит так остро ни в каком дру гом разделе желудочной хирургии». Задумываясь над ответом, невольно обращаешься к организации службы, скажем, кардиохирургии, где практически любой слож ности операция выполняется маэстро при самой высо кой ее не только технической обеспеченности.
Известно, что язвенные кровотечения среди других составляют большинство. Таких больных из 4829 наблюдавшихся в нашей клинике с желудоч ными кровотечениями было 48% в возрасте от 15 до 89 лет. Тяжесть кровопотери, согласно классификации
В.И. Стручкова и Э.В. Луцевича, была у 51,8% больных I степени, у 32,6% — II, у 11,4% — III и у 4,2% — IV степени. Источником кровотечения оказалась язва двенадцатиперстной кишки у 1192 больных, язва желуд ка и двенадцатиперстной кишки — у 29 (1,5%), язва гастроэнтероанастомоза — у 62 (3,5%). У 439 (9,1%) больных были выявлены острые язвы желудка или две надцатиперстной кишки. Подавляющее большинство больных с кровопотерей II, III и IV степени тяжести госпитализировались сразу в отделение реанимации.
Основной лечебной тактикой таких больных была инфузионно-трансфузионная терапия, которую при геморрагическом шоке начинали с введения кристаллоидных и коллоидных кровезаменителей, с последу ющим переливанием плазмы и эритроцитарной массы. Эндоскопический гемостаз считали важной составляю щей комплексной терапии.
Принципиально важным при лечении таких боль ных считаем поддержание круглосуточно рН желу дочного содержимого, равного 5,0—6,0, что может быть обеспечено внутривенным введением омепразола или фамотидина в течение 3 суток с переходом далее на таблетированные формы.
Не менее важно динамическое эндоскопическое наблюдение, мониторинг состояния язвы (обычно каж дые 24 часа в первые 3—4 дня госпитализации), что в сочетании с клиническими, гематологическими, волемическими и гемодинамическими данными позволяет более точно судить о тяжести кровопотери, прогнози ровать рецидив кровотечения и своевременно коррек тировать программу лечения.
Эндоскопический мониторинг не отягощает состо яния больного и всегда оказывается оправданным, высокоинформативным, способствующим определению целесообразности дальнейшего консервативного лече ния или принятия решения о необходимости хирурги ческого вмешательства.
Экстренной операции подвергнуты 74 (15%) боль ных. Срочная операция выполнена 114 (23%) пациентам. Плановые операции выполнены в 307 (62%) случаев.
Показанием к выполнению экстренной операции в любое время суток у больных с язвенным гастродуоденальным кровотечением (ЯГДК) считаем продолжа ющееся кровотечение, которое не удается остановить, используя и эндоскопические методики, рецидив на фоне проводимого лечения, угрозу рецидива кровотече ния при содержании гемоглобина до 80 г/л и гематокрита до 25% и отрицательную эволюцию язвы по данным эндоскопии. Практически показания к радикальному оперативному лечению при установленном источнике кровотечения, которым является язва с грубыми ана-
433
Абдоминальная хирургия
томическими изменениями, возникают одновременно с показаниями к заместительной гемотрансфузии.
Срочные операции выполняли чаще в первые 12— 24 ч после остановки кровотечения на фоне проводи мого лечения, в том числе и с использованием методик эндоскопического гемостаза больным с высоким риском рецидива кровотечения.
Плановые операции выполняли через 2—3 недели лечения больных в гастроэнтерологическом отделении.
При кровотечении из острых язв, даже при неод нократном его рецидиве, проводилось консервативное лечение, включавшее и применение эндоскопических методик. Подвергнуть операции при этом источнике кровотечения нам пришлось 31 (7%) пациента.
Что касается объема оперативного вмешательства, то у 80% наших больных выполнялась разного объема резекция желудка и у 20% (в основном в последние годы и у всех больных с острыми язвами) выполнялись органосохраняющие операции.
Главным требованием к операции при кровотече нии считаем удаление самого язвенного субстрата, обеспечивающее окончательный гемостаз. При ЯГДК операция не должна заканчиваться прошиванием крово точащего сосуда. Этот метод следует считать порочным, поскольку, по нашим наблюдениям, в 50% таких случаев наступает рецидив кровотечения в результате прогресси рующего некроза в патологическом очаге и аррозии того же сосуда. У 2/3 таких больных осложнение приводит к летальному исходу. Заканчивая операцию по поводу
желудочно-кишечного кровотечения, хирург должен быть уверен, что кровотечение не повторится. При операции прошивания, особенно каллезных, глубоких, больших размеров язв, такой уверенности никогда не бывает. Допустимым прошивание кровоточащего сосуда с оставлением субстрата язвы может быть, на наш взгляд, только в случаях крайней тяжести больного, когда риск расширения объема операции угрожает жизни пациента. Такую операцию следует относить к категории операций отчаяния, альтернатива которой в конкретной ситуации не просматривается.
При кровотечении из хронической язвы желуд ка методом выбора хирургического лечения счи таем резекцию желудка, хотя при исключительных обстоятельствах, связанных с крайней степенью риска радикального вмешательства и продолжительности операции, допускаем возможность иссечения язвы, так называемую экстрагастрацию.
Во всех случаях кровотечения из язв двенадцати перстной кишки считаем правомочным выполнение резекции желудка, отдавая предпочтение иссечению язвы путем так называемой экстрадуоденизации.
Принципиально важным считаем обработку культи две надцатиперстной кишки открытым способом под визу альным контролем с тем, чтобы иметь полную уверен ность в иссечении язвы. Общая летальность составила 4,8%, послеоперационная — 6,1%.
Публикуемые в литературе цифры летальнос ти при язвенных кровотечениях существенно варь ируют в зависимости от возраста больных, сроков выполнения операции, тяжести кровотечения и др. Немаловажное значение в этом отношении имеет состав бригады оперирующих хирургов, их опыт и техническая подготовленность, а также профиль лечебного учреждения. Например по данным главно го хирурга Москвы (2006 г.), в 40 стационарах горо да послеоперационная летальность за последние 5 лет колебалась от 7 до 22%, достигая 55% среди больных пожилого и старческого возраста. По нашим наблюдениям, после срочных операций летальность составила 7,9%, после экстренных — 21,6%.
Внастоящее время существует мнение, что техничес кие проблемы хирургического лечения язвенных желу дочно-кишечных кровотечений исчерпаны. В определен ной степени с этим можно было бы согласиться. Между тем использование в диагностике эндосонографии, органосохраняющих вмешательств по типу так называемых экстрагастрации и экстрадуоденизации, применение метода биэндоскопических вмешательств и др. сулят новые перспективы, в том числе и в техническом реше нии этой сложной проблемы абдоминальной хирургии.
Вулучшении результатов лечения таких больных большие надежды возлагаются на широкое использо вание, в комплексе с хирургическим, методов медика ментозного лечения (антихеликобактерная, антисек реторная терапия и др.), эндоскопического гемостаза,
атакже эффективного прогнозирования риска рециди ва геморрагии.
Несомненно, важную роль в успешном решении про блемы язвенных гастродуоденальных кровотечений имеют социально-экономические факторы, успешное лечение заболевания на ранних этапах его развития, профилак тика осложнений. Одним из реальных путей улучшения результатов лечения этой категории больных, по нашему мнению, является концентрация их в специализированных центрах, имеющих и высококвалифицированных специ алистов и мощную материально-техническую базу. Эти центры уже существуют и доказали собственную значи мость. Объективный анализ работы таких центров помог бы выработать рекомендации для практических хирургов страны при лечении больных с кровотечениями из острых
ихронических язв желудка и двенадцатиперстной кишки
иулучшить результаты лечения.
484
и лечение язвенных гастродуоденальных нровотечениО
Литература
IЕрмолов А.С. Состояние экстренной хирургической помо щи при острых заболеваниях органов брюшной полости
вМоскве за 2001—2005 гг. и в 2005 г. Эндоскопическая хирургия, 2006, 6, с. 49—66.
2. Никифоров П.А., Базарова М.А., Никитин С.А. и др. Применение Н2-блокаторов в терапии кровотечений из гастродуоденальных язв / Хирургия. М„ 2001, № 10,
с.49—50.
3.Панцырев Ю.М., Михалев А.И., Федоров Е.Д., Кузеев Е.Л. Лечение язвенных гастродуоденальных кровотечений / Хирургия. 2000, № 3, с. 21—25.
4.Саенко В.Ф., Кондратенко П.Е., Семенюк Ю.С. и др. Диаг ностика и лечение острого кровотечения в просвет пищеварительного канала. Ровно, 1997, 383 с.
5.Тимошенко В.О. Новые технологии диагностики и лечения язвенных гастродуоденальных кровотечений. Авгпореф. дисс... д-ра мед. наук. М., 2002, 47 с.
6.Савельев B.C. и др. Руководство по клинической эндоско пии. 1985, 543 с.
7.Савельев B.C. и др. Руководство по неотложной хирургии органов брюшной полости. М.: Медицина, 1986, 606 с.
8.Эндоскопическая хирургия. Под ред. Савельева B.C. и др. М., 1998, 351 с.
9.Стручков В.И., Луцевич Э.В., Белое И.Н.. Стручков Ю.В.. Желудочно-кишечные кровотечения и фиброэндоскопия. М., 1977, 269 с.
Ю.Юдин С.С. Этюды желудочной хирургии. М., 1955. И.Яремчук А.Я., Зотов А.С. Современные принципы профи
лактики острых послеоперационных поражений желудоч но-кишечного тракта/Вест, хирургии, 2001, т. 160, № 3, С. 101—104.
485
ЭВОЛЮЦИЯ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ КРОВОТЕЧЕНИЙ ИЗ ВАРИКОЗНО-РАСШИРЕННЫХ ВЕН ПИЩЕВОДА И ЖЕЛУДКА
А. К. Ерамишанцев
Можно найти немного заболеваний, для лечения которых было бы предложено столь много оперативных вмешательств, как при портальной гипертензии (ПГ). Данное обстоятельство свидетельствует о чрезвычай ной сложности проблемы ПГ и о неудовлетворенности хирургов результатами операций, что и обуславливает постоянный поиск более эффективных методов лечения этого страдания.
Основное показание к операции при ПГ — лечение и профилактика кровотечений из варикозно-расши- ренных вен (ВРВ) пищевода и желудка, являющихся главной причиной летального исхода. Указанному симп тому «обязан» практически весь арсенал хирургических пособий, применяемых при этой болезни. Именно этим симптомом ПГ объясняется повышенный интерес хирур гов к обсуждаемой проблеме.
К 1980 году общее количество разработанных операций и их модификаций при ПГ превышало 100. В последующие годы их количество еще более увели чилось. Между тем, в связи с развитием и внедрением в клиническую практику ортотопической трансплантации печени у больных циррозом печени (ЦП), характер их изменился благодаря появлению «малоинвазивных» эндоваскулярных и эндоскопических технологий, поз воляющих получить недолгосрочный гемостатический эффект.
В России трансплантация печени делает лишь пер вые шаги. Поэтому хирургические методы лечения ПГ у больных ЦП еще длительное время будут иметь пер востепенное значение. Что же касается внепеченочной портальной гипертензии (ВПГ), то альтернативы опера тивному лечению этой патологии нет.
Собственные наблюдения более чем за 2000 опе рированными больными с ПГ позволяют проследить эволюцию хирургического лечения ПГ и подвести неко торые итоги почти 40-летнего периода работы с этим контингентом больных.
Началом хирургического лечения ПГ следует считать 80—90-е годы XIX века, когда в основу оперативного вмешательства была взята идея декомпрессии порталь ной системы, т.е. создания новых путей оттока крови
из воротной вены. Для решения этой задачи почти одновременно были предложены 2 типа операций: 1-й — оментопариетопексия, т.е. подшивание большо го сальника к передней брюшной стенке, автором кото рой, согласно данным литературы, является S. Talma (1898); и 2-й — сосудистый портокавальный анасто моз (ПКА), что было предложено Н.В. Экком (1877).
Идея Talma дала начало целому направлению в хирургии ПГ, названному «органоанастомозы», его сто ронники использовали для этой цели не только сальник, фиксируя его к печени, почке, полой вене, но и целые органы, такие как тонкая кишка, желудок, печень, селе зенка, подшивая их в зависимости от уровня блока друг к другу, к легкому, диафрагме, мышцам, брюшной стенке. Сравнительно простая техника вышеуказанных операций способствовала их широкому распростране нию в клинической практике. При этом подавляющая часть хирургов совмещала их со спленэктомией или перевязкой селезеночной артерии, мотивируя такую комбинацию тремя обстоятельствами:
1)уменьшением притока крови в портальную сис тему, а следовательно, и снижением портального давления;
2)улучшением артериального кровообращения печени вследствие перераспределения потока крови в системе чревной артерии, что должно было улучшить функцию цирротической печени;
3)коррекцией гиперспленизма, часто сопутствую щего спленомегалии.
Следует заметить, что спленэктомия в комбинации с органоанастомозами среди российских хирургов и хирургов бывшего Союзного государства, так же как и в нашем отделении, была операцией выбора в течение как минимум 3-х десятилетий (1950—1980 гг.) при лече нии больных ПГ.
Изучение данных литературы и многолетний личный опыт показали малую эффективность этих операций в борьбе с проявлениями ПГ, следствием чего явился практически полный отказ от их выполнения. Кроме того, как показали наши наблюдения, спленэктомия сопровождалась высокой послеоперационной леталь-
486
Эвотгцнч хирургического лечения кровотечений из паринозна расширенных вен пищеяодо и желудка
ностью, связанной с тромбозом сосудов портальной системы с последующим кровотечением из венозных вариксов и печеночной недостаточностью. Последняя в немалой степени была обусловлена и интраоперационной кровопотерей, достигающей в ряде случаев двух и более литров крови. Попытки ее уменьшения путем предварительной перевязки селезеночной артерии или дооперационной эмболизации артериального притока к селезенке ощутимых результатов не дали.
Будучи даже благополучно перенесенной, спленэктомия в ряде наблюдений осложнялась новым еще более тяжелым страданием — аспленической тромбоцитемией, требующей новых лечебных подходов.
Начиная с 1980 года мы подвергли ревизии наше отношение к спленэктомии, как самостоятельной опе рации, и резко сузили показания к ней, ограничив их тремя ситуациями:
1)сегментарной портальной гипертензией, когда основным проявлением болезни служат профузные кровотечения из ВРВ желудка в результате непроходимости селезеночной вены;
2)артерио-венозной фистулой между селезеночной артерией и селезеночной веной, т.е. когда причи ной ПГ является нагрузка объемом крови;
3)инфантилизмом у подростков, имеющих ЦП, у которых удаление селезенки больших размеров ведет к нормализации физических параметров организма.
При наличии ВРВ пищевода и желудка спленэктомия должна быть дополнена их прошиванием.
Гиперспленизм, т.е. нарушение в составе перифери ческой крови, в настоящее время не рассматривается в качестве настоятельного показания к спленэктомии, ибо повышение числа тромбоцитов и лейкоцитов после удаления селезенки совершенно не влияет на течение ПГ, а в ряде случаев ухудшает прогноз болезни, о чем мы уже указали выше.
В единичных наблюдениях у больных ЦП показа нием к спленэктомии может быть желтуха и анемия, когда имеются доказательства гемолиза эритроцитов. Опыт показал, что спленэктомия в этой ситуации бла готворно влияет на состояние больных и способствует улучшению функции печени. Вместе с тем подобные случаи редки (за последние 3 года мы оперировали одного такого больного); при наличии ВРВ спленэк томия должна обязательно сочетаться с операцией на пищеводе и желудке, иначе риск кровотечения из ВРВ остается.
Если слишком большие размеры селезенки препятс твуют выполнению прямого вмешательства на вари козных венах пищевода и желудка, осуществляемого с
целью лечения или профилактики гастроэзофзгеальных кровотечений, а сосудистый ПКА не показан или невы полним, спленэктомию можно признать оправданной операцией, без которой основное вмешательство ока залось бы неосуществимым.
В связи с низкой эффективностью органоанастомозов и спленэктомии при кровотечениях из ВРВ пищево да и желудка в хирургии ПГ появилась новая проблема. Она заключается в повторных операциях у больных с ВПГ, которые в отличие от больных циррозом печени имеют практически нормальную функцию печени, а при отсутствии кровотечений — продолжительность жизни, не отличающуюся от таковой у здоровых людей. Перенеся по нескольку операций, выполненных в других лечебных учреждениях страны, эти больные поступали в наше отделение в связи с рецидивами кровотечения из ВРВ пищевода и желудка без всякой надежды на выздоровление.
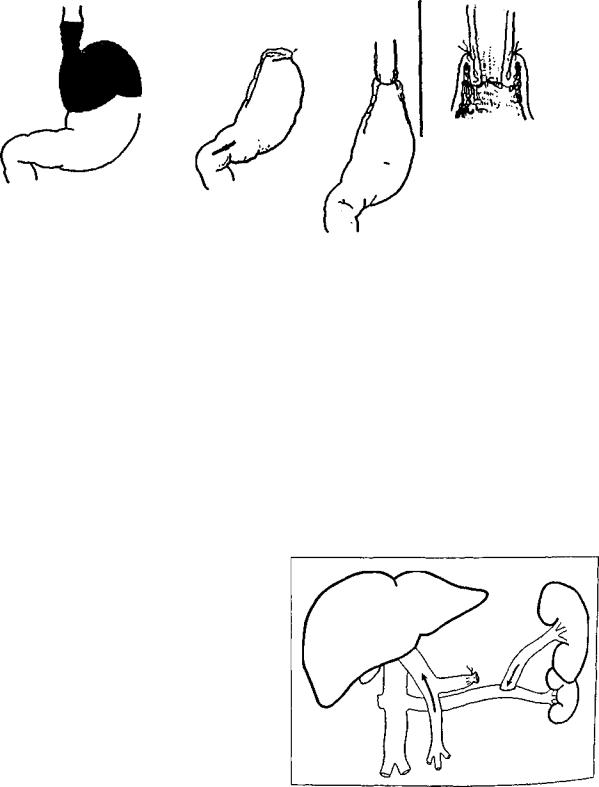
Вот почему, начиная с 1960 года, в нашем отделении операцией выбора у ранее оперированных больных, как правило, с ранее удаленной селезенкой, страдаю щих рецидивами, кровотечениями из ВРВ пищевода и желудка, становится резекция проксимального отдела желудка и дистального отдела пищевода (частичная эзофагогастрэктомия), т.е. участков пищеварительного тракта, являющихся в 95% случаев источником крово течения (рис. 1).
Первые операции частичной эзофагогастрэктомии в нашей клинике были выполнены проф. М.Д. Пациора в промежутке I960—1965 гг., однако из 9 больных 4умерли от несостоятельности швов пищеводно-желудочного анастомоза. И только с 1968 года после внедрения К.Н. Цацаниди инвагинационного метода пищеводного соустья непосредственные результаты этой операции значительно улучшились.
По данным мировой литературы 1960—1970-х годов, на эту операцию возлагались большие надежды как на наиболее радикальную, последнюю попытку борьбы с кровотечениями из флебэктазов пищевода и желудка, когда шунтирующие операции невыполнимы. К 1985 году мы имели опыт уже 80 подобных опера ций, однако анализ отдаленных результатов заставил нас отнестись к ее популяризации с осторожностью. У подавляющего большинства больных, перенесших эту операцию, развились диспепсические расстройства, которые в 42% сочетались с симптомами агастральной астении в виде значительной потери веса и анемии. Кроме того, серьезными осложнениями оказались эро- зивно-язвенные поражения культи желудка, которая в условиях нарушенного оттока крови служит источни ком рецидива кровотечений.
487
Абдоминальная хирургия
Рис. 1. Частичная эзофагогастрэктомпя. Этапы формирования ппщеводно-желудочпого анастомоза по Цацаниди
Вместе с тем у нескольких больных (9 случаев) срок наблюдения после операции уже превысил 30 лет; рецидивов кровотечения у них не отмечалось, больные сохранили трудоспособность при остающемся неболь шом дефиците массы тела. Анализ этих наблюдений не позволяет отказаться от этой операции, мы считаем ее показанной в тех редких ситуациях, когда другого пути помочь таким больным не остается. Возможно, что полное, а не частичное удаление желудка улучшит результаты этой операции за счет исключения тяжелой гастропатии со стороны остающейся культи этого орга на. Однако этот вопрос требует дальнейшего изучения.
Идея шунтирования портальной системы для боль ных ЦП сохраняет свою актуальность и по настоящее время. Между тем накопленный мировой и собствен ный опыт (более 450 операций за последние 20 лет) показал, что прямые ПКА между воротной и нижней
полой венами, радикально излечивая больного с ЦП от портальной гипертензии, как правило, влекут за собой ухудшение функционального состояния пече ни, следствием чего нередко является гепатоген ная энцефалопатия и смерть больного. Вот почему интерес к шунтирующим операциям у больных ЦП на длительное время угас и вновь возродился только после 50-х годов настоящего столетия, когда были предложе ны ПКА с «корнями» воротной вены — селезеночным и брыжеечным сосудами.
Однако и они сопровождались значительным чис лом осложнений, среди которых гепатогенной энцефа лопатии принадлежит основная роль. Позднее, в 1967 г., Warren была предложена операция «дистального спленоренального анастомоза» (ДСРА), суть которой
сводилась к шунтированию селезеночно-желудочного бассейна при сохранении кровотока по воротной вене (рис. 2), что позволило значительно улучшить результа ты шунтирующих операций. К этому времени было уже ясно, что, осуществляя декомпрессию портальной сис темы при ЦП, следует сохранять кровоток по воротной вене и что ДСРА позволяет решить эту дилемму. Вместе с тем анатомические условия редко позволяли осущес твить этот тип анастомозов. Кроме того, серьезным, иногда смертельным осложнением подобной операции был послеоперационный панкреатит.
Вот почему последующие годы в мировой практи ке, а в нашей клинике в основном с 1990 г. получают распространение так называемые «парциальные» сосу дистые ПКА, основной идеей которых становится огра-
Рис. 2. Дметальным гнлгнорсняльныи лнасгомол
438

хирургического лечения кровотечений из варикозно расширенных вен пищевода и желудка
ничение диаметра создаваемого портокавального соус тья, результатом чего будет не полный, а парциальный, т.е. частичный сброс портальной крови с сохранением остаточного проградного кровотока к печени. Практика показала, что оптимальный диаметр такого соустья должен находиться в пределах 8—10 мм. Последние 10 лет, осуществляя портокавальное шунтирование (ПКШ) у больных ЦП, мы выполняем ПКА указанного размера (130 операций). При этом стремимся осуществлять спленоренальный шунт в двух вариантах: Н-типа или «бок в бок» (рис. 3), избегая спленэктомии и трав-
мы поджелудочной железы. При удобном расположе нии селезеночной вены операцией выбора может быть ДСРА. Считаем, что для больных ЦП мезеитерикокаваль ный шунт (рис. 4) менее предпочтителен из-за более высокого риска развития энцефалопатии, но в ряде наблюдений по анатомическим условиям он является единственно возможным.
Отбор больных ЦП для выполнения сосудистого ПКА представляется наиболее ответственным моментом. Биохимические характеристики таких больных должны соответствовать параметрам группы А по Чайлду, а мар-
Рис. 3. Спленоренальный анастомоз Н-типа и «бок в бок
Рис. 4. Мезеитерикокавальный анастомоз Н-типа и
'" 80 лекций по хирургии |
489 |
Абдоминальная хирургия
керы цитолиза и сократительная функция миокарда — находиться в норме. Если имеются небольшие откло нения в биохимических показателях и больной может быть отнесен ближе к группе В или соответствует ей при нормальных показателях сократительной функции миокарда, то следует очень внимательно оценить нали чие латентной энцефалопатии, выявление которой
является абсолютным противопоказанием к нало жению шунта.
Кроме того, последние 10 лет мы придаем значение и показателям объемного кровотока по воротной вене. Как показали исследования, проведенные в отделении функциональной диагностики РНЦХ РАМН, объемный кровоток по воротной вене у здоровых лиц равен 897 ± 220,8 мл/мин, между тем как у больных ЦП, которых обследовали перед наложением сосудистого анас томоза, он был несколько ниже 739,75 ± 3 11,66 мл/ мин (р > 0,05). Ретроспективный анализ показал, что спустя 14—16 дней после выполнения парциального шунта кровоток плохо определялся или совсем не регистировался в тех наблюдениях, где в исходе он был существенно ниже нормы. Так, из 46 больных с наложенными парциальными шунтами при выписке из отделения кровоток по воротной вене не опре делялся у 8, у которых до операции он был равен или ниже 500 мл/мин. В отдаленном периоде, т.е. спустя 6 мес — 14 лет, из 39 обследованных нами больных ЦП и парциальными сосудистыми анасто мозами кровоток по воротной вене сохранился у 22 больных, у 17 он не определялся. Вместе с тем только у 3 из 17 больных результат операции оценен как неудовлетворительный, что выражалось в прогрессировании печеночно-клеточной недостаточности и последующим летальным исходом. Таким образом, парциальные анастомозы не гарантируют сохранения проградного кровотока к печени как в ближайшем, так и в отдаленном периодах. Однако клинические резуль таты их все же несопоставимы с тотальными ПКА, при которых портальный кровоток сразу или почти сразу прекращается. Следствием этого может быть резкое ухудшение функции печени, наступающее сразу после операции с последующей печеночной недостаточнос тью и смертью больного. Наши исследования показа ли, что частичная декомпрессия портальной системы у большинства больных сохраняет приток портальной крови к печени, хотя и редуцированный. В тех же
наблюдениях, где он не определялся, угасание его, как мы полагаем, происходило на протяжении более или менее длительного временного интервала, достаточ ного для адаптации печени к изменившимся условиям гемодинамики.
Изучая отдаленные клинические результаты парци альных ПКА у 78 больных ЦП в сроки от 6 месяцев до 14 лет, мы могли констатировать развитие энцефалопа тии в легкой форме в 23% случаев; при этом трудоспо собность сохранилась у 83% больных, работавших до операции. Пережили 2-летний срок 75% оперирован ных больных, 3-летний — 60%, из них 5-летний сроке момента операции — 50%. Основной причиной смер ти в отдаленном периоде было прогрессирование ЦП (19 больных) и рецидив кровотечения (4 пациента) вследствие тромбоза анастомоза. В течение первого года после операции умерли 9 из 19 больных, причем все они до операции относились к группе В по Чайлду и имели повышенные маркеры цитолиза.
Что касается больных с ВПГ, то, как показал наш опыт, диаметр и тип шунта не влияют на исходы операций. ПКШ для этой категории больных (более 300 операций за последние 20 лет) дает исключитель но хорошие результаты, полностью реабилитируя их от этого страдания. Между тем, отбирая больных с
ВПГ для шунтирующей операции, надо обязательно оценить сократительную функцию миокарда и, если
она скомпрометирована, от шунтирования следует отказаться.
При невыполнимости сосудистого анастомоза или наличии противопоказаний к его выполнению профи лактика и лечение кровотечений из ВРВ пищевода и желудка в настоящее время осуществляются с помо щью модифицированной проф. М.Д. Пациора операции Таннера (рис. 5). Она заключается в прошивании и перевязке вариксов дистального отдела пищевода и " проксимального отдела желудка путем гастротомии, выполняемой как из абдоминального, так и торакально го доступов. Из многочисленных операций такого типа, предложенных в мире, именно эта получила в России наибольшее распространение как наиболее простая в техническом отношении и непродолжительная по вре мени.
За последние 20 лет нами было выполнено 683 такие операции, из них в плановом порядке — 428 (62,7%) с общей послеоперационной летальностью 9,1%. При этом у больных ЦП она составила 13,6%, с ВПГ — 5,5%.
Комбинация этой операции со спленэктомией зна чительно повышала количество послеоперационных осложнений и летальных исходов. После ограничения показаний к спленэктомии общая летальность умень шилась и начиная с 1990 г. уже не превышала 6,1%.
При операциях, произведенных по срочным пока заниям, т.е. в период продолжающегося кровотечения, у 255 больных общая послеоперационная летальность достигла 31,4%. У больных ЦП она составила 39,3%, а с
490
