
- •Домашние задания по химии и методические указания по их выполнению для студентов дневной формы обучения
- •Содержание
- •Введение
- •Раздел 1. Основные классы неорганических соединений
- •Раздел 2. Газовые законы. Закон Авогадро и следствия из него. Уравнение Клапейрона-Менделеева. Моль. Молярный объём газов.
- •Примеры решения задач 71-82.
- •Раздел 3. Эквиваленты. Нахождение формул вещества. Стехиометрические расчеты.
- •Раздел 4. Строение атома и периодическая система д.И. Менделеева.
- •Раздел 5. Химическая связь и строение молекул
- •Относительная электроотрицательность атомов
- •Типовые задачи с решениями по разделу 5.
- •Раздел 6 Термохимия. Элементы химической термодинамики.
- •Раздел 7. Окислительно-восстановительные реакции.
- •Раздел 8 Скорость химической реакции. Химическое равновесие.
- •Примеры решения задач к разделу 8:
- •Раздел 9. Концентрации растворов. Коллигативные свойства растворов
- •Раздел 10. Растворы электролитов. Константа и степень диссоциации. Водородный показатель. Реакции ионного обмена. Произведение растворимости.
- •Типовые задачи с решениями по разделу 10:
- •Раздел 11. Гидролиз солей. Обменные реакции в растворах электролитов
- •Раздел 12. Электродные потенциалы. Химические источники электрической энергии.
- •Типовые задачи к разделу 12.
- •Раздел 13. Комплексные соединения.
- •Содержание
- •Литература
Раздел 7. Окислительно-восстановительные реакции.
Подобрать коэффициенты в приведенных ниже схемах реакций методом электронного баланса. Указать окислитель и восстановитель (301-350):
H2O2 + CrBr3 + NaOH
 Na2CrO4
+ NaBr + H2O
Na2CrO4
+ NaBr + H2OH2O2 + NaCrO2 + NaOH
 Na2CrO4
+ H2O
Na2CrO4
+ H2OKMnO4 + K2S + H2SO4
 MnO2
+ S + K2SO4
+H2O
MnO2
+ S + K2SO4
+H2OK2Cr2O7 + CrCl2 + H2SO4 → Cr2(SO4)3 + KCl + HCl + H2O
CrCl3 + Br2 + KOH
 K2CrO4
+ KBr + KCl + H2O
K2CrO4
+ KBr + KCl + H2OSb + KClO4 + H2SO4
 Sb2(SO4)3
+ KCl + H2O
Sb2(SO4)3
+ KCl + H2OMnO2 +KClO3 + KOH
 K2MnO4
+ KCl + H2O
K2MnO4
+ KCl + H2OI2 + KOH → KI + KIO3 + H2O
H2S + H2O2
 H2SO4
+ H2O
H2SO4
+ H2OHNO2 → HNO3 + NO + H2O
NiSO4 + KI + KIO3 + H2O
 Ni(OH)2
+ I2
+ K2SO4
Ni(OH)2
+ I2
+ K2SO4H2S + HIO3
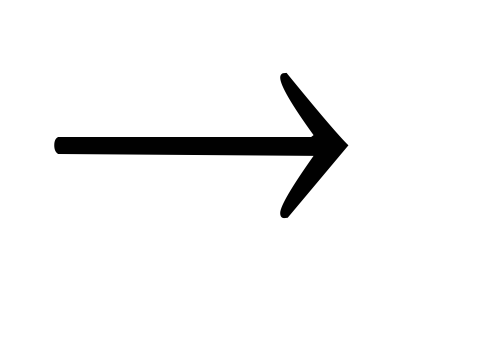 I2
+
S + H2O
I2
+
S + H2OAl + NaOH + H2O
 NaAlO2
+ H2
NaAlO2
+ H2
Pb + HNO3
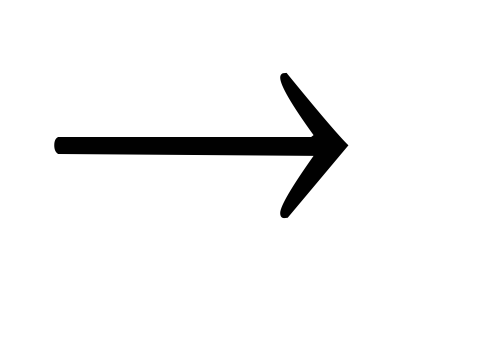 Pb(NO3)2
+
NO + H2O
Pb(NO3)2
+
NO + H2OW + NaNO3 + NaOH → Na2WO4 + NaNO2 + H2O
KMnO4 + Na3AsO3 + KOH
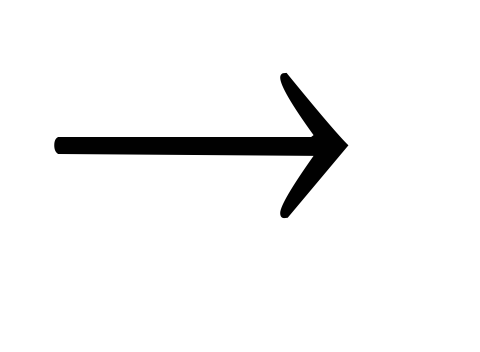 Na3AsO4
+ K2MnO4
+ H2O
Na3AsO4
+ K2MnO4
+ H2OKOH + Cl2
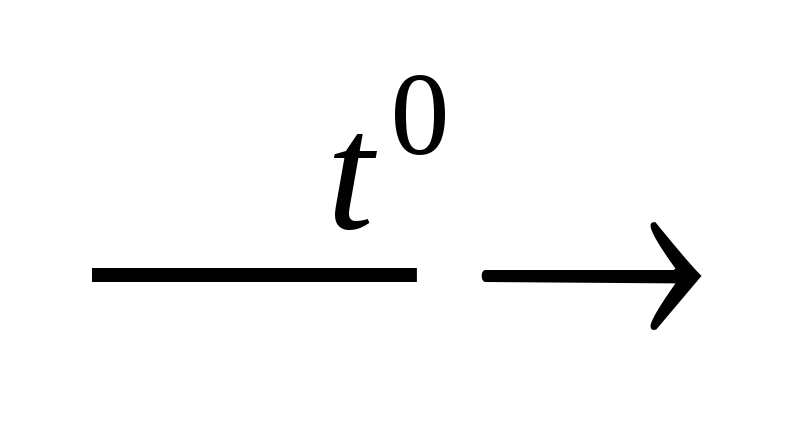 KCl + KClO3
+ H2O
KCl + KClO3
+ H2OP + HNO3 + H2O → H3PO4 + NO
KOH + Cl2 + MnO2
 KMnO4
+ KCl + H2O
KMnO4
+ KCl + H2OSi + NaOH + H2O → Na2SiO3 + H2
KOH + Cl2 + Fe(OH)3
 K2FeO4
+ KCl + H2O
K2FeO4
+ KCl + H2OZn + NaClO3 +NaOH
 Na2
Na2 Zn(OH)4
Zn(OH)4 + NaCl + H2O
+ NaCl + H2OAu + HCl + HNO3
 H
H AuCl4
AuCl4 + NO + H2O
+ NO + H2OOsO4+ HCl
 OsCl4
+ Cl2
+ H2O
OsCl4
+ Cl2
+ H2OK2Cr2O7 + KNO2 + H2SO4 → Cr2(SO4)3 + KNO3 + K2SO4 +H2O
FeSO4 + H2SeO4 + H2SO4
 Fe2(SO4)3
+ Se + H2O
Fe2(SO4)3
+ Se + H2OPbO2 + KI + HNO3
 KIO3
+
Pb(NO3)2
+ H2O
KIO3
+
Pb(NO3)2
+ H2OMnSO4 + K2CO3 + KNO3
 K2MnO4
+ KNO2
+
K2SO4
+ CO2
K2MnO4
+ KNO2
+
K2SO4
+ CO2Zn + KNO3 + KOH + H2O → K2[Zn(OH)4] + NH3↑
Na2SO3 + AuCl3 + H2O
 Au + NaHSO4+
NaCl + HCl
Au + NaHSO4+
NaCl + HClTlCl3 + SO2 + H2O
 TlCl + HCl +H2SO4
TlCl + HCl +H2SO4
Re + Cl2 + H2O
 HReO4
+ HCl
HReO4
+ HClReF6 + H2O
 HReO4
+ ReO2
+ HF
HReO4
+ ReO2
+ HFKNO2 + KI + H2SO4
 I2
+ NO + K2SO4
+
H2O
I2
+ NO + K2SO4
+
H2OAs2S3 + HNO3 + H2O
 H3AsO4
+ H2SO4
+ NO
H3AsO4
+ H2SO4
+ NOCu2S + HNO3
 Cu(NO3)2
+ S + NO + H2O
Cu(NO3)2
+ S + NO + H2OH2SO3 + HClO3
 H2SO4
+ HCl
H2SO4
+ HClNH3 + Br2
 NH4Br
+ N2
NH4Br
+ N2FeSO4 + HNO3 + H2SO4
 Fe2(SO4)3
+ NO + H2O
Fe2(SO4)3
+ NO + H2OHI + H2SO4
 I2
+ H2S
+ H2O
I2
+ H2S
+ H2OKNO2 + Zn + KOH
 NH3
+ K2ZnO2
+ H2O
NH3
+ K2ZnO2
+ H2OK2Cr2O7 + SnCl2 + HCl
 CrCl3
+ SnCl4
+ KCl + H2O
CrCl3
+ SnCl4
+ KCl + H2OK2Cr2O7 + SO2 + H2SO4
 Cr2(SO4)3
+ K2SO4
+ H2O
Cr2(SO4)3
+ K2SO4
+ H2OK2Cr2O7 + FeSO4 + H2SO4
 Cr2(SO4)3
+ Fe2(SO4)3
+ K2SO4
+ H2O
Cr2(SO4)3
+ Fe2(SO4)3
+ K2SO4
+ H2OKMnO4 + H3PO3 + H2SO4
 H3PO4
+ MnSO4
+ K2SO4
+ H2O
H3PO4
+ MnSO4
+ K2SO4
+ H2OKClO3 + HCl → Cl2+ KCl + H2O
H2O2 + FeSO4 + H2SO4
 Fe2(SO4)3
+ H2O
Fe2(SO4)3
+ H2OH2O2 + KMnO4 + H2SO4
 MnSO4
+ O2
+ K2SO4
+ H2O
MnSO4
+ O2
+ K2SO4
+ H2OCrCl3 + NaClO3 + NaOH
 Na2CrO4
+ NaCl + H2O
Na2CrO4
+ NaCl + H2OHNO3 + Ca
 Ca(NO3)2
+ NH4NO3
+ H2O
Ca(NO3)2
+ NH4NO3
+ H2O
Исходя из степени окисления элементов, укажите, какое из приведенных соединений может быть только окислителем, только восстановителем, обладает двойственными свойствами окислителя и восстановителя. Почему? (351-400):
|
|
|
