
- •Общие правила выполнения лабораторных работ
- •Кислотно-основные свойства оксидов и гидроксидов
- •Определение молярной массы газа
- •Определение молярной массы эквивалента металла
- •Определение теплоты химической реакции
- •Порядок выполнения работы
- •Опыт 3. Определение энтальпии реакции нейтрализации
- •Комплексные соединения
- •Скорость химических реакций
- •Смещение химического равновесия
- •Свойства растворов электролитов
- •Гидролиз солей
- •Окислительно-восстановительные реакции
- •Опыт 2. Окислительно-восстановительные свойства нитритов
- •Химические свойства металлов
- •Гальванические элементы. Коррозия металлов
- •Электролиз
- •Порядок выполнения работы
- •Жёсткость воды
- •Методы получения коллоидных систем
- •Коагуляция коллоидных систем
- •Концентрация растворов
- •1. Получите у преподавателя задание:
- •Таблица 2
- •1. Получите у преподавателя задание:
- •Приложения
- •Приложение 11
- •РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ В ВОДЕ
Вопросы для подготовки к защите лабораторной работы
1. Явная коагуляция золя BaSO4, полученного смешением растворов BaCl2 и K2SO4, наблюдается при добавлении растворов электролитов с минимальной концентрацией, моль/л: KCl (0,050), MgCl2 (0,032), Na2SO4 (0,055), Al2(SO4)3 (0,018). Изобразите структуру мицеллы данного золя.
2. Напишите схему мицеллы золя Cu(OH)2, если стабилизатором является сульфат меди(II). Какой электролит будет обладать наибольшей коагулирующей способностью для данного золя: NaCl, K2SO4, CrCl3, Ba(NO3)2, Na3PO4? Дайте мотивированный ответ.
ЛАБОРАТОРНАЯ РАБОТА №17
Концентрация растворов
Необходимые приборы и реактивы: набор ареометров, мерные цилиндры, коническая колба, технохимические весы, растворы H2SO4, NaCl, кристаллический K2Cr2O7.
Определение плотности раствора ареометром
Процентную концентрацию растворенного вещества можно вычислить путем измерения плотности раствора и последующего
нахождения его концентрации по табличным данным. |
|
|
|
||||
|
|
Плотность раствора |
определяют |
с |
|||
|
помощью ареометров с точностью до |
||||||
|
третьего десятичного знака. |
|
|
|
|||
|
|
Ареометр (рис.1) представляет собой |
|||||
|
стеклянный поплавок со шкалой плотности. |
||||||
|
Жидкость наливают в стеклянный цилиндр |
||||||
|
на ¾ его объёма и погружают в неё |
||||||
|
ареометр. При этом ареометр не должен |
||||||
|
касаться стенок цилиндра. Если шкала |
||||||
|
ареометра находится выше или ниже уровня |
||||||
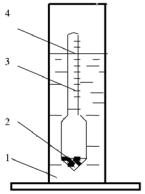
Рис.1. Определение плотности |
жидкости, следует взять ареометр с другими |
||||||
жидкости ареометром: |
пределами измерения. Значение на шкале, |
||||||
1 – изучаемая жидкость; 2 – |
до |
которого |
погружается |
ареометр, |
|||
балласт; 3 – шкала плотности; |
соответствует |
плотности |
жидкости. |
По |
|||
4 – уровень жидкости и |
окончании измерений ареометр промывают |
||||||
деление шкалы, соответст- |
|||||||
водой и убирают в коробку. |
|
|
|
||||
вующее ее плотности |
|
|
|
||||
|
|
Если значения плотности раствора по |
|||||
ареометру отсутствуют в таблице, концентрацию определяют интерполяцией.
45
