
- •Физические основы электроники
- •Тема 1 основы теории твердого тела
- •1.1.1 Виды связей
- •1.1.2 Кристаллическое строение веществ:
- •1.1.4 Дефекты кристалла
- •Контрольные вопросы к теме 1:
- •Тема 2 физические основы процессов в полупроводниковых материалах
- •2.1 Зонная модель полупроводников (пп). Вырожденные и невырожденные пп. Уровень Ферми в пп. Зависимость уровня Ферми от температуры, степени концентрации примеси
- •2.2 Понятие об электронно-дырочном переходе, типы переходов, токи в p – n переходе
- •2.3 Прямо смещенный p – n –переход.
- •Тема 2.4 Вольт амперные характеристики и p-n модель
- •2.4.1 Модель p-n , вах
- •2.4.2 Вольт – амперная характеристика
- •2.4.3 Физические процессы в контактах пп с различной шириной запрещенной зоны (гетеропереходы), металл - пп
- •2.4.4 Гетеропереходы
- •2.4.5 Люминесценция полупроводников
- •2.4.6 Фотопроводимость полупроводников
- •2.4.7 Эффект Холла
- •2.5 Эффект поля
- •2.5.2 Эффекты в структурах мдп
- •2.5.3 В идеальных мдп-структурах не учитывалось влияние зарядов в окисле и на границе окисел – кремний
- •3.1 Поляризация, электропроводность, диэлектрические потери, проницаемость
- •Виды поляризации: электронная, ионная, дипольно-релаксационная, ионно-релаксационная, самопроизвольная и др.
- •Ионная поляризация. Она возникает вследствие упругого смещения связанных ионов из положения равновесия на расстояние, меньшее постоянной кристаллической решетки.
- •Дипольно-релаксационная поляризация. Заключается в повороте (ориентации) дипольных молекул в направлении электрического поля.
- •Диэлектрики с ионной структурой. К ним относятся твердые неорганические диэлектрики с выше перечисленными поляризациями и делятся по потерям на 2 группы:
- •3.2 Электропроводность диэлектриков, диэлектрические потери, диэлектрическая проницаемость, электрическая прочность, виды пробоя в диэлектриках
- •Электропроводность. В твердых диэлектриках представляет собой сумму токов:
- •Пробой диэлектриков. Явление образования в диэлектрике проводящего канала под действием электрического поля называется пробоем. Различают два вида пробоя: полный и неполный.
- •Тепловой пробой. Обусловлен нарушением теплового равновесия диэлектрика вследствие диэлектрических потерь. Мощность, выделяющаяся в образце равна:
- •3.3 Сегнетодиэлектрики
- •3.4 Пьезоэлектрики
- •3.5 Активные диэлектрики
- •Вывод. При отсутствии внешнего поля сегентодиэлектрики представляет собой как бы мозаику из доменов – областей с различными направлениями поляризованности.
- •3.6 Электропроводность газообразных диэлектриков
- •4 Вида самостоятельного разряда:
- •Закон Пашека. Пробивное напряжение воздуха и других газов в электрическом поле является функцией произведения давления газа на расстояние между электродами:
- •3.7 Электролюминесценция, катодолюминесценция
- •Контрольные вопросы к теме 3:
- •Тема 4 физические эффекты в проводниках
- •4.1 Классификация проводников
- •4.2 Полукристаллические и аморфные металлы и сплавы. Особенности металлов в тонкопленочном состоянии
- •4.2.1 Медь
- •4.2.2 Алюминий
- •4.2.3 Железо
- •4.2.4 Натрий
- •4.2.5 Вольфрам
- •4.2.6 Молибден
- •4.2.7 Благородные металлы
- •4.2.8 Никель и кобальт
- •4.2.9 Свинец
- •4.2.10 Олово
- •4.2.11 Цинк и кадмий
- •4.2.12 Индий и галлий
- •4.2.13 Ртуть
- •4.3 Особенности металлов в тонко пленочном состоянии
- •Вольфрамобариевые катоды
- •Вторичная эмиссия
- •4.4 Сверхпроводящие проводники. Статический эффект Джозефсона. Применение сверхпроводимости
- •Применение
- •4.5 Контактная разность потенциалов, термо - эдс, эффекты.
- •Два закона:
- •Механизм возникновения
- •Контрольные вопросы к теме 3:
- •Тема 5 физические эффекты в магнитных материалах
- •5.2 Зависимость параметров от температуры. Свойства магнитных материалов в свч полях
- •Магнитодиэлектрики
- •Контрольные вопросы к теме 4:
- •Литература
Тема 1 основы теории твердого тела
Строение твердых тел
1.1.1 Виды связей
Все вещества – газообразные, жидкие и твердые – состоят из атомов и молекул. Способность атомов вступать в соединение с атомами других элементов и образовывать молекулы, обусловлены внешними валентными электронами.
Существующие виды связей:
а) ковалентная связь (рисунок 1.1) характеризуется образованием устойчивых электронных пар электронов, ранее принадлежавших отдельным атомам. Эти пары становятся общими для атомов, входящих в состав молекулы. Электроны при движении по молекулярной орбите чаще всего находятся между ядрами, где создается как бы избыток отрицательного заряда, что способствует сближению атомов.
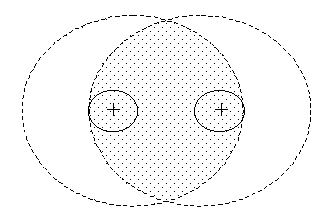
Рисунок 1.1 – Молекулы с ковалентной связью
Если двухатомная молекула состоит из атомов одного элемента (H2, N2, Cl2), то электронная пара в равной степени принадлежит обоим атомам, такую молекулу называют неполярной или нейтральной, у них центры положительных и отрицательных зарядов совпадают.
Если двухатомная молекула состоит из атомов различных элементов, то электронная пара может быть смещена к одному из атомов. Такую ковалентную связь называют полярной, а молекулу с полярной связью, у которой центры зарядов не совпадают, - полярными или дипольными. Дипольная молекула характеризуется величиной электрического дипольного момента, измеряемого в Кл·м:
![]() ,
,
где q – значение заряда, Кл;
l – расстояние между центрами зарядов.
Материалы с ковалентными связями характеризуются высокой твердостью, тугоплавкостью (Кремний).
б) ионная связь – вызывается силами электрического притяжения между положительными и отрицательными ионами. К ним относятся ряд металлов и типичные металлы. Например: хлористый цезий ClCs и титанита барий BaTiO3, оксиды Cu2O, ZnO, Fe2O3, NiO. Молекулы таких веществ – полярные, ионная связь менее прочная, чем ковалентная.
в) металлическая связь, в основном в металлах. Атом, отдавший внешний электрон, превращается в положительный ион, или вновь присоединяется, превращаясь в нейтральный атом. Т.е. металл можно рассматривать как систему, построенную из положительных ионов, находящихся в среде свободных электронов.
1.1.2 Кристаллическое строение веществ:
а) кристаллические – если атомы или молекулы характеризуются геометрически упорядоченным расположением;
б) аморфные (бесструктурные) – характеризуются хаотическим расположением;
в) аморфно – кристаллические, т.е. могут находиться как в кристаллическом, так и в аморфном состоянии (SiO2).
1.1.3 Кристаллические вещества – это большинство твердых веществ обладающих кристаллическим строением. Форма внутреннего строения – это геометрически правильное расположение атомов или молекул. Кристаллические решетки классифицируют по виду частиц и по форме элементарных ячеек. Возможны 14 видов пространственных решеток: триклинная, моноклинная, таллическая, тетрагональная, ромбоэдрическая, гексагональная, кубическая и т.д.
Триклинная – обладает наименьшей пространственной асимметрией, так как все ребра ячейки различны и не составляют между собой прямого угла.
Кубическая – наибольшая пространственная симметрия, так как ребра одинаковы, между собой составляют прямой угол.
Остальные - занимают промежуточные положения.
Кристаллические решетки обладают размерами, которые характеризуют ее параметр – это расстояние между ближайшими параллельными атомными плоскостями, образующими элементарную ячейку.
Параметр кубической решетки обозначают буквой, а≈0,28-0,6 Нм.
Параметр гексагональной решетки – обозначается двумя индексами: а – сторона шестигранника, с – высота призмы.
В зависимости от вида частиц, образующих кристаллическую решетку, различают: атомные, ионные, металлические и молекулярные решетки.
Атомные – в узлах нейтральные атомы связанные ковалентной связью.
Ионные – в них чередуются положительные и отрицательные ионы (ионная связь).
Металлические - в узлах положительные ионы, в промежутках – свободные электроны.
Молекулярные - в узлах молекулы, а связь – ковалентная и ионная.
