
- •Міністерство освіти і науки україни донецький національний технічний університет методичні вказівки
- •Міністерство освіти і науки україни донецький національний технічний університет методичні вказівки
- •1.1 Теоретична частина
- •Інструкція з техніки безпеки при виконанні лабораторних робот
- •1.2 Експериментальна частина
- •1.3 Звіт
- •1.4 Контрольні запитання
- •Додаток г
- •Додаток д Застосування евм в корозійних дослідженнях
- •1.5 Ситуація
- •Вплив зовнішніх факторів на газову корозію сталі та сплавів
- •2.1 Теоретична частина
- •Додаток б Десятибальна шкала корозійної стійкості металів та сплавів
- •Додаток в Закон росту оксидних плівок
- •Де Δm – збільшення маси зразку за час іспиту τ;
- •2.2 Експериментальна частина
- •2.3 Звіт
- •2.4 Контрольні запитання
- •2.5 Ситуація
- •10.4. Звіт
- •10.5. Контрольні питання
- •Лабороторна робота 3 Захист сталі і сплавів від газової корозії
- •3.1 Теоретична частина
- •3.2 Експериментальна частина
- •10.2 Мета роботи
- •10.3 Експериментальна частина
- •Визначення властивостей корозійностійких неметалевих покрить
- •10.1 Теоретична частина
- •3.2 Звіт
- •3.3 Контрольні запитання
- •3.4 Ситуація
- •Товщина досліджуємого металу, мм 0,1…3,0
- •9.3 Звіт
- •9.3 Контрольні питання
- •9.4 Ситуація
- •4.1 Теоретична частина
- •Прискорені методи корозійних іспитів оцинкованої сталі.
- •9.1 Теоретична частина
- •8.5. Ситуація
- •8.3. Звіт
- •8.4.Контрольні запитання
- •4.2 Експериментальна частина
- •Таблиця 4.1 - Об'ем газу, який виділяється, в залежності від тривалості електрохімічної корозії в розчині електроліту: температура °с; тиск гПа
- •Таблиця 4.2 - Показники електрохімічноі корозії вивчених сплавів у розчині електроліту за .......Рік
- •8.2 Експериментальна частина
- •4.3 Звіт
- •4.4 Контрольні запитання
- •4.5 Ситуація
- •Вплив зовнішніх факторів на електрохімічну корозію сталі та сплавів
- •5.1 Теоретична частина
- •Потенціостатичній метод вивчення корозійноϊ поведінки металевих матеріалів.
- •8.1 Теоретична частина
- •7.3. Зміст звіту
- •7.4 Питання для перевірки
- •7.5 Ситуація
- •7.1.3 Руйнування деревини
- •7.2 Експериментальна частина
- •7.1.2 Корозія бітумів
- •Контрольні запитання
- •Ситуація
- •Захист сталі та сплавів від електрохімічної корозії
- •6.1 Теоретична частина
- •Наслідку протекторного діяння. Для вуглецевої та низьколегованої сталі анодними покриттями є Zn та Cd. Металеві покриття наносять слідуючими методами:
- •Таблиця 1 – Стійкість деяких полімерів до агресивних середовищ
- •Корозія органічних матеріалів
- •7.1 Короткі теоретичні зведення
- •7.1.1 Корозія полімерів
- •Вплив зовнішніх факторів на корозію полімерів
- •6.2 Експериментальна частина
- •6.3 Звіт
- •6.4 Контрольні запитання
- •6.5 Ситуація
- •Необхідно виготувати патентировочну ванну для розплаву 50%
Таблиця 4.1 - Об'ем газу, який виділяється, в залежності від тривалості електрохімічної корозії в розчині електроліту: температура °с; тиск гПа
|
Час від початку іспиту, хв |
Матеріал та структура | |||
|
|
|
|
| |
|
Об’єм газу, що виділяється, м3 | ||||
|
|
|
|
| |
Таблиця 4.2 - Показники електрохімічноі корозії вивчених сплавів у розчині електроліту за .......Рік
|
Мате-ріал та струк-тура |
Роз-міри зразка, мм |
Поверх-ня зразка,м2. |
Маса зразка до іспиту,г |
Маса зразка після іспиту, г |
Об'ем газу що виді-лився, м3 |
Показники корозії | |||
|
Км, г/м2 *ч |
Коб, см3/(см2ч) |
Кn мм/хв |
І А/см2 | ||||||
|
|
|
|
|
|
|
|
|
|
|
Значення показників електрохімічної корозії для табл. 4.2 розраховують, користуючись дод. А. Групу стійкості матеріалу визначають, користуючись дод. Б.
За даними табл. 4.1 будуть графііки в координатах "Об'єм газу, що виділився – час", а за даними табл. 4.2 – у координатах " lg K - вміст елементу" або стовбчаті діаграми.
У висновках стисло оцінюють вплив внутрішніх факторів на електрохімічну корозію сталі та сплавів.
51
робочій електрод заземлюється потенціальним проводом. По цьому проводу не протікає струм і не створює, отже в робочому електроді падіння напруги, в результаті чого потенціал робочого електрода відносно електрода порівняння майже точно відповідатиме заданій величині.
Величина початкової напруги, а отже й потенціал робочого електрода можуть змінюватись ступінями або за лінейним законом.
Величина струму полярізації вимірюється міліамперметром мА.
Потенціостат може використовуватись також у режимі поідтримування потрібного значення струму полярізації робочого електрода.
Схему, що пояснює принцип роботи потенціостата у цьому режимі, наведено на рис. 8.3.
Р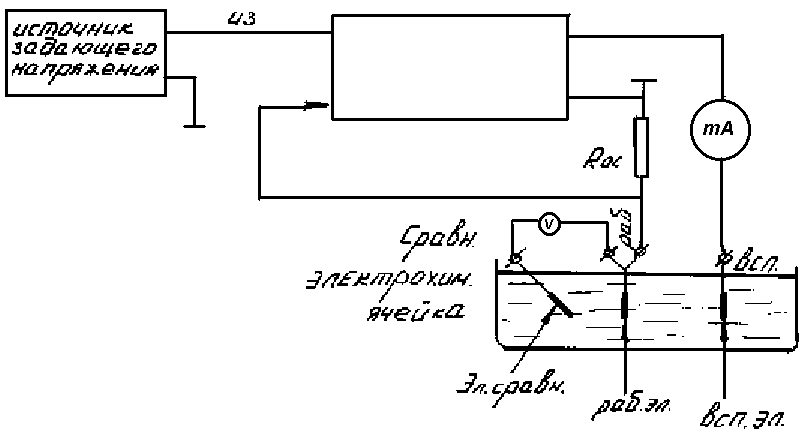 исунок
8.3 – Принципова схема роботи потенціостата
у режимі підтримування постійності
поляризуючого струму
исунок
8.3 – Принципова схема роботи потенціостата
у режимі підтримування постійності
поляризуючого струму
Зі схеми видно, що на один вхід підсилювача подається задаюча напруга, а на інший – падіння напруги, що створюється струмом поляризації на каліброваному опорі Rос.
Вхідні напруги в підсилювачі порівнюються, а одержана різниця керує вихідною напругою, підтримуючи задане значення струму поляризації.
Потенціал робочого електрода по відношенні до електрода порівняння при заданному струмі поляризації вимірюється вольтметром.
Як підсилювач, так і вольтметр повинні мати великі вхідні опори, які забеспечують струм споживання не більше 10-8 А, що необхідно для нормальної роботи електрохімічної комірки.
Величину і напрям поляризуючого струму можна регулювати зміною величини і полярності задаючої напруги.
50
8.2 Експериментальна частина
Будову та роботу потенціостату вивчають на прикладі потенціостату П-5827М.
Основною функцією потенціостата є підтримання потенціалу або поляризуючого струму досліджуваного (що далі іменується робочим) електрода на заданому рівні, незалежно від змін, що відбуваються у електрохімічній комірці.
Потенціостат підтримує заданий потенціал робочого електрода шляхом зміни виличини ( іноді й напряму) струму поляризації.
З потенціостатами використовуються електрохімічні комірки, що мають звичайно трьохелектродну систему, яка складається з електродів робочого і порівняння: по віднощенні до останнього вимірюється потенціал робочого електрода, а також допоміжнього, що створює з робочим ланцюг, через який проходить струм поляризації. Схему, що пояснює принцип дії потенціостата, наведено на рис. 8.2.

Рисунок 8.2 – Принципова схема потенциостатування
Зі схеми видно, що на один вхід підсилювача подається задаюча напруга, а на іншій – різниця потенціалів між електродом порівняння і робочим електродом. Вхідні напруги у підсилювачі порівнюються, і одержана різниця керує вихідним струмом підсилювача, що поляризує робочий електрод до потенціалу, який встановлено на джерелі задаючої напруги.
Похибка підтримування потенціалу робочого електрода визначається стабільністю підсилювача та коєфіціента його підсилення.
Для підвищення точності вимірювання та підтримування потенціалу робочого електроду у потенціостаті застосовано чотирьохпровідну схему вмикання електрохімічної комірки, в якій її
27
