
- •Министерство образования , науки, молодежи и спорта
- •Содержание
- •Раздел 1. Термические параметры состояния 6
- •Лекция №1
- •Введение
- •Раздел 1
- •1. Термические параметры состояния
- •1.1 Давление
- •1.2 Температура.
- •1. 3 Связь между параметрами состояния
- •1.4 Калорические параметры состояния. Внутренняя энергия
- •1.4 Параметры процесса Работа и теплота
- •Контрольные вопросы
- •2.2 Первый закон термодинамики для закрытой системы
- •Лекция № 3
- •Раздел 3
- •3. Основные термодинамические процессы идеального газа
- •3. 1 Законы идеального газа
- •3.2 Изохорный процесс
- •3.4 Изобарный процесс
- •3.5 Изотермический процесс
- •3.6 Адиабатный процесс
- •3.7 Политропные процессы и их обобщающие значения
- •Контрольные вопросы.
- •Лекція № 4
- •4. Второе начало термодинамики
- •4.1 Общие понятия
- •4.2 Круговые процессы ( циклы) тепловых машин
- •Цикл Отто
- •Цикл Дизеля
- •4.3 Устройство четырехтактного двигателя.
- •4. 4. Двухтактные двигатели.
- •4.5. Индикаторная мощность
- •4.6. Наддув.
- •4.7. Тепловой баланс и показатели экономичности двс.
- •4.8. Основные конструктивные элементы двс.
- •4.9. Термодинамический цикл газотурбинной установки (гту) с изобарным подводом теплоты
- •Контрольные вопросы.
- •Раздел 5
- •5. Общие свойства жидкостей и паров
- •5.1 Основные параметры состояния жидкости и пара
- •Теплота парообразования.
- •5.2 Диаграмма состояния воды и водяного пара I-s
- •Лекция № 6
- •Раздел 6
- •6. Влажный воздух
- •Лекция № 7
- •Раздел 7
- •7. Основы теплообмена
- •7.1. Общие понятия.
- •8.2. Перенос теплоты теплопроводностью через плоскую стенку.
- •Лекция № 8
- •Раздел 8
- •8. Конвективный теплообмен.
- •8.1 Подобие процессов конвективного теплообмена. Числа подобия.
- •Контрольные вопросы.
- •1. Закон Планка. Интенсивность излучения абсолютно черного тела js,λ и любого реального тела Jλ зависит от температуры т и длины волны λ.
- •3. Закон Стефана (1879 г.) – Больцмана (1884 г.).
- •9.2. Теплообмен между твердыми телами
- •При установке экрана
- •Контрольные вопросы.
- •Учебно-методические материалы
- •Конспект лекций Теоретические основы теплотехники
3.6 Адиабатный процесс
Основное условие адиабатного процесса dq = 0 или q = 0, т.е. в адиабатном процессе теплота к системе не подводится и не отводится от неё.
Однако в реальных условиях невозможно обеспечить условия, при которых теплообмен полностью исключен. Но применяя эффективную изоляцию рабочего тела от внешней среды можно свести к минимуму теплообмен и потерями тепла можно пренебречь. Например, процесс сжатия осуществляется настолько быстро, что теплоотдача не оказывает какого либо воздействия на его ход. Такой процесс можно считать адиабатным.
P

 T
1
T
1
 1 s =
const
1 s =
const

 q =
const =0
q =
const =0
 T
= const
T
= const
2 2

 0
0
V1 V2 V 0 S
Связь между параметрами процесса следующая
1. Уравнение самого процесса
q = 0; PVK = const , (3.13).
где К – показатель
адиабаты , равный
![]()
2. Связь между параметрами
![]()
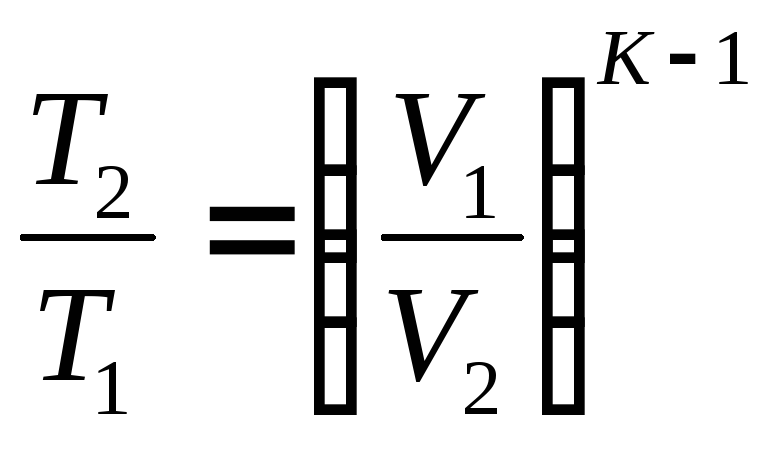 ;
;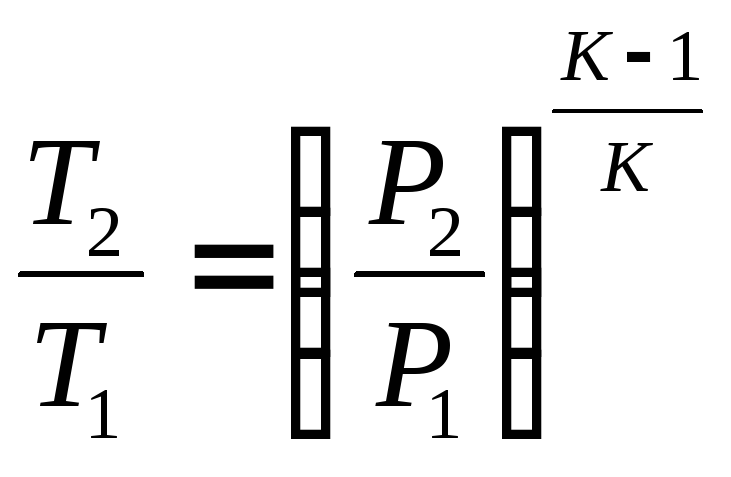 (3.14).
(3.14).
Изменение внутренней энергии
ΔU
= CV
(T2
– T1)
=
![]() Vm
Vm![]() (3.15).
(3.15).
Энтальпия
Δi
= CP(T2
– T1)
=
![]() Pm
Pm![]() (
3.16).
3.
Механическая работа
(
3.16).
3.
Механическая работа
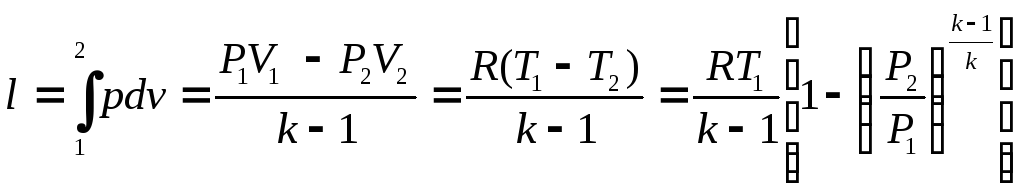
 (3.17).
(3.17).
6. Теплоёмкость
процесса
![]() (3.18).
(3.18).
7. Изменение энтропии.
ΔS = q/T = 0 ; S2 – S1 = const
Адиабатный процесс называют ещё изоэнтропным процессом.
Пример 3.4. Воздух массой 2 кг при давлении р1= 1МПа и температуре
t1 = 3000С расширяется по адиабате так, что его объем увеличивается в 5 раз.
Найти конечный объём, давление, температуру, работу изменения объема и изменение внутренней енергии. Принимаем R = 286,7 Дж/(кг·К).
Р е ш е н и е. 1. Находим начальный объём газа V1
V1 = mRT1/р1= 2*286,7*573/(1*106) = 0,33 м3.
По условию конечный объём V2=5 V1, поэтому
V2=5 · 0,33 = 1,65 м3.
2. Находим конечное давление р2 из уравнения
Р1/Р2 = (V2/V1)k
Примем для воздуха значение показателя адиабаты
k = 1,4, как для смеси двухатомных газов, тогда Р1/Р2 = 51,4 = 9,96.
Отсюда р2 = р1/9,96=1·106/9,96 ≈ 0,1МПа. Из уравнения состояния (3.3) найдем конечную температуру Т2=p2V2/ mR =0,1·106·1,65/(2·287,1) = =288 К или
t2 = 288-273=150С.
Для вычисления работы L1,2 используем уравнение (3.17) в упрощенном виде
L1,2 =m·R(t1 - t2)/( k—1) = 2·287,7(300-15)/(1,4 –1) = 419·103 Дж=419 кДж.
Изменеие внутренней энергии в адиабатном процессе равно работе изменения объёма, поэтом U2 — U1 = - L1,2= - 419 кДж.
