
- •Министерство образования , науки, молодежи и спорта
- •Содержание
- •Раздел 1. Термические параметры состояния 6
- •Лекция №1
- •Введение
- •Раздел 1
- •1. Термические параметры состояния
- •1.1 Давление
- •1.2 Температура.
- •1. 3 Связь между параметрами состояния
- •1.4 Калорические параметры состояния. Внутренняя энергия
- •1.4 Параметры процесса Работа и теплота
- •Контрольные вопросы
- •2.2 Первый закон термодинамики для закрытой системы
- •Лекция № 3
- •Раздел 3
- •3. Основные термодинамические процессы идеального газа
- •3. 1 Законы идеального газа
- •3.2 Изохорный процесс
- •3.4 Изобарный процесс
- •3.5 Изотермический процесс
- •3.6 Адиабатный процесс
- •3.7 Политропные процессы и их обобщающие значения
- •Контрольные вопросы.
- •Лекція № 4
- •4. Второе начало термодинамики
- •4.1 Общие понятия
- •4.2 Круговые процессы ( циклы) тепловых машин
- •Цикл Отто
- •Цикл Дизеля
- •4.3 Устройство четырехтактного двигателя.
- •4. 4. Двухтактные двигатели.
- •4.5. Индикаторная мощность
- •4.6. Наддув.
- •4.7. Тепловой баланс и показатели экономичности двс.
- •4.8. Основные конструктивные элементы двс.
- •4.9. Термодинамический цикл газотурбинной установки (гту) с изобарным подводом теплоты
- •Контрольные вопросы.
- •Раздел 5
- •5. Общие свойства жидкостей и паров
- •5.1 Основные параметры состояния жидкости и пара
- •Теплота парообразования.
- •5.2 Диаграмма состояния воды и водяного пара I-s
- •Лекция № 6
- •Раздел 6
- •6. Влажный воздух
- •Лекция № 7
- •Раздел 7
- •7. Основы теплообмена
- •7.1. Общие понятия.
- •8.2. Перенос теплоты теплопроводностью через плоскую стенку.
- •Лекция № 8
- •Раздел 8
- •8. Конвективный теплообмен.
- •8.1 Подобие процессов конвективного теплообмена. Числа подобия.
- •Контрольные вопросы.
- •1. Закон Планка. Интенсивность излучения абсолютно черного тела js,λ и любого реального тела Jλ зависит от температуры т и длины волны λ.
- •3. Закон Стефана (1879 г.) – Больцмана (1884 г.).
- •9.2. Теплообмен между твердыми телами
- •При установке экрана
- •Контрольные вопросы.
- •Учебно-методические материалы
- •Конспект лекций Теоретические основы теплотехники
3.7 Политропные процессы и их обобщающие значения
Понятие о политропных процессах широко используется при изучении процессов в газовых двигателях. Реальные процессы в этих машинах принимают промежуточное положение между частными процессами, рассмотренными выше, т.е. при постоянных P,V, T и адиабатный процесс. Политропными процессами наз. обратимые процессы, протекающие при постоянной теплоёмкости.
1. Уравнениями процесса являются
Сn = const или PVn = const (3.19).
где n –показатель политропы в пределах - ∞ < n < + ∞
Рассмотрим обобщающее значение политропы.
При pvn = const
1) n = 0; pvn = p =const → изобарный процесс;
2) n = 1; рv1 = рv = const→ изотермический процесс;
3) n=± ∞; рv∞≈
![]() v= р0v=v=
const→
изохорный процесс;
v= р0v=v=
const→
изохорный процесс;
4) n = k; рvk = const→ адиабатный процесс.
2. График процесса в Р-V координатах
Р




 n=±∞
n=±∞

n =0
 1<n<k
1<n<k
 n= к
n=1
n= к
n=1
V

3. Изменение внутренней энергии
ΔU
=СV
(Т2
– Т1)
=Сvm![]() Сvm
Сvm![]() ·t1
(3.20).
·t1
(3.20).
4. Изменеие энтальпии аналогично всем процессам, определяемым через изобары и теплоемкость.
5.
Механическая работа.
![]()
ℓ =
 (3.21).
(3.21).
6. Количество подведенного или отведенного тепла.
qn = Cn(T2 – T1) (3.22).
7. Теплоемкость процесса.
Сп
=
![]()
![]() (3.23).
(3.23).
8. Энтропия процесса.
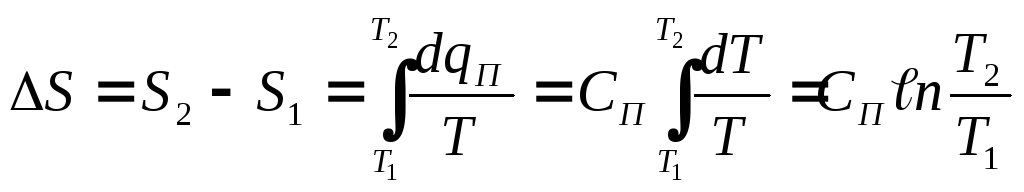 (3.24).
(3.24).




![]() (3.25).
(3.25).
9. Связь параметров

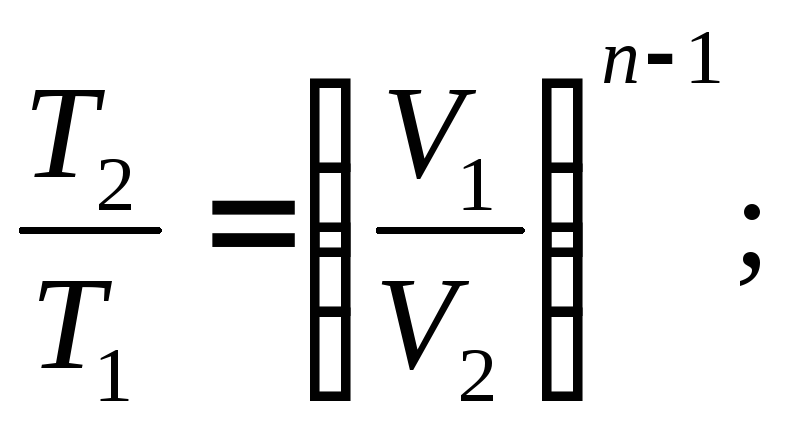 (3.27).
(3.27).
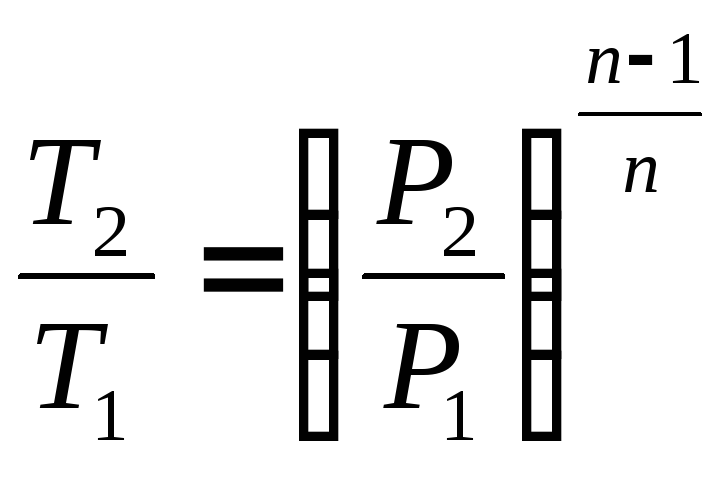 (3.28).
(3.28).
10. График политропного процесса в T-S координатах.





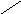 T
n=±∞∞
n=0
T
n=±∞∞
n=0
 n=1
n=1
n=k
S
Для практических целей используются политропные процессы с показателем политропы 1≤ n ≤ k. Значение политропы можно определить, если известны давления и объёмы в начале и в конце процесса по зависимости
ℓn p2 -ℓn p1 = n (ℓn v1 -ℓn v2); (3.29).
![]() (3.30).
(3.30).
Пример 3.5. Воздух с начальным объёмом 8 м3 и начальной температурой t1 = 200С сжимается по политропе с показателем n= 1,2 от абсолютного давления р1 = 0,09 МПа до давления р2 = 0,81 МПа. Найти конечную температуру, объём воздуха и работу изменения объёма.
Р е ш е н и е. 1. Находим конечную температуру из уравнения (3.28):
T2 = T1(p2/p1)(n—1)/n =293(0,81/0,09)(1,2—1)/1,2 = 293·90,167≈ 423 K, или t2 = 1500С.
2. Определяем конечный объем V2 из уравнения: р1v1/Т1 = р2v2/Т2, откуда
V2 = (V1·р1/р2)/(Т2/Т1) =(8·0,09/0,81)(423/293)=1,28 м3.
3. Находим работу изменения объема:
L1,2=(р1V1- р2V2)/(n -1)=(0,09·106·8 -0,81·106·1,28)/(1,2-1)=1,58·106 Дж или 1,58 МДж.
