Теплотехника_2 / Теплотехника Тесты на ПМК 1 ЕН
.rtfМІНІСТЕРСТВО АГРАРНОЇ ПОЛІТИКИ ТА ПРОДОВОЛЬСТВА УКРАЇНИ
ТАВРІЙСЬКИЙ ДЕРЖАВНИЙ АГРОТЕХНОЛОГІЧНИЙ УНІВЕРСИТЕТ
ТЕСТОВІ ЗАВДАННЯ
для проведення ЗМ-1 серед фахівців ОКР ″ бакалавр ″
2 курсу
напряму 6.050503 ″ Машинобудування″
з навчальної дисципліни ″ Теоретичні основи теплотехніки″
Мелітополь
2012
ТЕРМОДИНАМІКА
1. Наука, що вивчає процеси взаємоперетворення теплоти і роботи в теплових двигунах і машинах, а також теплофізичні властивості робочих тіл, які приймають участь у цих перетвореннях це:
термодинаміка;
+ технічна термодинаміка;
теплотехніка
теплопередача.
2. Робочими тілами в технічній термодинаміці служать:
тверді тіла;
+ гази;
рідкі тіла;
+ пара .
3. Сукупність матеріальних тіл, що знаходяться в енергетичній взаємодії між собою і зовнішнім середовищем, це:
рівноважний стан;
термодинамічний стан;
+ термодинамічна система;
критичний стан.
4. Певна кількість термодинамічних параметрів термодинамічної системи характеризує:
+термодинамічний стан;
термодинамічний процес;
термодинамічні харектеристики;
критичний стан.
5. Будь-яка зміна термодинамічного стану, це:
термодинамічний стан;
критичний стан;
+ термодинамічний процес;
термодинамічний параметр.
6. Термодинамічний процес відбувається в результаті обміну ____________ між термодинамічною системою і зовнішнім середовищем:
+ енергією;
молекулами;
масою;
ентальпєю.
7. Форма передачі енергії, обумовлена силовим впливом одного тіла на інше у процесі видимого спрямованого руху, це:
ентальпія;
+ робота;
теплота;
внутрішня енергія.
8. Форма передачі енергії, обумовлена різницею температур між тілами і хаотичним рухом молекул, це:
робота;
внутрішня енергія;
+ теплота;
ентальпія.
9. Загальною міра енергії в термодинамічній системі визначається таким параметром як:
внутрішня енергія;
робота;
теплота;
+ ентальпія.
10. Загальна зміна кількості переданої енергії від одного тіла до іншого визначається:
роботою;
внутрішньою енергією;
теплотою;
+ ентальпією.
11. Речовина, яка бере участь у термодинамічних перетвореннях, це:
+ робоче тіло;
теплове джерело;
термодинамічна субстанція;
вода.
12. Сумарна енергія всіх мікрочастинок ідеального газу, це:
потенціальна енергія;
внутрішня енергія;
кінетична енергія;
+ повна енергія.
13. Тиск ідеального газу є функцією:
+ температури;
маси;
теплоти;
питомого об'єму.
14. Внутрішня енергія реального газу залежить:
тільки від температури.
тільки від тиску.
тільки від питомого об’єму.
+ від тиску, питомого об’єму і температури.
15. Робота газу є функцією:
термодинамічного стану;
термодинамічного процесу.
температури;
+ параметрів стану
16. Згідно з одиницями SI роботу вимірюють у:
+ Джоулях.
кілокалоріях.
кілограмах.
кіловаттах.
17. Ентальпія ідеального газу є функцією:
+температури;
параметрів стану;
термодинамічного процесу;
тиску.
18. Основними термічними параметрами стану є:
тиск;
температура;
об'єм;
+ абсолютний тиск;
надлишковий тиск;
+ абсолютна температура;
+ питомий об'єм .
19. Термодинамічний стан робочого тіла, це:
співвідношення між внутрішньою енергією та зовнішньою роботою;
зв’язок тільки термічних параметрів;
зв’язок тільки калоричних параметрів;
+ зв’язок термічних і калоричних параметрів.
20. У термодинаміці при рівноважному стані робочого тіла, однаковими для нього мають бути:
тільки температури і тиски;
тільки всі термічні параметри;
+ термічні і калоричні параметри;
тільки калоричні параметри.
21.
Абсолютний тиск
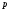 ,
питомий об’єм
,
питомий об’єм
 ,
абсолютна температура
,
абсолютна температура
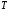 - це _____________ параметри.
- це _____________ параметри.
термодинамічні;
фізичні;
калоричні;
+ термічні.
22.
Внутрішня енергія
 ,
ентальпія
,
ентальпія
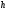 ,
ентропія
,
ентропія
 - це ______________ параметри.
- це ______________ параметри.
термодинамічні;
фізичні;
+ калоричні;
термічні.
23.
Відношення
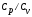 є показником:
є показником:
ізохори;
політропи;
+ адіабати;
ізотерми.
24. Основними формами передачі енергії від одного тіла до іншого є:
зміна калоричних параметрів.
+ робота і теплота.
зміна термічних параметрів.
величина потенціальної і кінетичної енергії.
25. У термодинаміці термічними параметрами стану робочого тіла є:
парціальний тиск, ентальпія і ентропія.
парціальний тиск, ентальпія і питомий об’єм.
+ абсолютний тиск, абсолютна температура і питомий об’єм.
парціальний тиск, температура і внутрішня енергія.
26. У термодинаміці калоричними параметрами стану робочого тіла є:
ентальпія, температура і питомий об’єм.
+ ентальпія, ентропія і внутрішня енергія.
ентальпія, ентропія і парціальний тиск.
ентальпія, питомий об’єм і парціальний тиск.
27. Політропний процес – це процес, що протікає при:
постійній температурі;
постійному тиску;
постійній ентропії;
+ постійній теплоємності.
28. Сила, яка діє на одиницю площі, це:
+ тиск;
робота;
густина;
енергія.
29. Середня сила, яка виникає в результаті ударів молекул об поверхню, що обмежує об'єм газу за нормаллю до неї і діє на одиницю поверхні, це:
кінетична енергія;
+ абсолютний тиск;
робота;
густина.
30. Основна одиниця вимірювання тиску в системі SI, це:
+ Паскаль;
Ньютон;
Ватт;
фізична атмосфера.
31. Один паскаль це:
кг/сек
Дж/м3
+ Н/м2
Н/м
32. Абсолютний тиск атмосферного повітря вимірюють за допомогою:
манометра.
+ барометра.
психрометра.
потенціометра.
33. Парціальним тиском компонента газової суміші називається тиск, який діє на поверхню, коли :
він має об’єм і ентальпію суміші.
він має об’єм і ентропію суміші.
він має об’єм і внутрішню енергію суміші.
+ він один займає об’єм суміші.
34. Тиск газової суміші дорівнює:
тиску окремого компонента суміші газів.
+ сумі парціальних тисків газів, що входять у суміш.
сумі добутків парціальних тисків газів на їх температури.
сумі добутків парціальних тисків газів на їх питомі об’єми.
35. Міра середньої кінетичної енергії поступального руху молекул називається:
+ абсолютним тиском ;
роботою;
абсолютною температурою;
тиском
36. Одиниця вимірювання абсолютної температури, це:
Дж;
+ Кельвін;
Вт;
°С.
37. Питомий об'єм газу визначають за формулою:
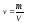 ;
;
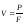 ;
;
+
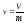 .
.
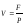
38. Густину газу визначають за формулою:
+
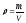 ;
;
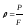 ;
;
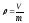 .
.
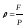
39. Об'єм, який займає 1 кг маси, називають:
певним об'ємом ;
+ питомим об'ємом;
парціальним об'ємом;
густиною.
40. Кількість кг маси, яка знаходиться в 1 м3 об'єму газу, називають:
+ густиною;
силою;
концентрацією;
об’ємом.
41. Одиниця вимірювання питомого об'єму, це:
+ м3/кг ;
м3/кмоль;
м3;
кг.
42. Одиницею вимірювання густини є:
 ;
;
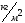 ;
;
+
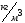 ;
;
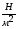 .
.
43. Ентальпія це:
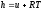
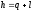
+
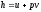
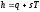
44. Зміну внутрішньої енергії газу визначають за формулою:
+
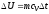 ;
;
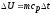 ;
;
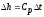 ;
;
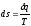 .
.
45.
Під час розрахунку кількості теплоти
для нагрівання речовини у формулі
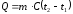 використовують теплоємкість:
використовують теплоємкість:
об’ємну.
+ масову.
мольну.
ізохорну об’ємну.
46. При постійному об’ємі питома теплоємність:
ізотермічна;
ізобарична;
адіабатична;
+ ізохорна;
політропна
47. Питому масову теплоємність газу визначають за формулою:
+
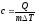 ;
;
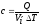 ;
;
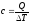 .
.
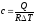
48. Питому об'ємну теплоємність визначають за формулою:
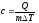 ;
;
+
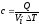 ;
;
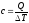 .
.
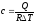
49. Кількість теплоти, яку слід підвести до тіла, щоб змінити його температуру на 1 градус, називають:
+ теплоємністю ;
питомою теплоємністю;
теплотою пароутворення;
питомою теплотою.
50. Кількість теплоти, яку треба підвести до 1 кг тіла, щоб змінити його температуру на 1 градус, називають:
питомою теплотою ;
+ масовою питомою теплоємністю;
теплоємністю;
теплотою пароутворення.
51. Кількість теплоти, яку треба підвести до 1м3 тіла за нормальних умов, щоб змінити його температуру на 1 градус, називають:
об'ємною теплотою ;
+ об'ємною питомою теплоємністю;
ізохорною теплоємністю;
питомою теплотою.
52. Кількість теплоти, яку треба підвести до 1 кмолю газу, щоб змінити його температуру на 1 градус, називають:
мольною теплотою ;
+ мольною теплоємністю;
питомою теплотою;
ізобарною теплоємністю.
53. Кількість теплоти, яку треба підвести до робочого тіла за сталого об'єму, щоб змінити його температуру на 1 градус, називають:
+ ізохорною теплоємністю;
питомою ізохорною теплотою;
об'ємною питомою теплоємністю;
ізобарною теплоємністю.
54. Кількість теплоти, яку треба підвести до тіла за сталого тиску, щоб змінити його температуру на 1 градус, називають:
питомою ізобарною теплоємністю;
+ ізобарною теплоємністю;
ізохорною теплотою;
питомою ізохорною теплотою
55. Залежно від температури із збільшенням температури теплоємність газу:
зменшується;
не змінюється;
+ збільшується ;
спочатку збільшується, а потім зменшується.
56. Теплоємність, яка відноситься до певного інтервалу температур і стала в цьому інтервалі, це:
+ середня теплоємність;
питома теплоємність;
стала теплоємність;
дійсна теплоємність.
57. Теплоємність для одиниці об’єму або маси називають:
сталою теплоємністю;
дійсною теплоємністю;
+ питомою теплоємністю;
середньою теплоємністю.
58. Рівняння Майєра:
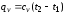
+
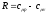
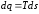
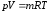
59. Кількість теплоти в термодинамічному процесі визначають за формулою:
+
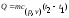 ;
;
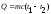 ;
;
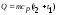 ;
;
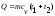 .
.
60. Ізобарний процес – це процес, який протікає при:
постійному об’ємі;
постійній температурі;
+ постійному тиску;
постійній ентропії.
61. Ізотермічний процес – це процес, який протікає при:
постійному об’ємі;
+ постійній температурі;
постійному тиску;
постійній ентропії.
62. Ізохорний процес – це процес, який протікає при:
+ постійному об’ємі;
постійній температурі;
постійному тиску;
постійній ентропії.
63. Адіабатний процес – це процес, який протікає без:
зміни температури;
зміни ентальпії;
+ теплообміну з навколишнім середовищем;
масообміну з навколишнім середовищем.
64. Рівнянням адіабатного процесу є:
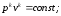
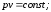
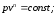
+
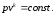
65. Рівнянням ізотермічного процесу є:
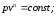
+
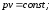
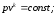
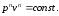
66. Рівняння політропного процесу в pv- діаграмі має вигляд:
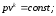
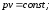
+
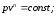
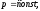
67. Робота в політропному процесі визначається за формулою:
+
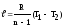
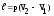
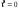
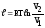
68. Перший закон термодинаміки встановлює:
+ незмінність сумарної кількості енергії в ізольованій термодинамічній системі.
перетворюваність потенціальної енергії робочого тіла у кінетичну.
перетворюваність теплової енергії в електричну.
перетворюваність хімічної енергії в теплову.
69. Перший закон термодинаміки: коефіцієнт корисної дії (к.к.д.) любого двигуна завжди менше ___________________
к.к.д. циклу Карно;
+ одиниці;
к.к.д. ідеального двигуна;
101%.
70. Перший закон термодинаміки: вічний двигун другого роду ___________
можливий;
+ неможливий;
можливий при певних умовах;
не спроектований.
71. Рівняння І закону термодинаміки має вигляд:
+
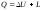 ;
;
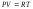 ;
;
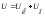 ;
;
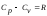 .
.
72. Основне рівняння стану, записане для 1 кг газу, має вигляд:
+
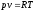
pVμ = μRT;
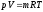
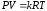 .
.
73. Основне рівняння стану, записане для всієї маси газу, має вигляд:
pv = RT;
pVμ = μRT;
+
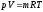 ;
;
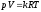 .
.
74. Основне рівняння стану, записане для 1 кмоль, має вигляд:
pv = RT;
+ pVμ = μRT;
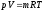
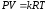
75. Який із наведених математичних виразів є виразом закону Бойля-Маріотта?
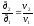 .
.
+
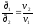 .
.
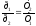 .
.
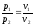 .
.
76. Який із наведених математичних виразів є виразом закону Гей-Люссака?
+
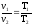 .
.
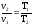 .
.
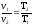 .
.
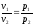 .
.
77. Який із наведених математичних виразів є виразом закону Шарля?
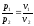 .
.
+
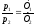 .
.
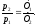
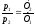 .
.
78. Закон Мендєлєєва-Клайперона визначається формулою:
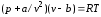
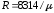
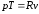
+