
- •Строение вещества
- •Методические указания для самостоятельной работы
- •Студентов всех специальностей и проведения
- •Практических занятий по химии
- •1 Строение атома
- •1.1 Современные представления о строении атома
- •1.2 Строение электронной оболочки атома
- •1.2.2 Принципы заполнения атомных орбиталей.
- •1.3 Электронные формулы элементов
- •1.4 Электронные семейства элементов
- •1.5 Атомная валентная зона. Возможные валентные состояния
- •1.6 Проскок (провал) электронов
- •2 Периодическая система элементов
- •2.1 Периодический закон
- •2.2 Современная структура Периодической таблицы Менделеева
- •2.3 Периодичность атомных характеристик
- •3 Химическая связь
- •3.1 Основные характеристики химической связи
- •3.3 Типы химических связей
- •3.4 Геометрия молекул. Гибридизация атомных орбиталей
- •3.5 Химическая связь в твердых телах. Кристаллические решетки
- •4 Вопросы и задания
1.4 Электронные семейства элементов
В зависимости от того, на какой подуровень попадает последний электрон, все элементы делятся на четыре семейства:
s - элементы—I-II группа главная подгруппа, а также водород и гелий;
p - элементы—III-VIII группа главная подгруппа, кроме водорода и гелия;
d - элементы— все побочные подгруппы I- VIII групп;
f - элементы— актиноиды и лантаноиды.
1.5 Атомная валентная зона. Возможные валентные состояния
Атомная валентная зона (АВЗ) – это часть электронной оболочки, которая может перестраиваться по ходу образования химической связи. АВЗ включает, как правило, внешний s– подуровень (ns) и тот подуровень, который заполняется у данного элемента (таблица 3).
Таблица 3 - АВЗ
|
Семейство |
АВЗ |
Максимально возможная валентность |
|
s |
ns |
1-2 |
|
p |
ns np |
1-8 |
|
d |
(n-1)d ns |
1-8 |
|
f |
(n-2)f ns |
1-8 |
Оставшаяся часть электронной оболочки в совокупности с ядром называется атомным остовом или химическим ядром.
Пример.
Определите возможные валентные состояния и укажите семейство для элементов с порядковыми номерами 11, 20, 8, 34, 22, 43, 28.
Запишем электронные формулы этих элементов, подчеркнём их АВЗ и для неё построим энергетическую диаграмму:

11Na 1s22s22p63s1 На внешнем энергетическом уровне у натрия находится только один электрон, поэтому он может проявлять только одну валентность, равную единице (В=1).
2 0Ca
1s22s22p63s23p64s2
На внешнем энергетическом уровне
у кальция находится два спаренных
электрона. А поскольку с точки зрения
спин–валентной теории участвовать в
образовании связи могут только свободные
электроны, то в стационарном состоянии
валентность кальция будет равна нулю
(В=0).
0Ca
1s22s22p63s23p64s2
На внешнем энергетическом уровне
у кальция находится два спаренных
электрона. А поскольку с точки зрения
спин–валентной теории участвовать в
образовании связи могут только свободные
электроны, то в стационарном состоянии
валентность кальция будет равна нулю
(В=0).
П ри
получении незначительного количества
энергииэлектроны
могут переходить с одного энергетического
подуровня на другой,
но только
в пределах своего уровня.
Энергия, затрачиваемая на распаривание
электронов, незначительна и окупается
энергией, выделяющейся при образовании
связи.
ри
получении незначительного количества
энергииэлектроны
могут переходить с одного энергетического
подуровня на другой,
но только
в пределах своего уровня.
Энергия, затрачиваемая на распаривание
электронов, незначительна и окупается
энергией, выделяющейся при образовании
связи.
В таком состоянии валентность кальция равна двум (В*=2).

8O 1s22s22p4 Поскольку здесь нет свободного d– подуровня на втором энергетическом уровне, то электроны распаривать некуда и кислород может быть только двухвалентен.

34Se 1s22s22p63s23p63d104s24p4 В=2. Но, не смотря на то, что и селен, и кислород стоят в одной группе, имеют сходное строение электронной оболочки и должны проявлять одинаковую валентность, оказывается, что у селена имеется свободный d– подуровень на четвёртом уровне, куда могут распариваться валентные электроны.
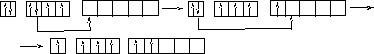
В этом случае В*=4; 6.

2
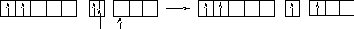 2Ti
1s22s22p63s23p63d24s2.
На первый взгляд, в атоме титана имеется
два неспаренных электрона на предвнешнем
d–
подуровне, которые могли бы вступить в
образование связи. Но, на самом деле,
они экранируются внешними спаренными
s– электронами,
поэтому в стационарном состоянии
валентность титана равна нулю. В
возбуждённом состоянии внешние
s– электроны
четвертого уровня распариваются (один
из них переходит на р– подуровень того
же уровня). Поскольку сразу два электрона
получили некоторый избыток энергии, то
они оба вступают в химическое
взаимодействие, то есть В*=2.
2Ti
1s22s22p63s23p63d24s2.
На первый взгляд, в атоме титана имеется
два неспаренных электрона на предвнешнем
d–
подуровне, которые могли бы вступить в
образование связи. Но, на самом деле,
они экранируются внешними спаренными
s– электронами,
поэтому в стационарном состоянии
валентность титана равна нулю. В
возбуждённом состоянии внешние
s– электроны
четвертого уровня распариваются (один
из них переходит на р– подуровень того
же уровня). Поскольку сразу два электрона
получили некоторый избыток энергии, то
они оба вступают в химическое
взаимодействие, то есть В*=2.
Что касается d– электронов на третьем энергетическом уровне, то они расположены ближе к ядру и поэтому обладают меньшим запасом энергии. Вследствие этого они менее активны и в образование связи могут вступать по одному. То есть В*=3; 4. Но, поскольку не все теоретически определённые валентности для элементов d– семейства обнаруживаются экспериментально, для них целесообразно указывать интервал валентностей. Например, В*=2-4.

43Tc 1s22s22p63s23p63d104s24p64d55s2
В стационарном (невозбуждённом) состояние В = 0.
В возбуждённом состоянии В* = 2-7.
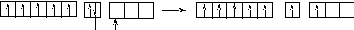
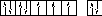
28Ni 1s22s22p63s23p63d84s2 В=0.
Следует учитывать, что хотя у никеля присутствуют и спаренные электроны на 3d– подуровне, и вакантные места на 4р– подуровне, мы не можем переместить эти электроны с 3d– подуровня на 4р– подуровень, поскольку это различные энергетические уровни.

В возбуждённом состоянии В*=2-5.
Первые два элемента (Na и Са) относятся к s– семейству, поскольку у них последним застраивается s- подуровень, вторые два элемента (O и Se) относятся к p– семейству, поскольку у них последним застраивается p– подуровень, последние три элемента (Ti, Tc и Ni) относятся к d– семейству, поскольку у них последним застраивается d– подуровень.
