
- •Министерство образования и науки рф Физика
- •Часть 2
- •Общие методические указания
- •Работа, выполненная не по своему варианту, не зачитывается.
- •Правила оформления контрольных работ:
- •Основная
- •Магнитное поле в веществе
- •Электромагнитная индукция
- •13. Работа по перемещению замкнутого контура с током в магнитном поле ,
- •Примеры решения задач
- •Контрольное задание 2.1
- •Часть 2.2 Волновая и квантовая оптика программа
- •Квантовая оптика
- •Экспериментальное обоснование основных идеи квантовой механики
- •Методические указания к выполнению контрольной работы
- •Часть 2.2 Волновая и квантовая оптика. Основные законы и формулы
- •Примеры решения задач
- •Контрольное задание 2.2
- •Методические указания к выполнению
- •Примеры решения задач
- •Контрольное задание 2.3
- •Приложения
- •Показатель преломления
- •7. Массы лёгких изотопов
- •8. Работа выхода электронов
- •9. Масса и энергия покоя некоторых частиц.
Методические указания к выполнению
КОНТРОЛЬНОЙ РАБОТЫ
Часть 2.3
Основные законы и формулы
Теория Бора
1.Момент импульса электрона ( второй постулат Бора)
Ln =m vn rn= n(h/2),
где m- масса электрона; vn- скорость электрона на n-й орбите;
rn – радиус n-ой стационарной орбиты; h- постоянная Планка;
n- главное квантовое число (n=1,2….).
2.Радиус n-й стационарной орбиты:
rn = ao n2,
где ao=0,529 . 10-10 м –первый Боровский радиус.
3.Энергия электрона в атоме водорода.
En = - Ei /n2,
где Еi- энергия ионизации атома водорода.
4.Энергия , излучаемая атомом водорода.:
![]() E
= (h/2)
= En2-En1
= Ei
(1/n
E
= (h/2)
= En2-En1
= Ei
(1/n![]() - 1/n
- 1/n![]() ),
),
где n2 и n1 – квантовые числа, соответствующие энергетическим уровням, между которыми совершается переход электрона в атоме.
5.Спектроскопическое
волновое число:![]() ,
,
где λ – длина волны излучения или поглощения атомом,
R – постоянная Ридберга.
Волновые свойства частиц.
6.Длина волны де Бройля:
![]()
где p – импульс частицы.
7.Импульс частицы и его связь с кинетической энергией Т:
а)
p=m![]() ;
;![]()
б)
p=m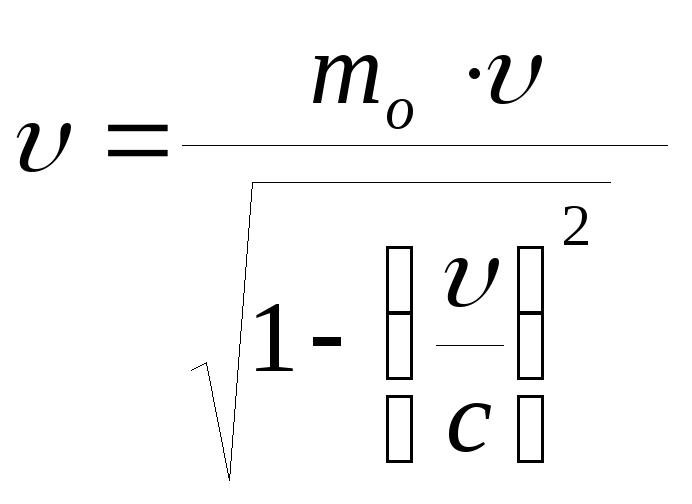 =
=![]() ,
,
где mo –масса покоя частицы; m- релятивистская масса;
![]() -
скорость частицы; с- скорость света в
вакууме;
-
скорость частицы; с- скорость света в
вакууме;
![]() - энергия покоя
частицы.
- энергия покоя
частицы.
8.Соотношение неопределённостей:
а) для координаты и импульса:
![]()
![]() ,
,
где
![]() - неопределённость проекции импульса
на осьx
;
- неопределённость проекции импульса
на осьx
;
![]() неопределённость
координаты.
неопределённость
координаты.
б) для энергии и времени:
![]() ,
,
где![]() -
неопределённость энергии;
-
неопределённость энергии;
![]() -время
жизни квантовой системы в данном
энергетическом состоянии.
-время
жизни квантовой системы в данном
энергетическом состоянии.
9.Одномерное уравнение Шредингера для стационарных состояний:
![]() ,
,
где
![]() -
волновая функция, описывающая состояние
частицы,
-
волновая функция, описывающая состояние
частицы,
m- масса частицы, Е – полная энергия, U – потенциальная энергия частицы.
10.Плотность вероятности:
![]() ,
,
где
![]() -
вероятность того, что частица может
быть обнаружена вблизи точки с координатой
х на участкеdx.
-
вероятность того, что частица может
быть обнаружена вблизи точки с координатой
х на участкеdx.
11.Вероятность обнаружения частицы в интервале от х1 до х2;
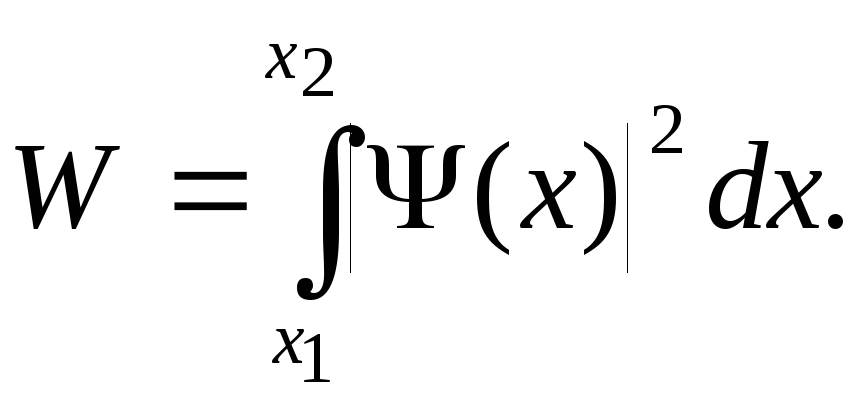
12.Решение уравнения Шредингера для микрочастицы в одномерном бесконечно глубоком прямоугольном потенциальном ящике:
а)
собственные нормированные волновые
функции:
![]()
б) собственные значения энергии:
![]() ,
,
где
n
=1,2,3,…- квантовое число,
![]() - ширина ящика,
- ширина ящика,![]() -
масса микрочастицы.
-
масса микрочастицы.
.
Пространственная решётка кристалла.
13.Молярный объём кристалла:
![]()
![]() ,
,
где
![]() -
молярная масса;
-
молярная масса;![]() -
плотность кристалла.
-
плотность кристалла.
14.Объём элементарной ячейки для решётки кубической сингонии:
![]() ,
,
где
![]() – параметр решётки.
– параметр решётки.
15.Число элементарных ячеек в одном моле кристалла:
![]() .
.
16.Если кристалл состоит из одинаковых атомов, то
![]() ,
,
где
![]() -
число одинаковых атомов, приходящихся
на элементарную ячейку;NA
- постоянная
Авогадро.
-
число одинаковых атомов, приходящихся
на элементарную ячейку;NA
- постоянная
Авогадро.
17.Число элементарных ячеек в единице объёма кристалла:
![]() .
.
18.Если кристалл состоит из одинаковых атомов, то
![]()
19.Параметр кубической решётки из одинаковых атомов:
![]()
20.Расстояние между соседними атомами в кубической решётке:
а)
d=![]() ( гранецентрированной);
( гранецентрированной);
б)
d=![]() (объёмноцентрированной).
(объёмноцентрированной).
Полупроводники.
21.Удельная проводимость собственных полупроводников:
![]()
где
![]() – элементарный заряд;
– элементарный заряд;
![]() -
концентрация носителей заряда ( электронов
и дырок);
-
концентрация носителей заряда ( электронов
и дырок);
![]() и
и
![]() -
подвижности электронов и дырок
,соответственно.
-
подвижности электронов и дырок
,соответственно.
22.Напряжение на гранях прямоугольного образца при эффекте Холла (холловская разность потенциалов):
UH=RHBja,
где RH- постоянная Холла, В – магнитная индукция,
j- плотность тока, а – ширина пластины (образца).
23.Постоянная Холла для полупроводников типа алмаз, германий, кремний и др., обладающих носителями заряда одного вида (n или р);
RH
=
![]() ,
,
где
![]() -
концентрация носителей заряда.
-
концентрация носителей заряда.
Атомное ядро. Радиоактивность.
24.Массовое число ядра (число нуклонов в ядре) :
A = Z + N ,
где Z – зарядовое число (число протонов);
N- число нейтронов.
25.Закон радиоактивного распада:
dN
= -
![]() Ndt
или N
= N0
Ndt
или N
= N0
![]() ,
,
где dN - число ядер, распадающихся за интервал времени dt;
N – число ядер, нераспавшихся к моменту времени t;
No – число ядер в начальный момент (t=0); λ- постоянная радиоактивного распада.
26.Число ядер, распавшихся за время t :
![]()
27.В случае , если интервал времени ∆t, за который определяется число распавшихся ядер, много меньше периода полураспада
![]() ,
то число распавшихся ядер можно определить
по формуле
,
то число распавшихся ядер можно определить
по формуле
![]()
28.Зависимость периода полураспада от постоянной радиоактивного распада:
![]()
29.Среднее
время
![]() жизни
радиоактивного ядра, т.е. интервал
времени, за который число нераспавшихся
ядер уменьшается в
жизни
радиоактивного ядра, т.е. интервал
времени, за который число нераспавшихся
ядер уменьшается в
e раз.
![]()
30.Число N атомов, содержащихся в радиоактивном изотопе:
![]() ,
,
где m- масса изотопа;
![]() -
молярная масса;
-
молярная масса;
NA – постоянная Авогадро.
31.Активность А радиоактивного изотопа:
![]() ,
,
где dN- число ядер, распадающихся за интервал времени dt;
Ао – активность изотопа в начальный момент времени.
32.Удельная активность изотопа:
![]() .
.
33.Дефект массы ядра:
![]() ,
,
где
Z
– зарядовое число (число протонов в
ядре ); А- массовое число (число нуклонов
в ядре );
![]() -масса
протона ;
-масса
протона ;![]() - масса нейтрона ;
- масса нейтрона ;![]() - масса ядра .
- масса ядра .
34.Энергия связи ядра :
![]() ,
,
где ∆m- дефект массы ядра ; с – скорость света в вакууме.
35.Во внесистемных единицах энергия связи ядра равна
![]() МэВ,
МэВ,
где дефект массы ∆m в а.е.м.; 931 – коэффициент пропорциональности (1 а.е.м. ~ 931 МэВ)
