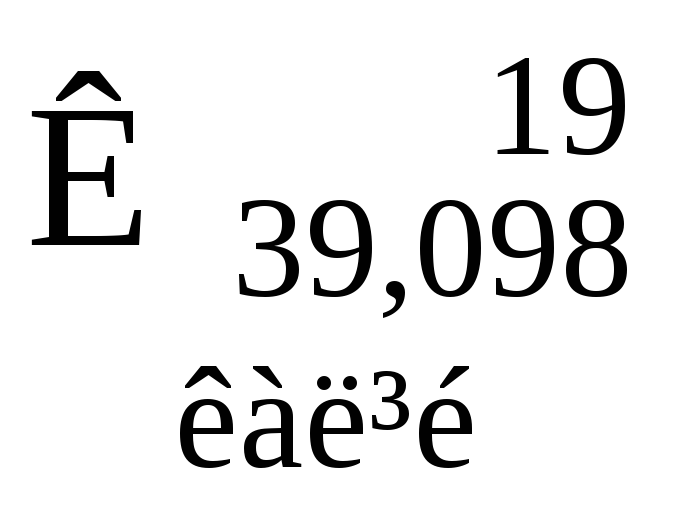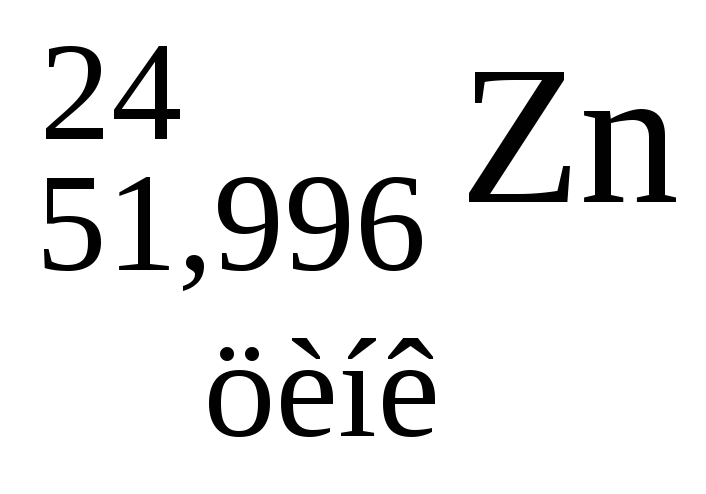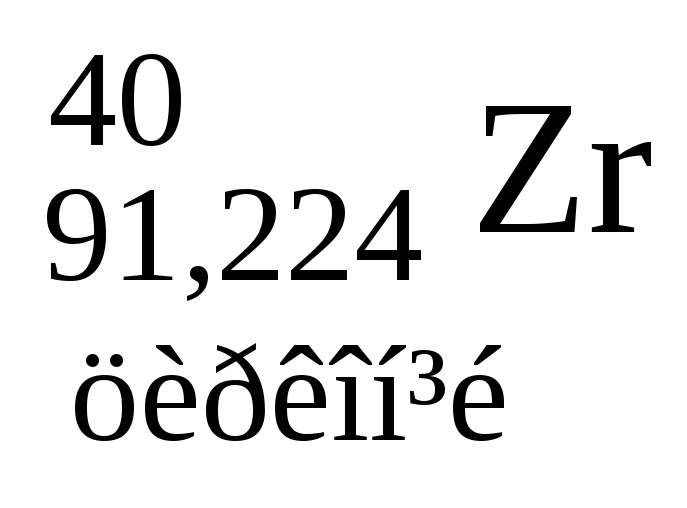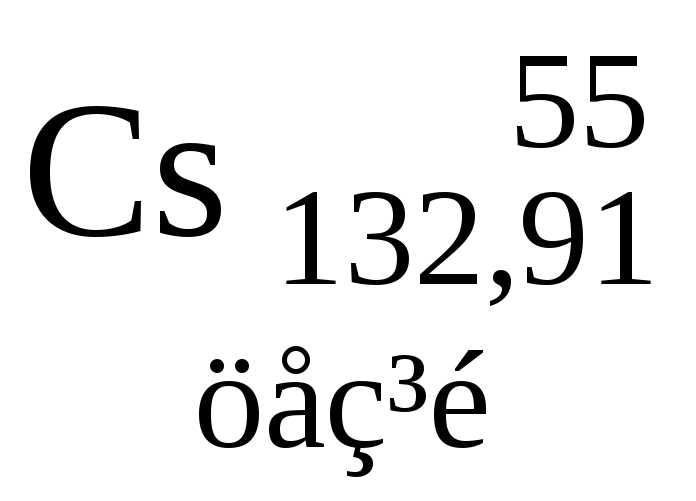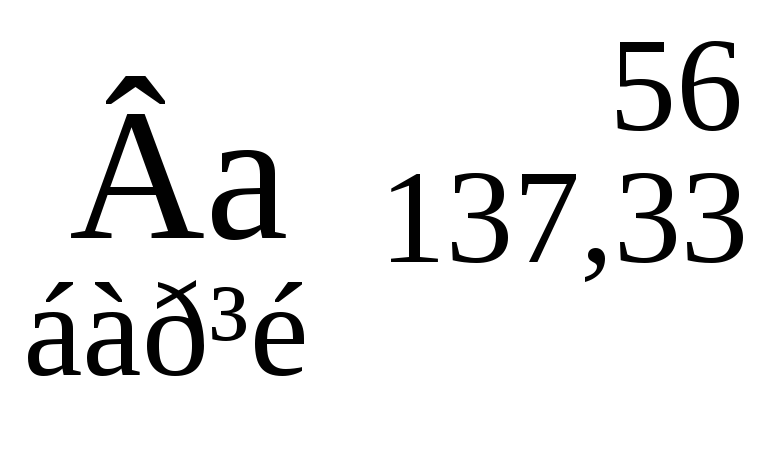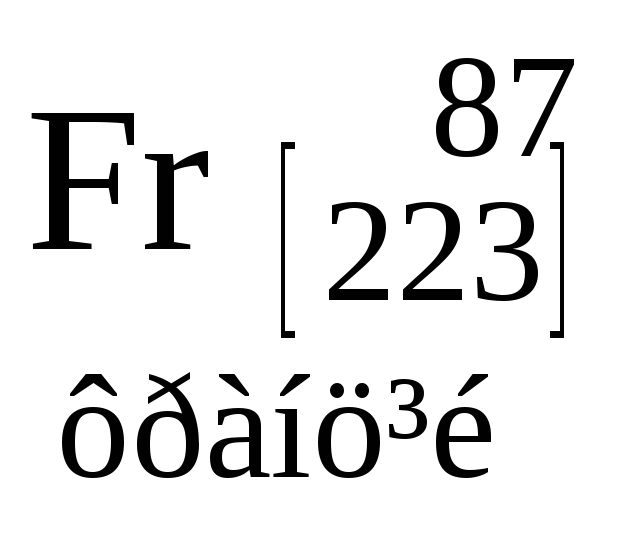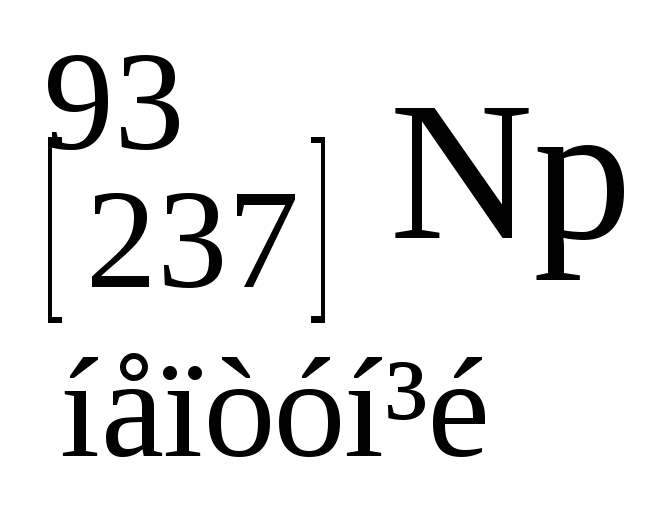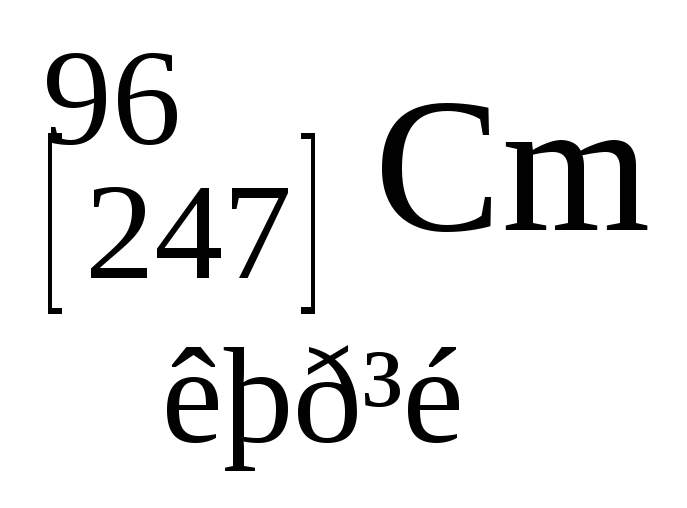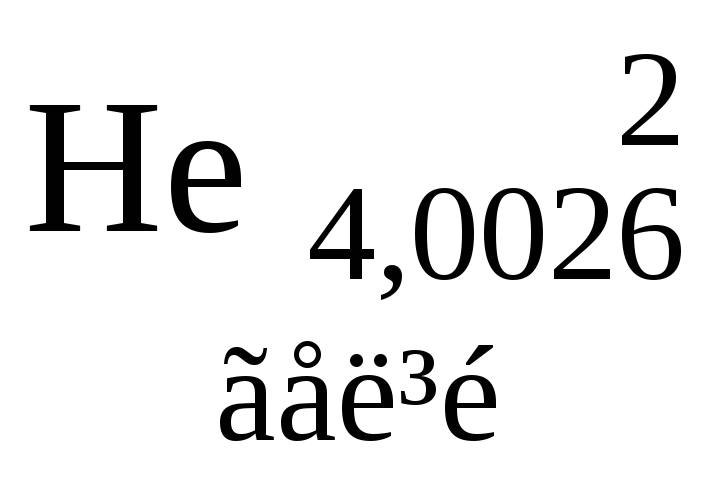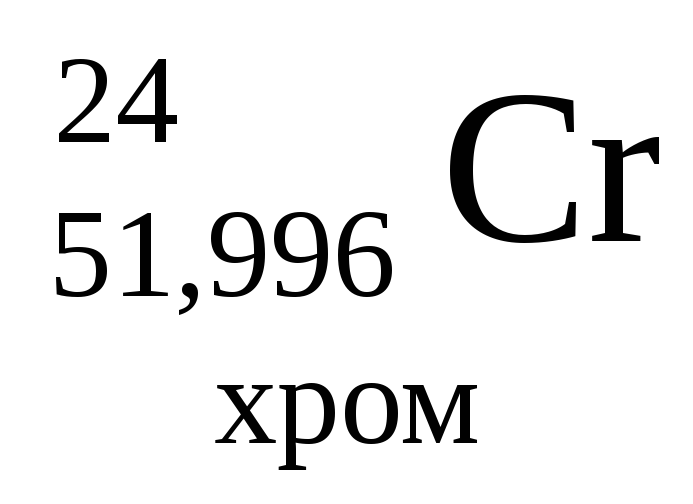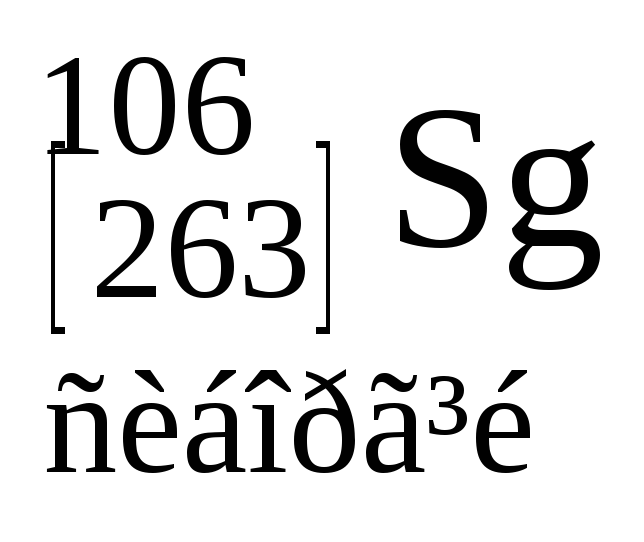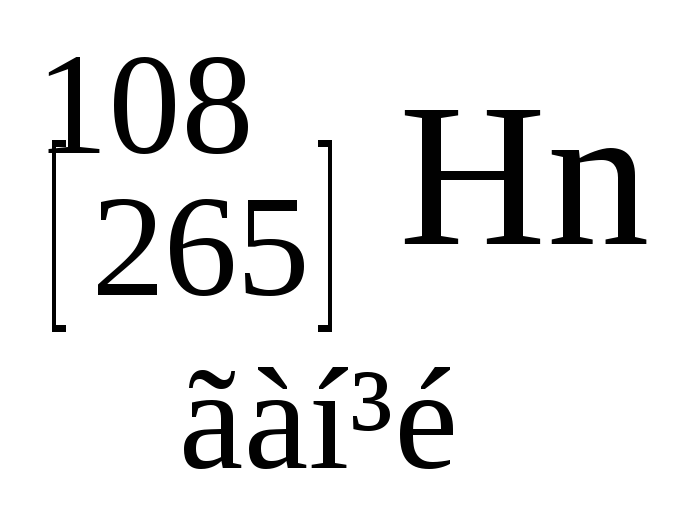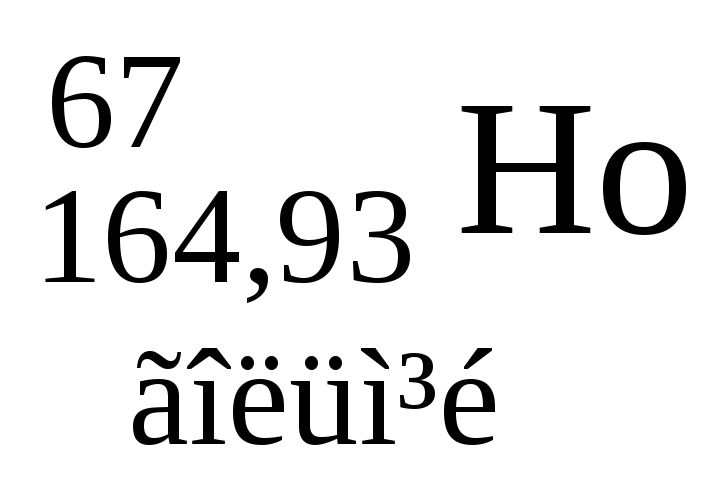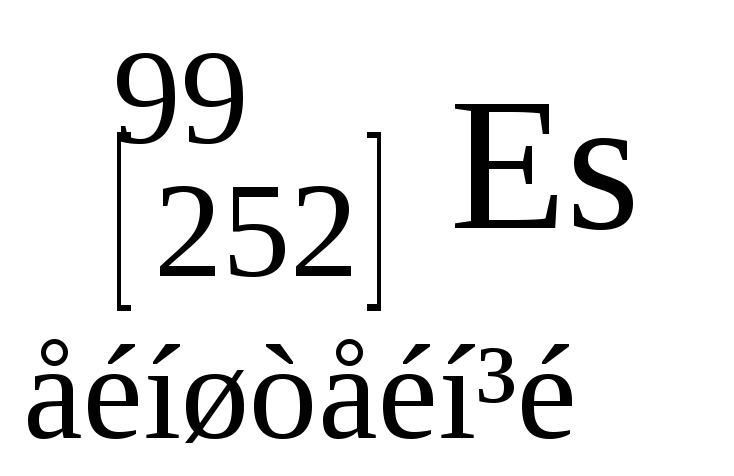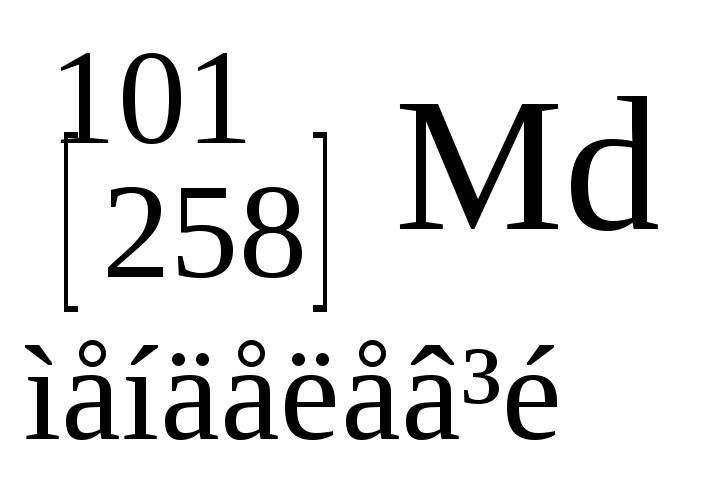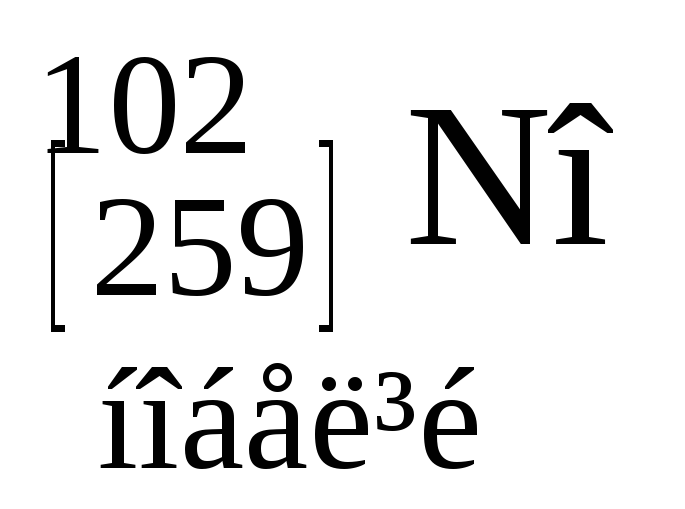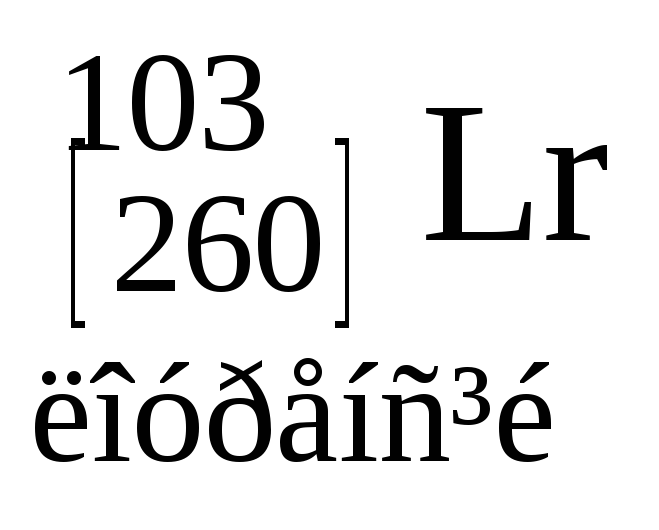Таблиця 3. ПЕРІОДИЧНА СИСТЕМА
|
ПЕРІОД |
I |
II |
III
|
IV |
V | |||||||||
|
I |
|
|
|
|
| |||||||||
|
II |
|
|
|
|
| |||||||||
|
III |
|
|
|
|
| |||||||||
|
IV |
|
|
|
|
| |||||||||
|
|
|
|
|
| ||||||||||
|
V |
|
|
|
|
| |||||||||
|
|
|
|
|
| ||||||||||
|
VI |
|
|
|
|
| |||||||||
|
|
|
|
|
| ||||||||||
|
VII |
|
|
|
|
| |||||||||
|
* Л А Н Т А Н О | ||||||||||||||
|
|
|
|
|
|
|
| ||||||||
|
**А К Т И Н О | ||||||||||||||
|
|
|
|
|
|
|
| ||||||||
Елементів д.І.Менделєєва
|
VI
|
VII |
VIII
| ||||||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
|
|
| |||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
|
|
| |||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
|
|
| |||||||||||||
|
|
|
|
| |||||||||||||||
|
|
|
|
|
|
| |||||||||||||
|
Ї Д И | ||||||||||||||||||
|
|
|
|
|
|
|
| ||||||||||||
|
Ї Д И | ||||||||||||||||||
|
|
|
|
|
|
|
| ||||||||||||
Таблица 4. Назви деяких кислот і їхніх солей
|
Формула кислоти |
Назва | |
|
кислоти |
кислотного залишку середньої солі | |
|
|
Фторидна (плавікова) |
Фтори |
|
|
Хлоридна (соляна) |
Хлорид |
|
|
Бромідна |
Бромід |
|
|
Іодидна |
Іодид |
|
|
Нітратна (азотна) |
Нітрат |
|
|
Нітритна |
Нітрит |
|
|
Ціанідна |
Ціанід |
|
|
Сульфатна (сірчана) |
Сульфат |
|
|
Сульфітна |
Сульфіт |
|
|
Сульфідна |
Сульфід |
|
|
Карбонатна (вугільна) |
Карбонат |
|
|
Силікатна |
Силікат |
|
|
Метафосфатна |
Метафосфат |
|
|
Ортофосфатна |
Ортофосфат |
|
|
Ортофосфітна |
Ортофосфіт |
|
|
Перманганатна |
Перманганат |
|
|
Гіпохлоритна |
Гіпохлорит |
|
|
Хлоритна |
Хлорит |
|
|
Хлоратна |
Хлорат |
|
|
Перхлоратна |
Перхлорат |
|
|
Хроматна |
Хромат |
|
|
Дихроматна |
Дихромат |
Таблиця 5. ТЕРМОДИНАМІЧНІ КОНСТАНТИ ДЕЯКИХ РЕЧОВИН
|
Речовина |
кДж/моль |
кДж/моль |
Дж/моль·К
|
|
1 |
2 |
3 |
4 |
|
Al(K) |
0 |
0 |
28,31 |
|
Al2O3(K) |
-1675,0 |
-1576,4 |
50,94 |
|
C(алмаз) |
1,897 |
2,866 |
2,38 |
|
С(графит) |
0 |
0 |
5,74 |
|
СО(Г) |
-110,5 |
-137,27 |
197,4 |
|
СО2(Г) |
-393,51 |
-394,38 |
213,6 |
|
СН4(Г) |
-74,85 |
-50,79 |
186,19 |
|
СН3ОН(Р) |
-238,7 |
-166,31 |
126,7 |
|
С2Н5ОН(Р) |
-227,6 |
-174,77 |
160,7 |
|
СаО(К) |
-635,1 |
-604,2 |
39,7 |
|
Са(ОН)2(К) |
-986,50 |
-896,76 |
83,4 |
|
CaSiO3(K) |
-1579,0 |
-1495,4 |
87,45 |
|
Са3(РО4)2(К) |
-4125,0 |
-3899,5 |
240,9 |
|
СаСО3(К) |
-1206,0 |
-1128,8 |
92,9 |
|
Сl2(Г) |
0 |
0 |
222,9 |
|
O3(K) |
-1141,0 |
-1046,84 |
81,1 |
|
Fe(К) |
0 |
0 |
27,2 |
|
FeO(K) |
-263,68 |
-244,35 |
58,79 |
|
Fe2O3 |
-821,32 |
-740,99 |
89,96 |
|
Fe3O4 |
-1117,9 |
-1014,8 |
146,3 |
|
H2(Г) |
0 |
0 |
130,6 |
|
НСl(Г) |
-92,4 |
-94,5 |
186,9 |
|
Н2О(Г) |
-241,84 |
-228,8 |
188,74 |
|
Н2О(Р) |
-285,84 |
-237,5 |
69,96 |
|
Н2О2(Р) |
-187,0 |
-117,57 |
105,86 |
|
Mg(K) |
0 |
0 |
32,55 |
|
MgCO(3) |
-1096,2 |
-1029,3 |
65,69 |
|
KCl(K) |
-435,9 |
-408,6 |
82,60 |
|
KClO3(K) |
-391,2 |
-289,9 |
143,0 |
|
MgO(К) |
-601,8 |
-569,6 |
26,94 |
|
N2(Г) |
0 |
0 |
191,49 |
|
N2O(Г) |
81,55 |
103,6 |
220,0 |
|
1 |
2 |
3 |
4 |
|
NO(Г) |
90,37 |
86,69 |
210,62 |
|
N2O4(Г) |
9,37 |
98,29 |
304,3 |
|
NO2(Г) |
33,89 |
51,84 |
240,45 |
|
NH3(Г) |
-46,19 |
-16,64 |
192,5 |
|
Na2O(K) |
-430,6 |
-376,6 |
71,1 |
|
Na2SiO3(K) |
-1518,0 |
-1426,7 |
113,8 |
|
NaCl(K) |
-410,9 |
-384,0 |
72,36 |
|
NaF(K) |
-577,0 |
-541,0 |
51,0 |
продовження табл.5
|
1 |
2 |
3 |
4 |
|
О2(Г) |
0 |
0 |
205,03 |
|
О3(Г) |
142,3 |
163,4 |
238,8 |
|
P2O5(K) |
-1492,0 |
-1348,8 |
114,5 |
|
PCl3(Г) |
-287,0 |
-260,5 |
311,7 |
|
PCl5(Г) |
-374,9 |
-305,4 |
352,7 |
|
PbO(K) |
-217,9 |
-188,5 |
67,4 |
|
PbO2(K) |
-276,6 |
-218,99 |
76,44 |
|
PbS(K) |
-94,28 |
-92,68 |
91,20 |
|
S(ромб) |
0 |
0 |
31,88 |
|
SO2(Г) |
-296,9 |
-300,37 |
248,1 |
|
H2S(Г) |
-20,15 |
-33,02 |
205,64 |
|
Тi |
0 |
0 |
30,7 |
|
TiO2 |
-943,9 |
-888,6 |
50,3 |
|
SiO2(K) |
-859,3 |
-803,75 |
42,09 |
Таблиця 6. КРІОСКОПІЧНІ ТА ЕБУЛІОСКОПІЧНІ КОНСТАНТИ РОЗЧИННИКІВ
|
Розчинник |
ККР |
КЕ |
TПЛ |
TКИП |
|
Анілін |
5,87 |
3,22 |
-5,96 |
184,4 |
|
Ацетон |
2,4 |
1,48 |
-94,6 |
56,0 |
|
Бензол |
5,1 |
2,57 |
5,4 |
80,2 |
|
Вода |
1,85 |
0,516 |
0 |
100 |
|
Камфора |
40,0 |
6,90 |
174,0 |
204 |
|
Нітробензол |
6,90 |
5,27 |
5,7 |
210,9 |
|
Фенол |
7,3 |
3,6 |
41,0 |
182,1 |
|
Хлороформ |
4,9 |
3,88 |
-63,2 |
61,2 |
|
Чотирихлористий вуглець |
2,98 |
5,3 |
-23 |
76,7 |
Таблиця 7. КОНСТАНТИ ДИСОЦІАЦІІ ДЕЯКИХ СЛАБКИХ ЕЛЕКТРОЛІТІВ
(250С)
|
Речовина |
Кд |
Речовина |
Кд |
|
НСООН |
К=1,77·10-4 |
Н2О |
К=1,8·10-16 |
|
СН3СООН |
К=1,75·10-5 |
NH4OH |
К=1,79·10-5 |
|
НСN |
К=7,9·10-10 |
Al(OH)3 |
К3=1,38·10-9 |
|
Н2СО3 |
К1=4,45·10-7 |
Zn(OH)2 |
К1=4,4·10-5 |
|
|
К2=4,8·10-11 |
|
К2=1,5·10-9 |
|
HF |
К=6,61·10-4 |
Cd(OH)2** |
К2=5·10-3 |
|
HNO2* |
К=4·10-4 |
Fe(OH)2 |
К2=1,3·10-4 |
|
H2SO3 |
К1=1,7·10-2 |
Fe(OH)3 |
К2=1,82·10-11 |
|
|
К2=6,3·10-8 |
|
К3=1,35·10-12 |
|
H2S |
К1=1,1·10-7 |
Cu(OH)2 |
К2=3,4·10-7 |
|
|
К2=1·10-14 |
Ni(OH)2 |
К2=2,5·10-5 |
|
H2SiO3 |
К1=1,3·10-10 |
Cr(OH)3 |
К3=1·10-10 |
|
|
К2=2·10-12 |
AgOH |
К=1,1·10-4 |
|
H3PO4 |
К1=7,5·10-3 |
Pb(OH)2 |
К1=9,6·10-4 |
|
|
К2=6,31·10-8 |
|
К2=3·10-8 |
|
|
К3=1,3·10-12 |
|
|
|
HAlO2 |
К=6·10-13 |
|
|
|
H3BO4 |
К1=5,8·10-10 |
|
|
|
|
К2=1,8·10-13 |
|
|
|
|
К3=1,6·10-14 |
|
|
|
HClO |
К=5·10-8 |
|
|
|
*Кд визначені при 180С | |||
|
**Кд визначені при 300С | |||
Таблиця 8. ВІДНОСНА ЕЛЕКТРОНЕГАТИВНІСТЬ ДЕЯКИХ ЕЛЕМЕНТІВ
(ТАБЛИЦЯ ПОЛІНГА)
|
I |
II |
III |
IV |
V |
VI |
VII |
|
Н 2,1 |
|
|
|
|
|
|
|
Li 1,0 |
Be 1,5 |
B 2,0 |
C 2,5 |
N 3,0 |
O 3,5 |
F 4,0 |
|
Na 0,9 |
Mg 1,2 |
Al 1,5 |
Si 1,8 |
P 2,1 |
S 2,5 |
Cl 3,0 |
|
K 0,8 |
Ca 1,0 |
Sc 1,3 |
Ti 1,6 |
|
|
|
|
|
Zn 1,6 |
Ca 1,6 |
Ge 1,7 |
As 2,0 |
Se 2,4 |
Br 2,8 |
|
Rb 0,8 |
Sr 1,0 |
V 1,3 |
Zr 1,6 |
|
|
|
|
|
|
In 1,5 |
Sn 1,7 |
Sb 1,8 |
Fe 2,1 |
I 2,6 |
|
Cs 0,7 |
Ba 0,9 |
|
|
|
|
|