
- •0Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Термохімія та термохімічні розрахунки основні поняття та визначення
|
Термохімія
|
- розділ хімії, який вивчає теплові ефекти хімічних реакцій і фазових перетворень. |
|
Термохімічні рівняння
|
- рівняння процесів, в яких указані теплові ефекти та агрегатні стани речовин. |
|
Ентальпія (Н) |
-
тепловміст системи, що включає внутрішню
енергію і роботу розширення.
|
|
Тепловий ефект хімічної реакції (ентальпія реакції, ΔН) |
- кількість теплоти, що виділяється або поглинається під час перебігу хімічної реакції, якщо система не здійснює ніякої роботи, окрім роботи розширення. В ізобаричних процесах тепловий ефект дорівнює зміні ентальпії системи ΔН. Він називається також ентальпією реакції. Розмірність кДж.
|
|
Стандартна ентальпія реакції ΔН0 |
- тепловий ефект реакції за стандартних умов (Р = 101,3 кПа, Т=298К).
|
|
Екзотермічна реакція |
- реакція, що відбувається з виділенням теплоти Q > 0, тобто з пониженням ентальпії системи ΔН < 0.
|
|
Ендотермічна реакція |
- реакція, що відбувається з поглинанням теплоти Q < 0, тобто з підвищенням ентальпії системи ΔН > 0.
|
|
Ентальпія (теплота) утворення (ΔНутв) |
- тепловий ефект утворення 1 моль речовини з простих речовин, стійких за стандартних умов (Т = 298К, Р = 101,3 кПа). Розмірність кДж/моль.
|
|
Закон Гесса |
- тепловий ефект реакції залежить від природи і стану вихідних речовин і продуктів реакції і не залежить від шляху перебігу реакції, тобто від числа і характеру проміжних стадій. |
|
Перший наслідок із закону Гесса
|
- тепловий ефект (ентальпія) хімічної реакції дорівнює різниці між сумою теплот утворення продуктів реакції та сумою теплот утворення вихідних речовин з урахуванням стехіометричних коефіцієнтів
|
|
Другий наслідок із закону Гесса |
- тепловий ефект (ентальпія) реакції дорівнює різниці між сумою теплот згоряння вихідних речовин і сумою теплот згоряння продуктів реакції з урахуванням стехіометричних коефіцієнтів.
|
|
Теплота (ентальпія) згоряння ΔНзг |
- тепловий ефект реакції окиснення 1 моль речовини киснем з утворенням вищих оксидів. Розмірність кДж/моль.
|
|
Теплотворна здатність Q |
- теплота, що виділяється при згорянні 1 кг твердого або рідкого палива та 1 м3 газоподібного палива. Розмірність кДж/кг, кДж/м3. |
Приклади виконання завдань
При виконанні завдань цього розділу див. табл. 4.
Приклад 1. Визначити кількість теплоти, що виділяється при згорянні 112 л (н.у.) сірководню, якщо продуктами реакції є пари води і оксид сірки (1V). Термохімічне рівняння реакції горіння сірководню має вигляд:
![]() .
.
Розв’язання.
Як видно з термохімічного
рівняння, при згорянні 2 моль, тобто
2·22,4 л (взятих за н.у.), сірководню
виділяється 1037,18 кДж
теплоти. Тому кількість теплоти, що
виділяється при згорянні 112 л
![]() ,може бути розрахована з
пропорції:
,може бути розрахована з
пропорції:
4 4,8
л 1037,8 кДж
4,8
л 1037,8 кДж
 112 л х кДж
112 л х кДж
![]() .
.
Приклад 2. Визначити об’єм (н.у.) і масу сірководню, необхідного для реакції
![]() ,
,
якщо при цьому виділяється 2592,95 кДж. теплоти.
Розв’язання. Як видно з термохімічного рівняння, при згорянні 2 моль, тобто 2х22,4 л (взятих за н.у.), сірководню виділяється 1037,18 кДж теплоти. Тому об’єм H2S, необхідний для виділення 2592,95 кДж теплоти, може бути розрахований з пропорції:
2 ·22,4
л 1037,8 кДж
·22,4
л 1037,8 кДж
 х л 2592,95 кДж
х л 2592,95 кДж
![]() (л).
(л).
Для
знаходження маси H2S
необхідно знати молярну масу
![]() =
1· 2+32=34 г/моль.
=
1· 2+32=34 г/моль.
Маса 1 моль займає об’єм 22,4 л за нормальних умов. Тоді масу H2S можна розрахувати з пропорції:
 34 г 22,4 л
34 г 22,4 л
 х г 112 л
х г 112 л
![]() (г).
(г).
Приклад 3. Визначити кількість теплоти, що виділяється при гашенні 100 кг вапна водою, якщо термохімічне рівняння має вигляд:
![]()
Розв’язання.
Як видно з термохімічного
рівняння, при гашенні 1 моль вапна
виділяється 65,26 кДж
теплоти, а при гашенні
1 кмоль вапна – 65260 кДж.
![]() =
56 г/моль = 56 кг/кмоль. Тому кількість
теплоти, що виділяється при гашенні 100
кг СаО може
бути розрахована з пропорції:
=
56 г/моль = 56 кг/кмоль. Тому кількість
теплоти, що виділяється при гашенні 100
кг СаО може
бути розрахована з пропорції:
 56 кг 65260 кДж
56 кг 65260 кДж
 100 кг х кДж
100 кг х кДж
![]() (кДж).
(кДж).
Приклад 4. Визначити масу вапна, необхідну для реакції
![]() ,
,
якщо при цьому виділяється 116536 кДж теплоти.
Розв’язання.
Як видно з термохімічного
рівняння, при гашенні 1 моль вапна
виділяється 65,26 кДж теплоти.
![]() = 56 г/моль. Тому
маса СаО,
необхідна для виділення 116536 кДж
теплоти, може бути
розрахована з пропорції:
= 56 г/моль. Тому
маса СаО,
необхідна для виділення 116536 кДж
теплоти, може бути
розрахована з пропорції:
5 6
г 65,26 кДж
6
г 65,26 кДж
 х г 116536 кДж
х г 116536 кДж
![]() (г)
= 100 (кг).
(г)
= 100 (кг).
Приклад
5. При розчиненні 1
моль безводного сульфату міді в досить
великій кількості води виділяється
66,1 кДж теплоти , а при розчиненні 1 моль
кристалогідрату
![]() поглинається 11,7 кДж теплоти. Розрахувати
теплоту гідратації сульфату міді.
поглинається 11,7 кДж теплоти. Розрахувати
теплоту гідратації сульфату міді.
Розв’язання. Під теплотою гідратації солі розуміють тепловий ефект реакції утворення 1 моль кристалогідрату з безводної солі
![]() . (1)
. (1)
Виходячи з умов задачі, можна записати термохімічні рівняння:
![]() ;(2)
;(2)
![]() . (3)
. (3)
Задача розв’язується на основі закону Гесса: тепловий ефект реакції не залежить від шляху її перебігу, а залежить лише від природи і фізичного стану вихідних речовин та продуктів реакції. З термохімічними рівняннями можна оперувати так само, як і з алгебраїчними. Отже, щоб отримати рівняння (1) необхідно від рівняння (3) відняти рівняння (2) і тоді
![]()
Приклад 6. Визначити тепловий ефект реакції:
![]()
за відомими величинами стандартних теплот утворення речовин.
Розв’язання. Для цього використовуємо перший наслідок із закону Гесса:
![]() .
.
Значення
![]() речовин беремо в таблиці 4:
речовин беремо в таблиці 4:

![]()
![]() .
.
Враховуючи, що теплоти утворення простих речовин умовно прийняті рівними нулю, отримуємо:
![]() ,
,
![]() .
.
Відповідь: 247,36 кДж.
П![]() риклад
7.Знайти теплоту
утворення
риклад
7.Знайти теплоту
утворення
![]() ,
використовуючи теплоти утворення
,
використовуючи теплоти утворення![]() і тепловий ефект реакції
і тепловий ефект реакції
Розв’язання.
Для знаходження теплоти
утворення
![]() використовуємо першийнаслідок
із закону Гесса:
використовуємо першийнаслідок
із закону Гесса:
![]() .
.
Значення
![]() речовин беремо в таблиці 4:
речовин беремо в таблиці 4:
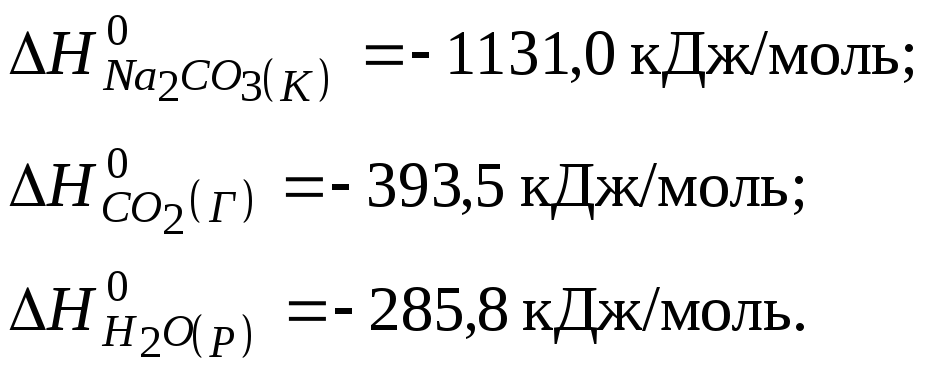
Тоді
![]()
![]() (кДж/моль).
(кДж/моль).
Відповідь: -426,6 кДж/моль.
Приклад
8. Визначити теплотворну
здатність бензолу
![]() ,
якщо теплота згоряння його становить
,
якщо теплота згоряння його становить![]() .
.
Розв’язання. Під теплотворною здатністю розуміють теплоту, що виділяється при згорянні 1 кг твердого та рідкого палива або 1 м3 газоподібного. Виходячи з умов задачі, при згорянні 1 моль або 78 г бензолу виділяється 3267,70 кДж теплоти. Звідси можна скласти пропорцію:
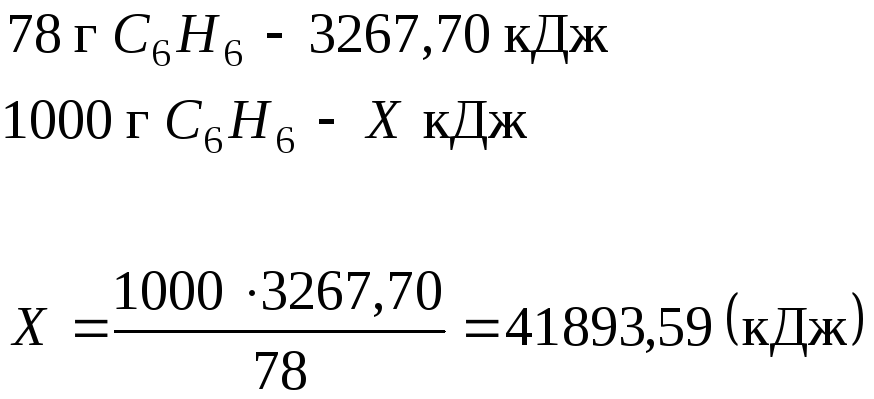
Відповідь: 41893,59 кДж/кг
