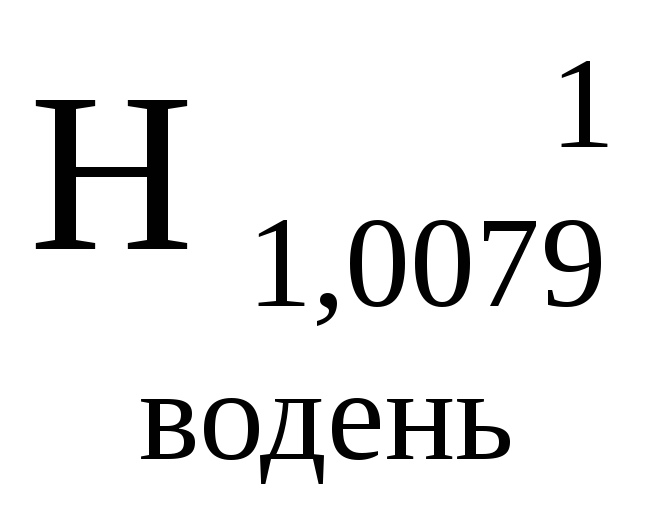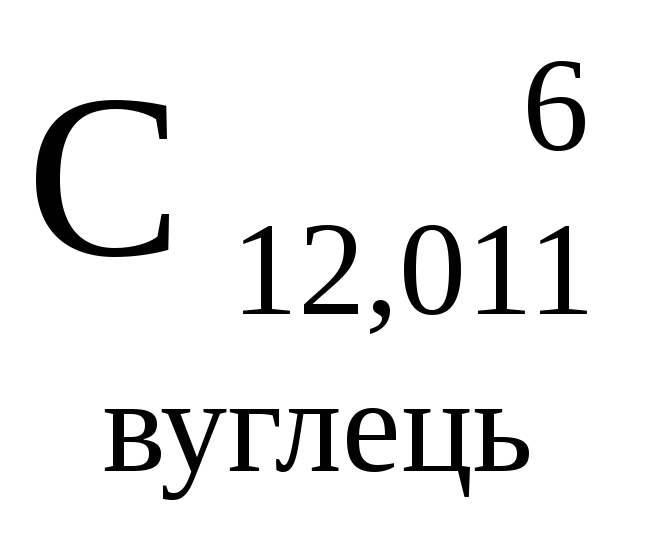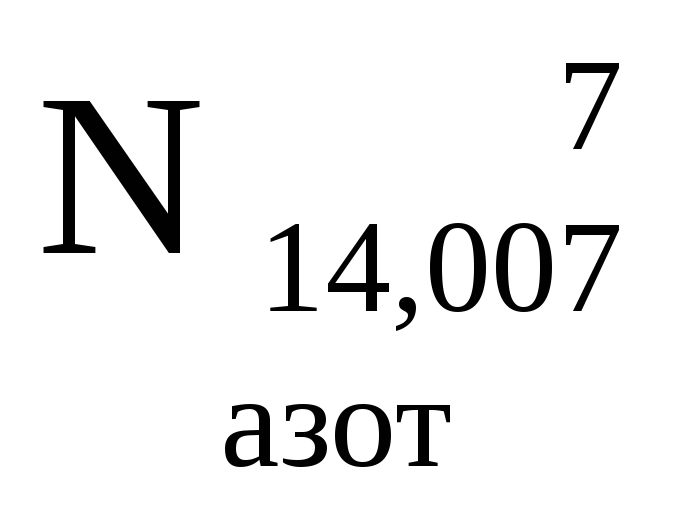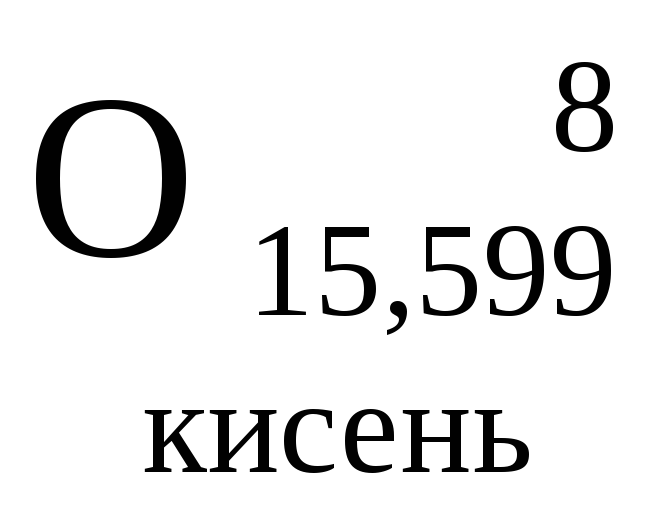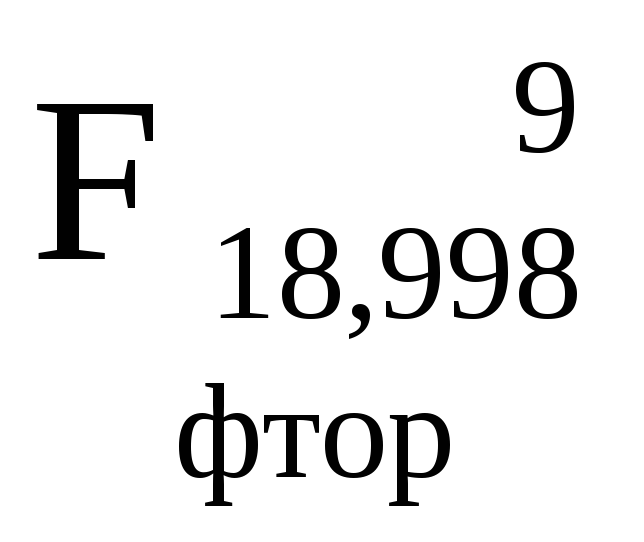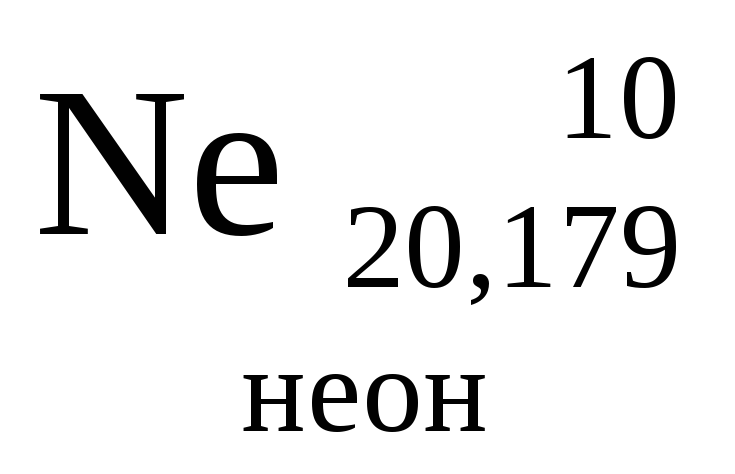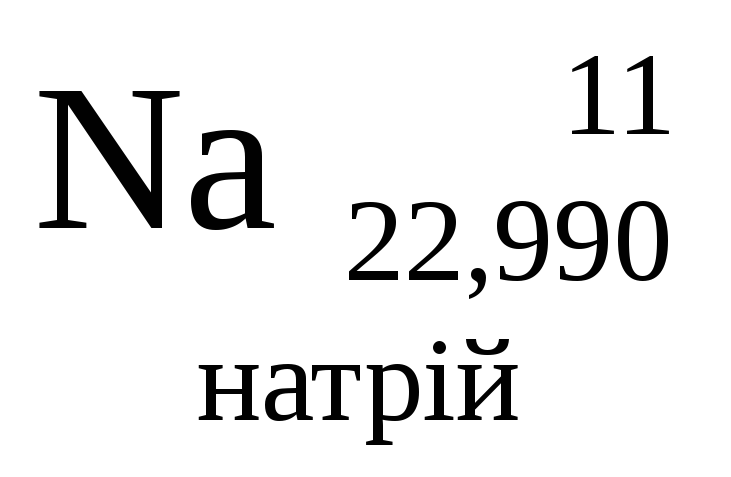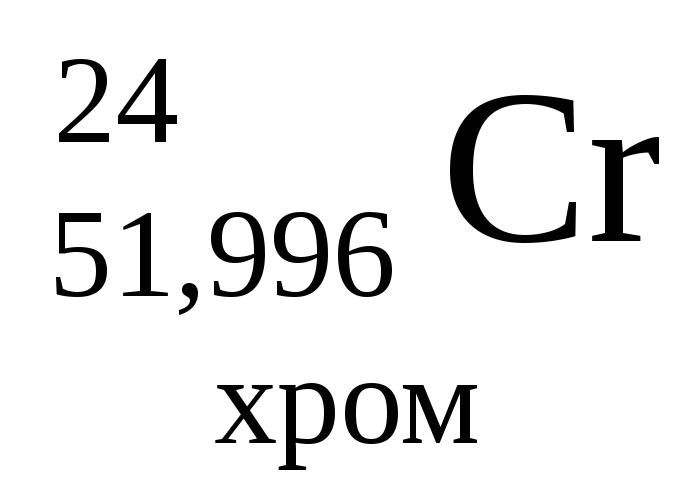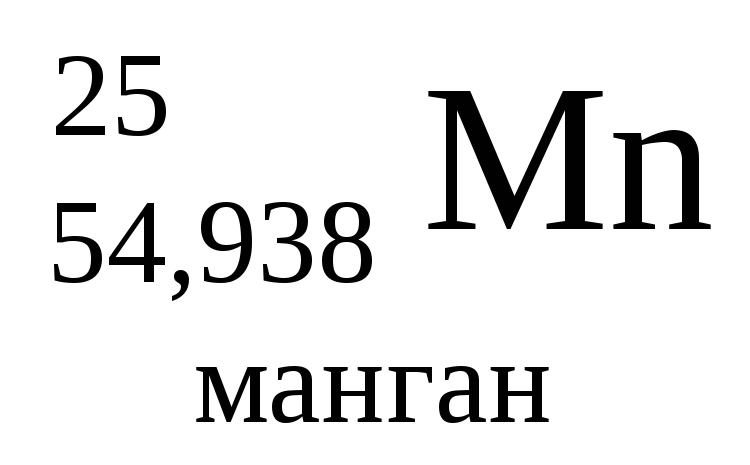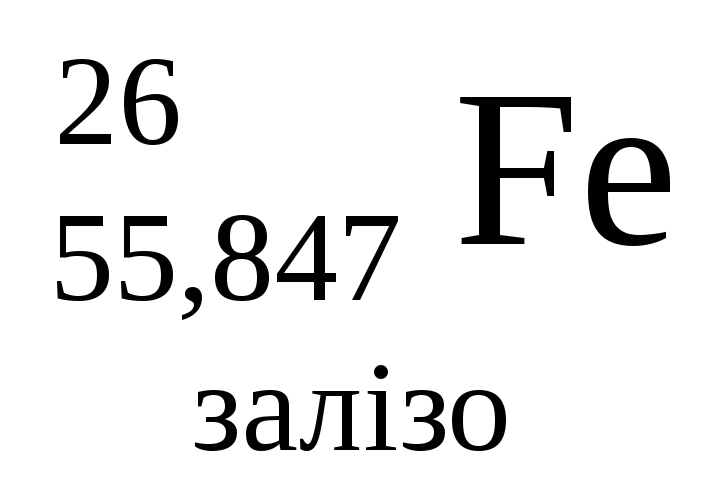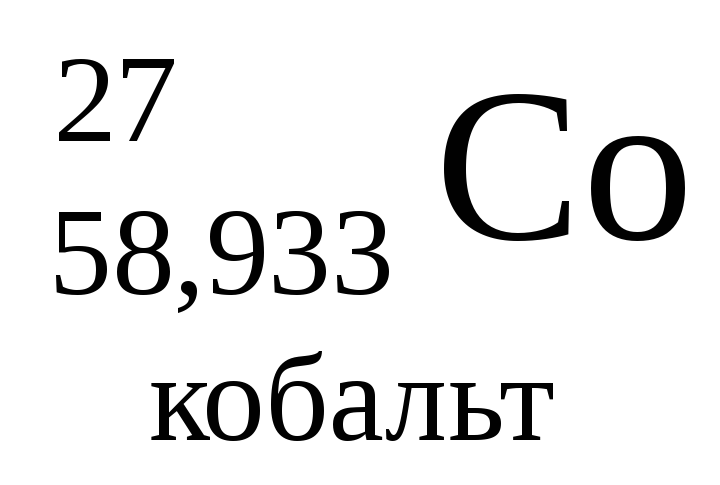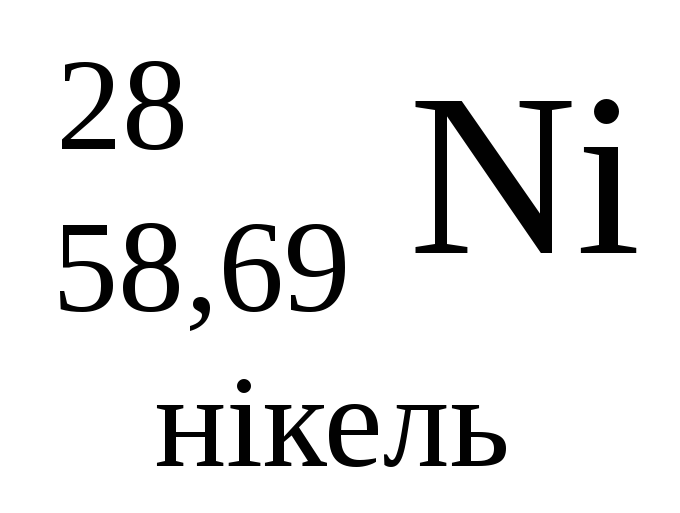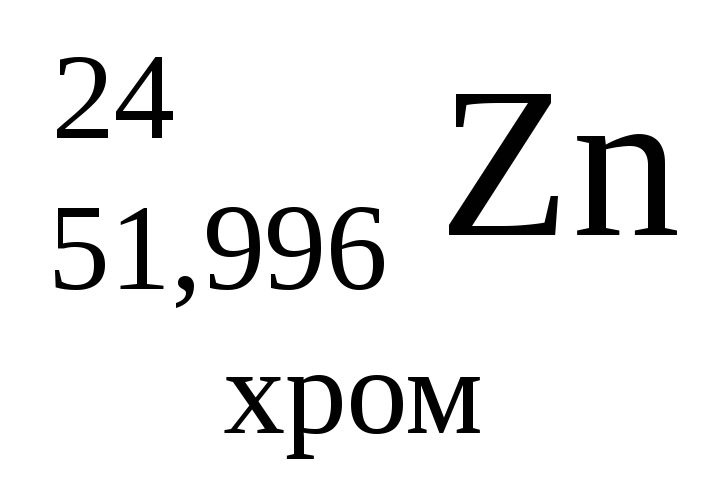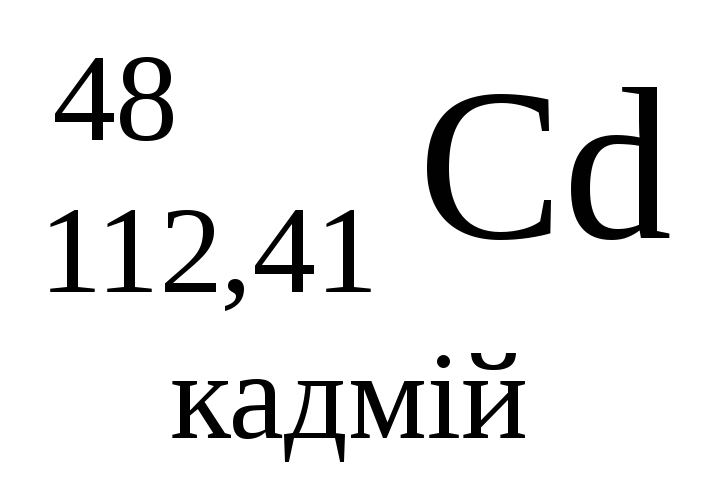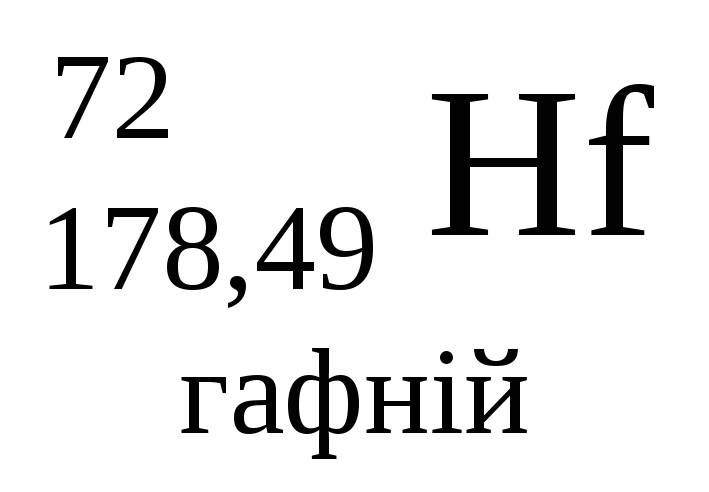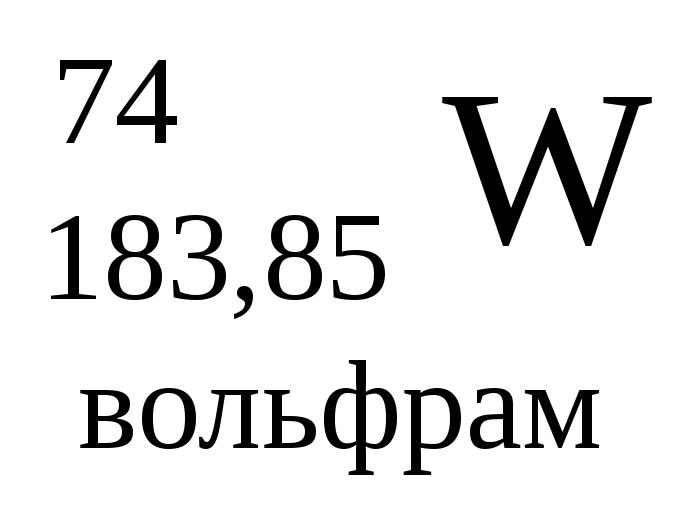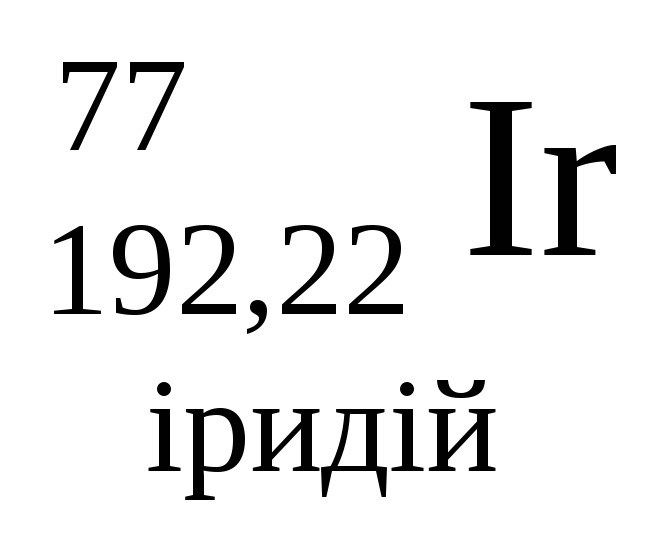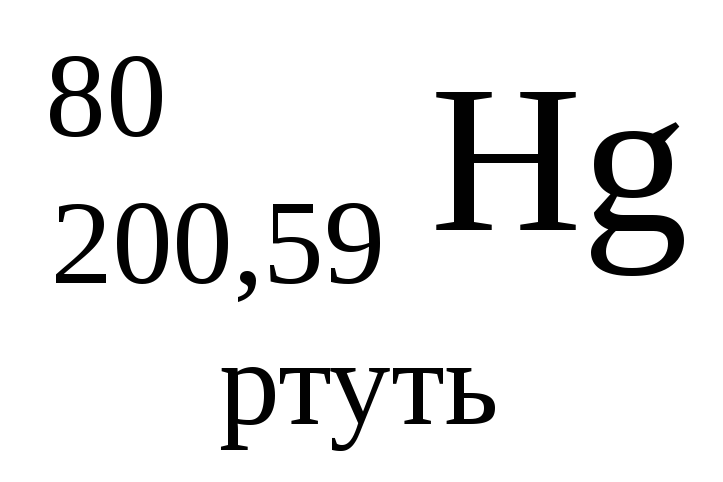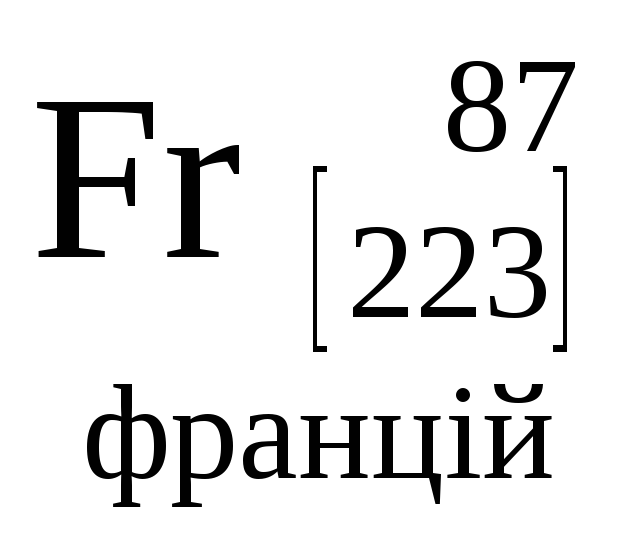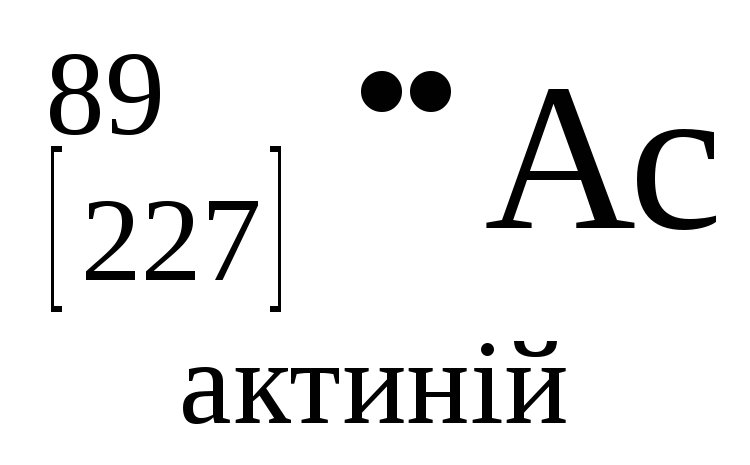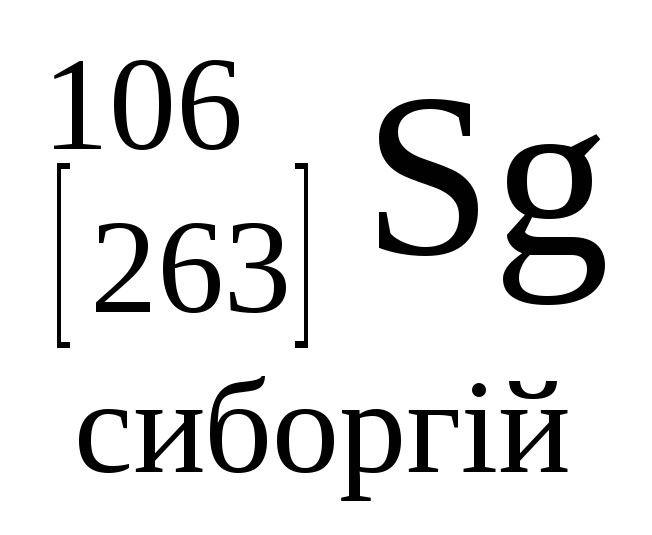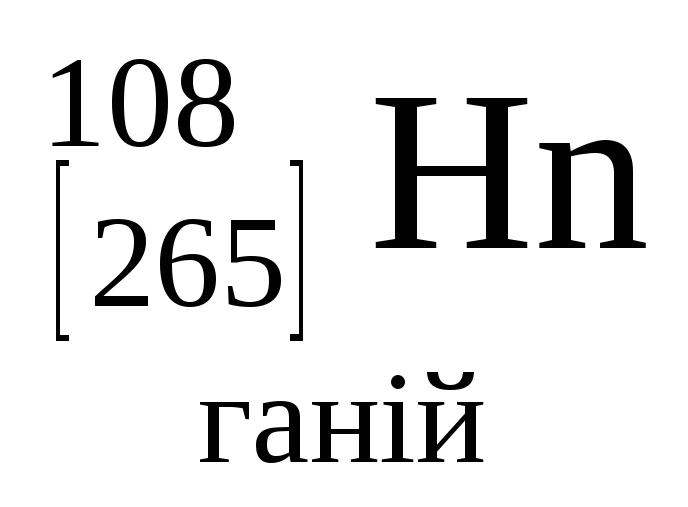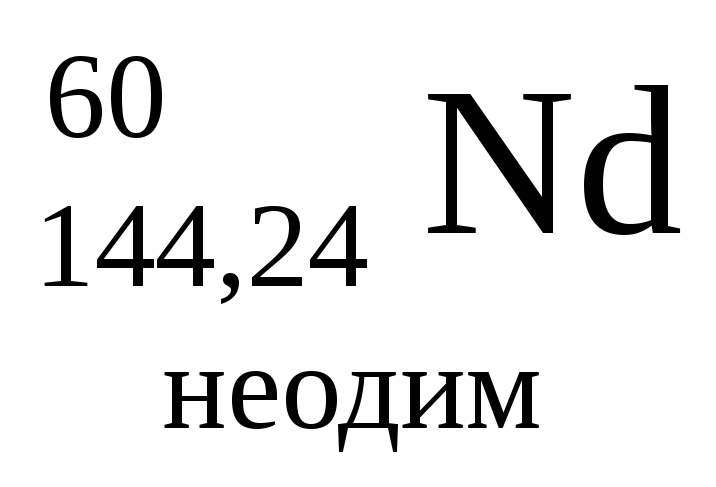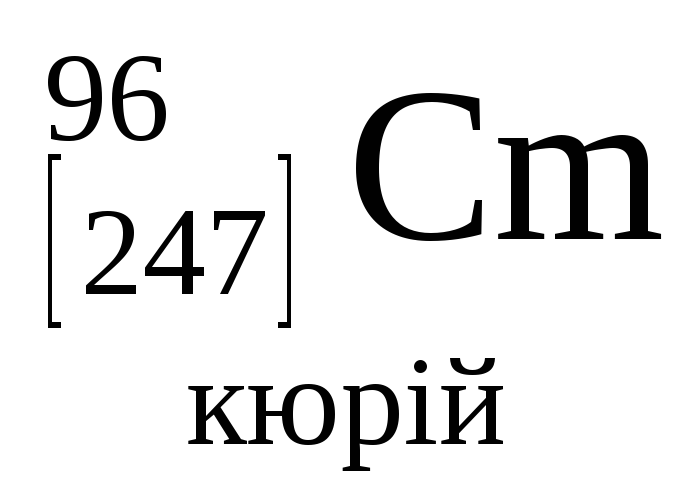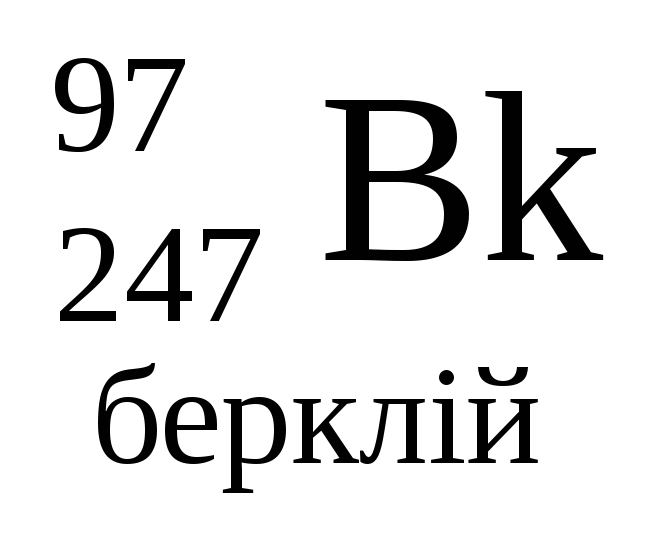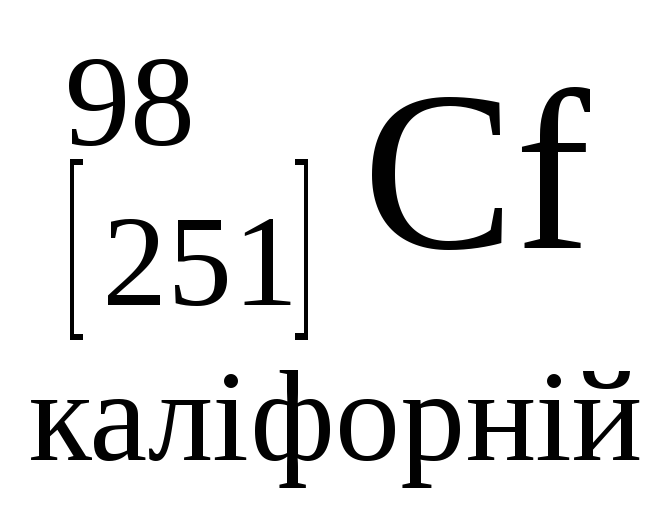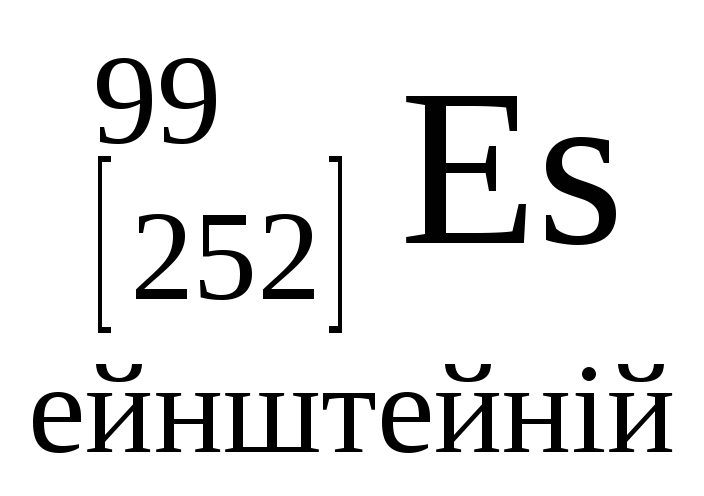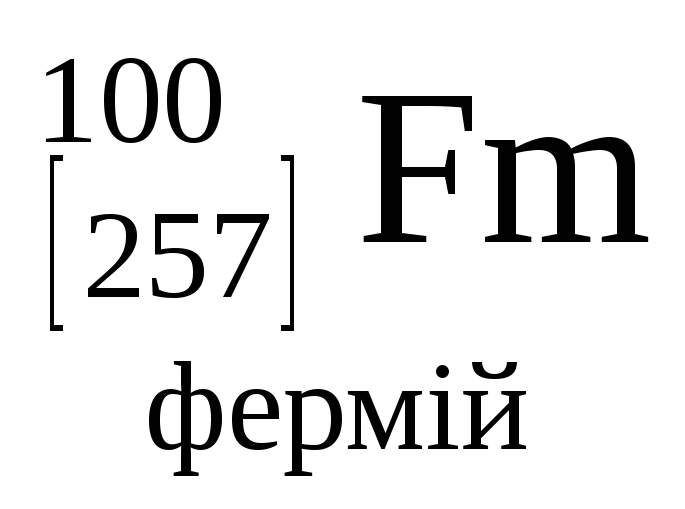- •0Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Періодична система хімічних елементів д.І.Менделєєва
|
ПЕРІОД |
I |
II |
III
|
IV |
V |
VI
|
VII |
VIII
| ||||||||||||||||||||||
|
I |
|
|
|
|
|
|
|
|
| |||||||||||||||||||||
|
II |
|
|
|
|
|
|
|
|
| |||||||||||||||||||||
|
III |
|
|
|
|
|
|
|
|
| |||||||||||||||||||||
|
IV |
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||
|
V |
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||
|
VI |
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
|
|
|
|
|
|
|
|
| ||||||||||||||||||||||
|
VII |
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||||
|
* Л А Н Т А Н О Ї Д Ы | ||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||
|
** А К Т И Н О Ї Д Ы | ||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| |||||||||||||||||
Таблиця 2
Деякі одиниці міжнародної системи (сі)
|
Величина |
Одиниця | |
|
Назва |
Позначення | |
|
Довжина |
Метр |
м |
|
Маса |
Кілограм |
кг |
|
Час |
Секунда |
с |
|
Сила електричного струму |
Ампер |
А |
|
Температура |
Кельвін |
К |
|
Кількість речовини |
Моль |
моль |
|
Об’єм |
Кубічний метр |
м3 |
|
Тиск |
Паскаль |
Па |
|
Енергія, робота Кількість теплоти |
Джоуль |
Дж |
|
Кількість електрики |
Кулон |
Кл |
|
Електрична напруга Електрорушійна сила |
Вольт |
В |
Таблиця 3
Значення деяких фундаментальних фізичних сталих
|
Стала |
позначення |
Чисельне значення |
|
Число Авогадро |
NA |
6,022045·1023 моль-1 |
|
Число Фарадея |
F |
96485 Кл/моль |
|
Газова стала |
R |
8,3144 Дж/(моль·К) |
|
Елементарний електричний заряд |
е |
1,602189·10-19 Кл |
Таблиця 4
Термодинамічні константи деяких речовин
|
Речовина |
кДж/моль |
кДж/моль |
Дж/(моль·К
|
|
1 |
2 |
3 |
4 |
|
Al(K) |
0 |
0 |
28,31 |
|
Al2O3(K) |
-1675,0 |
-1576,4 |
50,94 |
|
Al2(SO4)3(K) |
-3434,0 |
-3091,9 |
239,2 |
|
BaO(K) |
-556,6 |
-528,4 |
70,3 |
|
BaCO3(K) |
-1202,0 |
-1138,8 |
112,1 |
|
C(алмаз) |
1,897 |
2,866 |
2,38 |
|
С(графит) |
0 |
0 |
5,74 |
|
СО(Г) |
-110,5 |
-137,27 |
197,4 |
|
СО2(Г) |
-393,51 |
-394,38 |
213,6 |
|
СОСl2(Г) |
-223,0 |
-210,5 |
289,2 |
|
CS2(Г) |
115,3 |
65,1 |
237,8 |
|
CCl4(Г) |
-106,7 |
-63,95 |
309,7 |
|
СН4(Г) |
-74,85 |
-50,79 |
186,19 |
|
С2Н6(Г) |
-84,67 |
-32,89 |
229,5 |
|
С2Н4(Г) |
52,28 |
68,12 |
219,4 |
|
С2Н2(Г) |
226,75 |
209,2 |
200,8 |
|
С6Н6(Р) |
49,04 |
124,50 |
173,2 |
|
СН3ОН(Р) |
-238,7 |
-166,31 |
126,7 |
|
С2Н5ОН(Р) |
-227,6 |
-174,77 |
160,7 |
|
СаО(К) |
-635,1 |
-604,2 |
39,7 |
|
СaSiO3(K) |
-1579,0 |
-1495,4 |
87,45 |
|
Са3(РО4)2(К) |
-4125,0 |
-3899,5 |
240,9 |
|
СаСО3(К) |
-1206,0 |
-1128,8 |
92,9 |
|
Сl2(Г) |
0 |
0 |
222,9 |
|
Cl2O3(K) |
-1141,0 |
-1046,84 |
81,1 |
|
Fe(K) |
0 |
0 |
27,2 |
|
FeO(K) |
-263,68 |
-244,35 |
58,79 |
|
FeCl2(K) |
-341,0 |
-302,08 |
119,66 |
|
FeCO3(K) |
-744,75 |
-637,88 |
92,9 |
|
Fe2O3(K) |
-821,32 |
-740,99 |
89,96 |
|
Fe3O4(К) |
-1117,9 |
-1014,8 |
146,3 |
|
H2(Г) |
0 |
0 |
130,6 |
|
НСl(Г) |
-92,4 |
-94,5 |
186,9 |
|
1 |
2 |
3 |
4 |
|
Н2О(Г) |
-241,84 |
-228,8 |
188,74 |
|
Н2О(Р) |
-285,84 |
-237,5 |
69,96 |
|
MgO(K) |
-601,24 |
-569,6 |
26,94 |
|
N2(Г) |
0 |
0 |
191,49 |
|
N2O(Г) |
81,55 |
103,6 |
220,0 |
|
NO(Г) |
90,37 |
86,69 |
210,62 |
|
NO2(Г) |
33,89 |
51,84 |
240,45 |
|
NH3(Г) |
-46,19 |
-16,64 |
192,5 |
|
О2(Г) |
0 |
0 |
205,03 |
|
О3(Г) |
142,3 |
163,4 |
238,8 |
|
P2O5(K) |
-1492,0 |
-1348,8 |
114,5 |
|
PCl3(Г) |
-287,0 |
-260,5 |
311,7 |
|
PCl5(Г) |
-374,9 |
-305,4 |
352,7 |
|
S(ромб) |
0 |
0 |
31,88 |
|
SO2(Г) |
-296,9 |
-300,37 |
248,1 |
|
SO3(Г) |
-395,2 |
-370,37 |
256,23 |
|
H2S(Г) |
-20,15 |
-33,02 |
205,64 |
|
H2S(Р) |
-39,33 |
-27,36 |
122,2 |
|
Тi(K) |
0 |
0 |
30,7 |
|
TiO2(K) |
-943,9 |
-888,6 |
50,3 |
|
SiO2(K) |
-859,3 |
-803,75 |
42,09 |
|
ZnO(K) |
-349,0 |
-318,19 |
43,5 |
Таблиця 5