
- •0Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
Мета роботи - визначення молярної маси еквівалента карбонату кальцію.
Загальні вказівки
При виконанні даної роботи
необхідно знати, що хімічним еквівалентом
(Е)
називається реальна або умовна частинка
речовини, що може заміщувати, приєднувати,
вивільняти або будь-яким іншим чином
бути еквівалентною одному іону водню
![]() у кислотно-основних, або одному електрону
в окисно-відновних реакціях.
у кислотно-основних, або одному електрону
в окисно-відновних реакціях.
Так, наприклад, у сполуках
![]() формули еквівалентів хлору, сірки, азоту
мають вигляд:
формули еквівалентів хлору, сірки, азоту
мають вигляд:
![]() .
.
Для того, щоб визначити склад еквівалента речовини і вірно записати його хімічну формулу, необхідно виходити з конкретної реакції, в якій приймає участь дана речовина. Так, у реакціях:
|
|
|
|
|
|
|
|
|
Масу 1 моль еквівалента називають молярною масою еквівалента
( МЕ, г/моль.).
Молярні маси еквівалентів окремого елемента та складних речовин розраховують за формулами:
![]()
![]()
![]()
![]()
![]() .
.
Для розрахунку молярного об’єму газу необхідно знати кількість молів еквівалентів в одному молі газу.
Слід також звернути увагу на формулювання закону еквівалентів: речовини взаємодіють і утворюються в еквівалентних кількостях.
Так, для реакції
![]()
Оскільки
![]() , то
, то
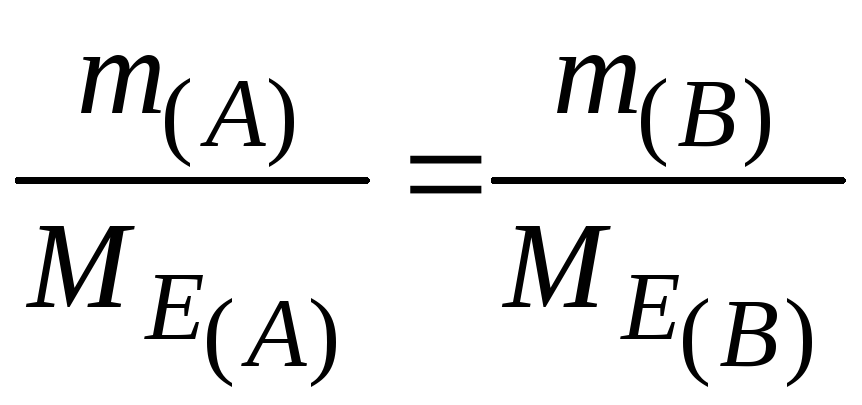 або
або
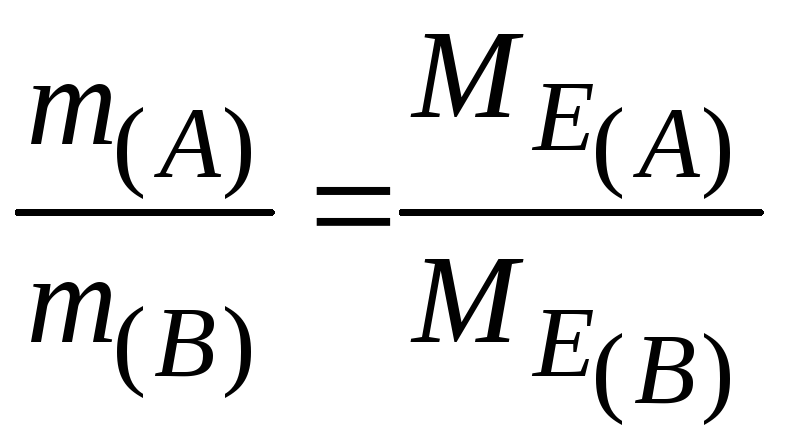
Тобто маси речовин, що взаємодіють або утворюються, пропорційні молярним масам їхніх еквівалентів.
Для газів замість мас у законі еквівалентів можна використовувати відповідні об’єми:
 або
або
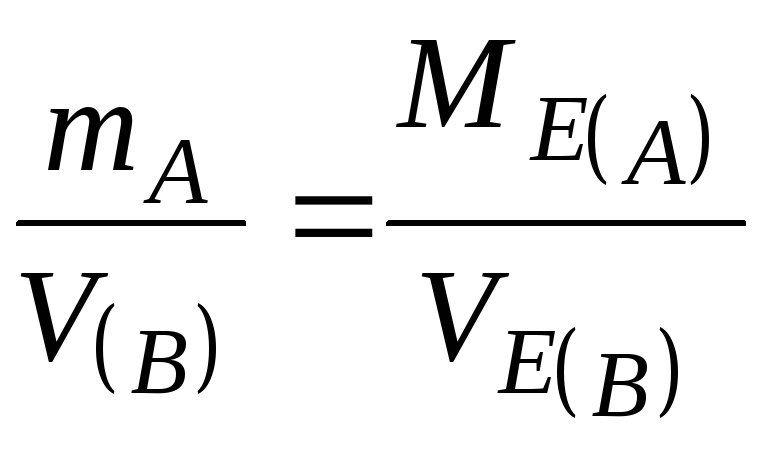
Порядок виконання роботи
Для визначення молярної маси еквівалента карбонату кальцію використовують реакцію взаємодії його з соляною кислотою
![]()
Вуглекислий газ, що утворюється при цьому збирають і вимірюють його об’єм.
З
цією метою в роботі використовується
прилад для визначення об’єму газу (рис.
2).![]()




Рис. 2 Прилад для визначення молярної маси еквівалента
- Колба Вюрца; 2 - краплинна лійка, 3 – хімічна лійка, 4 – бюретка
Помістити наважку мармуру в колбу Вюрца 1, закрити колбу пробкою з краплинною лійкою 2 і перевірити на герметичність. Для цього відкрити кран краплинної лійки і підняти хімічну лійку 3 з водою на деяку висоту. Закрити кран краплинної лійки, укріпити хімічну лійку 3 в штативі і слідкувати за рівнем рідини. Якщо прилад герметичний, то в перший момент при опусканні лійки рівень води в бюретці 4 трохи знизиться, а потім залишиться постійним.
Якщо рівень води в бюретці буде безперервно знижуватися, то прилад не герметичний. Необхідно усунути причини, що викликають негерметичність.
Якщо прилад герметичний, то треба ще раз відкрити кран краплинної лійки і пересуваючи хімічну лійку вгору, установити рівень води в бюретці на нульовій позначці або трохи нижче. Після цього закрити кран краплинної лійки і опустити хімічну лійку.
Відмірявши циліндром 10 мл розведеної соляної кислоти, помістити її в краплинну лійку і далі вилити кислоту в колбу Вюрца, де знаходиться мармур. Кран краплинної лійки перекрити в ту мить, коли в ній ще є декілька крапель кислоти, щоб не з’єднати колбу Вюрца з зовнішньою атмосферою. Під тиском газу, що утворився в результаті хімічної реакції, рідина з бюретки переходить у лійку. Після закінчення реакції і охолодження колби до кімнатної температури привести рідину в бюретці і лійці до одного рівня, тобто створити в бюретці тиск, що дорівнює атмосферному. Для цього лійку опустити вниз, записати новий рівень рідини в бюретці і показання термометра та барометра під час досліду.
Оформлення результатів роботи
Записати в журнал результати досліду:
- маса мармуру,
![]() ,
г;
,
г;
- об’єм соляної кислоти
залитий у колбу Вюрца,
![]() ,
мл;
,
мл;
- рівень рідини в бюретці:
- до реакції
![]() ,
мл;
,
мл;
- після реакції
![]() ,
мл;
,
мл;
- температура,
![]() ,
0С;
,
0С;
- тиск,
![]() мм рт. ст.
мм рт. ст.
Розрахувати об’єм газу (![]() ),
що виділився,
),
що виділився,
![]()
та абсолютну температуру, К
(Т=273+![]() ).
).
Застосувавши рівняння
Менделєєва-Клапейрона
![]() ,
обчислити масу одержаного вуглекислого
газу (
,
обчислити масу одержаного вуглекислого
газу (![]() )
(
)
(![]() 62400
мм рт.ст·мл/К моль).
62400
мм рт.ст·мл/К моль).
Скориставшись законом еквівалентів

обчислити
молярну масу еквівалента карбонату
кальцію, маючи на увазі, що молярна маса
еквівалента
![]() в реакції нейтралізації, яка відбувається
з утворенням середньої солі, дорівнює
в реакції нейтралізації, яка відбувається
з утворенням середньої солі, дорівнює
![]() моль.
моль.
Обчислити відносну помилку досліду за формулою:
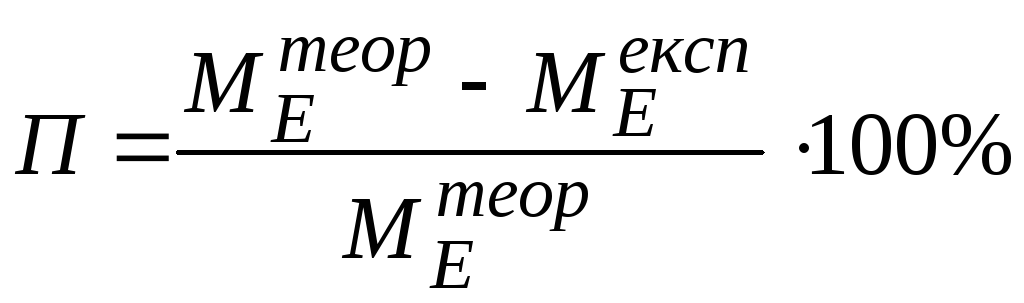 ,
,
де
![]() -
відносна помилка, %,
-
відносна помилка, %,
![]() -
теоретичне значення молярної маси
еквівалента,
-
теоретичне значення молярної маси
еквівалента,
![]() - значення молярної маси
еквівалента, обчисленої на основі
вимірювань.
- значення молярної маси
еквівалента, обчисленої на основі
вимірювань.
