
- •0Міністерство освіти і науки україни
- •Передмова
- •Загальні методичні вказівки
- •Робоча програма
- •Додаткова література
- •Основні поняття та закони хімії основні поняття та визначення
- •Приклади виконання завдань
- •28 Г n2займають об’єм 22,4 л
- •Контрольні завдання
- •Термохімія та термохімічні розрахунки основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: 27822,2 кДж/кг
- •Відповідь: 25,12 кДж.
- •Можливість та напрямленість перебігу реакцій основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Відповідь: - 91,016 кДж
- •Відповідь: -131,58 кДж
- •Відповідь: -1235,18 кДж
- •Відповідь: - 35,75 кДж
- •Відповідь: 313,94 кДж
- •230. Користуючись значеннями стандартних теплот утворення та абсолютних стандартних ентропій, обчислити реакції, що відбувається за рівнянням
- •Хімічна кінетика та рівновага основні поняття та визначення
- •Приклади виконання завдань
- •Швидкість реакції зросла у
- •Контрольні завдання
- •Відповідь: 2,6.
- •Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
- •Розчини основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Властивості розчинів неелектролітів основні поняття і визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Розчини електролітів основні поняття та визначення
- •Приклади виконання завдань
- •У результаті гідролізу в розчині виникає надлишок іонів , які зумовлюють лужне середовище ().
- •Контрольні завдання
- •Будова атома основні поняття та визначення
- •Приклади розв’язання задач
- •Контрольні завдання
- •Періодична система елементів д.І.Менделєєва приклади розв’язання задач
- •Контрольні завдання
- •Хімічний зв’язок основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Окиcно-відновні реакції основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електродні потенціали. Гальванічні елементи основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання. Схема даного гальванічного елемента
- •Контрольні завдання
- •Корозія металів основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Електроліз основні поняття та визначення
- •Приклади виконання завдань
- •Контрольні завдання
- •Метали контрольні завдання
- •Неметали контрольні завдання
- •Твердість води основні поняття та визначення
- •Приклади виконання завдань
- •Розв’язання.Оскільки твердість води показує число ммоль еквівалентів солей в 1 л її, розрахуємо твердість води за формулою:
- •20 (Мг/ммоль).
- •5 (Ммоль е/л).
- •Приклад 3 Визначити масу фосфату натрію, необхідну для пом’якшення 1м3 води з загальною твердістю 8 ммоль е/л.
- •Контрольні завдання
- •2,3 Ммоль е/л.
- •Відповідь: 8 ммоль е/л
- •Неорганічні в’яжучі речовини основні поняття та визначення
- •Контрольні завдання
- •Елементи органічної хімії. Органічні полімерні матеріали основні поняття та визначення
- •Контрольні завдання
- •Правила техніки безпеки та перша допомога в нещасних випадках
- •Деякі основи та їхні залишки
- •Деякі кислоти та їхні залишки
- •Лабораторна робота № 2 визначення молярної маси еквівалента складної речовини
- •Питання для самоперевірки
- •Лабораторна робота № 3 визначення теплових ефектів хімічних реакцій
- •Порядок виконання роботи
- •Хімічна кінетика
- •Хімічна рівновага
- •Лабораторна робота № 6 приготування розчину даної концентрації і встановлення його титру
- •Питання для самоперевірки
- •Лабораторна робота № 7 електролітична дисоціація. Реакції в розчинах електролітів
- •Гідроліз солей
- •Лабораторна робота № 9 електрометричне визначення рН розчинів електролітів
- •Оформлення результатів роботи
- •Питання для самоперевірки
- •Адсорбція
- •Дослід 1. Приготування суспензії крейди у воді.
- •2 Процес окиснення
- •1. Які реакції називаються окисно-відновними?
- •Властивості алюмінію та заліза
- •Лабораторна робота № 16 комплексні сполуки
- •Корозія металів
- •Дослід 2. Електрохімічна корозія оцинкованого і лудженого заліза.
- •Визначення карбонатної твердості води
- •Лабораторна робота № 19 визначення агресивного діоксиду вуглецю
- •Визначення процентного вмісту оксидів кальцію та магнію у вапні
- •Обчислити процентний вміст у вапні за формулою:
- •Кремній та його сполуки
- •Спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Для прискореної форми навчання спеціальність 7.092101 “промислове і цивільне будівництво”
- •Спеціальність 7.092108 “теплогазопостачання і вентиляція”
- •Періодична система хімічних елементів д.І.Менделєєва
- •Деякі одиниці міжнародної системи (сі)
- •Значення деяких фундаментальних фізичних сталих
- •Термодинамічні константи деяких речовин
- •Растворимость солей, кислот и оснований в воде
- •Відносна електронегативність деяких елементів (таблиця полинга)
- •Стандартні потенціали металевих і газових електродів
Як зміняться швидкості прямої та зворотної реакцій і в якому напрямку зміститься рівновага при збільшенні об’єму системи вдвічі?
308. Як зміняться швидкості прямої і зворотної реакцій в гетерогенній системі
![]() ,
,
якщо підвищити тиск у системі в 3 рази? В якому напрямку зміститься рівновага?
309. Чи зміститься хімічна рівновага в гомогенній системі
![]()
при зменшенні об’єму в 1,5 рази? Висновок обґрунтувати розрахунками зміни швидкостей прямої та зворотної реакцій.
310. Розрахувати зміну швидкостей прямої та зворотної реакцій в гетерогенній системі
![]()
при збільшенні об’єму в 1,5 рази. В якому напрямку зміститься рівновага?
311. Як зміняться швидкості прямої та зворотної реакцій в гомогенній системі
![]() ,
,
якщо зменшити тиск втричі? В якому напрямку зміститься хімічна рівновага?
312. Чи зміститься хімічна рівновага в гомогенній системі
![]()
при зменшенні об’єму вдвічі? Як при цьому зміняться швидкості прямої та зворотної реакцій?
313. В якому напрямку зміститься хімічна рівновага в системі
![]()
та як зміняться швидкості прямої та зворотної реакцій при збільшенні тиску в 3 рази?
314. Розрахувати зміну швидкостей прямої та зворотної реакцій в гетерогенній системі
![]()
при зменшенні тиску удвічі. В якому напрямку зміститься хімічна рівновага?
315. Як зміняться швидкості прямої та зворотної реакцій в гомогенній системі
![]() ,
,
якщо зменшити об’єм удвічі? В якому напрямку зміститься хімічна рівновага?
316. Чи зміститься хімічна рівновага в гетерогенній системі
![]()
при збільшенні об’єму втричі? Як зміняться при цьому швидкості прямої та зворотної реакцій?
317. В якому напрямку зміститься хімічна рівновага в системі
![]()
та як зміняться швидкості прямої та зворотної реакцій при зростанні об’єму системи в 3 рази?
318. Розрахувати зміну швидкостей прямої та зворотної реакцій в гомогенній системі
![]()
при зменшенні об’єму системи вдвічі. В якому напрямку зміститься хімічна рівновага?
319. Як зміняться швидкості прямої та зворотної реакцій в гетерогенній системі
![]() ,
,
якщо збільшити об’єм системи в 2 рази? В якому напрямку зміститься хімічна рівновага?
320. Розрахувати зміну швидкостей прямої та зворотної реакцій в гетерогенній системі
![]()
при підвищенні тиску в 3 рази? В якому напрямку зміститься хімічна рівновага?
321. В якому напрямку відбудеться зміщення хімічної рівноваги при збільшенні а) температури, б) тиску в системах:
![]()
322. В якому напрямку відбудеться зміщення хімічної рівноваги при збільшенні а) об’єму, б) температури в системах:
![]()
323. За яких умов рівновага реакції
![]()
буде зміщуватися в бік утворення хлору?
324. Як впливатиме підвищення а) температури, б) тиску на стан рівноваги в таких системах:
![]()
325. За яких умов рівновага реакції
![]()
зміщується праворуч?
326.
Як максимально підвищити вихід
![]() (змістити рівновагу праворуч) у системі:
(змістити рівновагу праворуч) у системі:
![]()
327. За яких умов рівновага реакції
![]()
зміщується ліворуч?
328.
Як максимально підвищити вихід
![]() (змістити рівновагу праворуч) в системі:
(змістити рівновагу праворуч) в системі:
![]()
329. В якому напрямку відбудеться зміщення хімічної рівноваги в системі
![]() ,
,
якщо: а) підвищити температуру, б) зменшити об’єм ?
330. В який бік зміститься рівновага в системі
![]() ,
,
якщо: а) збільшити тиск, б) зменшити концентрації реагуючих речовин, в) підвищити температуру?
331. За яких умов рівновага в системі
![]()
зміститься ліворуч?
332. Як максимально підвищити вихід HJ (змістити рівновагу праворуч)
![]() ?
?
333. В якому напрямку відбудеться зміщення рівноваги при підвищенні температури в системах:
![]()
334. В якому напрямку відбудеться зміщення рівноваги при підвищенні концентрації реагуючих речовин у системах:
![]()
335.Як впливатиме на рівновагу реакції
![]()
а) збільшення концентрації
![]()
б) збільшення концентрації
![]()
в) підвищення тиску;
г) збільшення об’єму реакційної посудини?
336. В якому напрямку відбудеться зміщення рівноваги в системах:
![]()
якщо: а) підвищити тиск; б) зменшити об’єм газової суміші?
337. Як впливатиме на рівновагу реакції
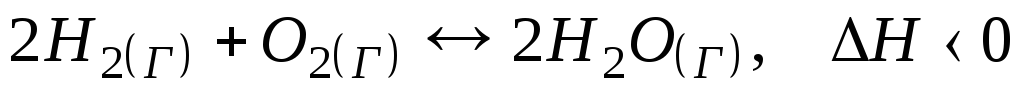
а) підвищення температури;
б) підвищення тиску;
в)
зниження концентрації
![]()
338. В якому напрямку відбудеться зміщення рівноваги в системах:
![]()
якщо: а) зменшити тиск, б) збільшити об’єм реакційної посудини, в) підвищити температуру?
339. В якому напрямку відбудуться зміщення рівноваги в системах:
![]()
якщо:
а) зменшити концентрації
![]() і
і![]() ;
б) підвищити температуру; в) збільшити
об’єм газової суміші?
;
б) підвищити температуру; в) збільшити
об’єм газової суміші?
340. В якому напрямку відбудеться зміщення рівноваги в системах:
![]()
якщо: а)
збільшити концентрації
![]() ;
б) підвищити температуру; в) зменшити
тиск?
;
б) підвищити температуру; в) зменшити
тиск?
