
- •Предисловие
- •Введение молекулярная физика и термодинамика
- •1. Основы молекулярно-кинетической теории газов
- •1.1. Основное уравнение кинетической теории газов
- •1. 2. Вероятность
- •1.3. Распределение Максвелла
- •1.4. Экспериментальная проверка закона распределения.
- •1.5. Распределение Больцмана. Барометрическая формула.
- •1.6 Распределение Гиббса
- •1.7 Средняя длина свободного пробега молекул
- •1.8 Распределение энергии по степеням свободы.
- •1.9 Явления переноса
- •Соотношения между коэффициентами переноса
- •2 Термодинамика
- •2.1Первое начало термодинамики
- •2.2. Теплоемкость идеальных газов и адиабатный процесс
- •2.3 Энтропия
- •2.4 Второе начало термодинамики
- •2.5 Цикл Карно и кпд тепловой машины
- •3.1 Реальные газы
- •Вопросы Основные понятия молекулярной физики.
- •Молекулярно-кинетическая теория идеального газа
- •I – е начало термодинамики
- •II – е начало термодинамики
- •Фазовое равновесие и фазовые превращения
- •Примеры решения задач.
- •27 Библиографический список
- •Приложение Математические постоянные
- •Интегралы
- •Основные интегралы и соотношения кинетической теории газов.
- •Таблицы
Соотношения между коэффициентами переноса
![]() ,
,
![]() ,
,
![]()
2 Термодинамика
Теплота-это энергия, которая переходит от одного тела к другому из-за разницы в их температурах. Другими словами, это способ передачи энергии от одного тела к другому. Под работой понимают любой способ передачи энергии, который не связан с разностью температур. Термодинамика имеет дело с процессами, в которых передается теплота и совершается работа.
2.1Первое начало термодинамики
 Равновесное
состояние системы определяется
переменными P, V, T и числом молей газа ν.
Когда над системой совершается работа
(например, сжатие газа) или когда в
систему поступает или отбирается
теплота, состояние системы изменяется.
Работа и теплота входят в термодинамические
процессы, которые могут переводить
систему из одного состояния в другое,
но не являются характеристиками самого
состояния в отличие от таких величин
как давление, объем, температура и масса.
Равновесное
состояние системы определяется
переменными P, V, T и числом молей газа ν.
Когда над системой совершается работа
(например, сжатие газа) или когда в
систему поступает или отбирается
теплота, состояние системы изменяется.
Работа и теплота входят в термодинамические
процессы, которые могут переводить
систему из одного состояния в другое,
но не являются характеристиками самого
состояния в отличие от таких величин
как давление, объем, температура и масса.
Рис.2.1.1
Рассчитаем работу, совершаемую в простом
термодинамическом процессе при
изменении объема, когда п
Рис.2.1.1.
![]() ,
,
где S- площадь поршня; p- давление газа.
Работа, совершаемая при изменении объема от V1 до V2,
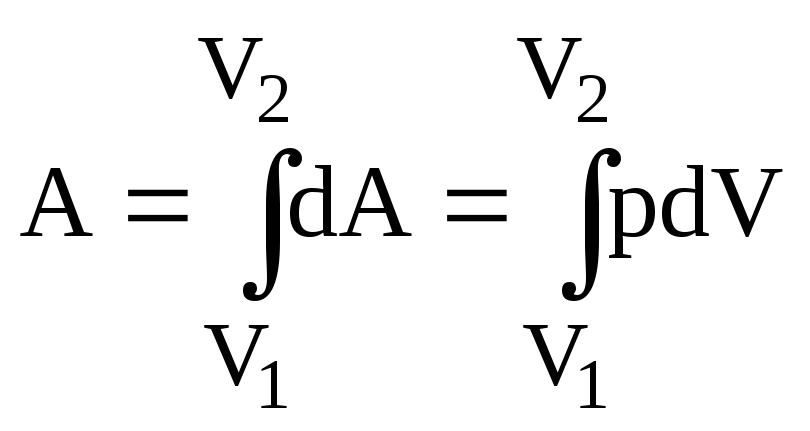 (2.1.1).
(2.1.1).
Чтобы проинтегрировать данное выражение надо знать, как изменяется давление, а это зависит от вида процесса. Процессы могут быть:
Изотермическими
Изохорическими
Изобарическими
Чтобы проинтегрировать выражение 2.1.1 , используем уравнение состояния идеального газа:
![]()
где ν- число молей вещества.
Работа при
изотермическом процессе, согласно 2.1.1
, равна площади между кривой на pV диаграмме
и осью V (рис.2.1.2):
 (2.1.2).
(2.1.2).
Однако газ из
положения 1 в 2 можно перевести по любой
ломаной a-b-c. Первый участок a-b- при
постоянном объеме. Работа при этом равна
нулю. На втором участке b-c давление
остается постоянным, поэт
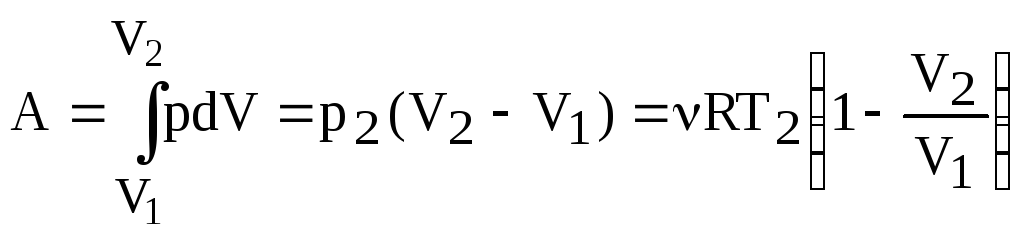 (2.1.3)
(2.1.3)
Работа газа равна площади ограниченной кривой a-b-c и осью V. Сравнивая формулы (2.1.2) и (2.1.3) и определяемые ими площади на диаграмме, можно заключить, что величина работы и изменение количества теплоты при переходе системы из одного состояния в другое зависят не только от начального и конечного состояния, но и от вида процесса.
Теперь введем понятие внутренней энергии.
Внутренней энергией системы называют полную сумму всех видов энергии всех молекул, принадлежащих системе.

Рис.2.1.2
Следует различать температуру Т, количество теплоты Q и внутреннюю энергию U. Температура служит мерой средней кинетической энергии отдельных молекул системы. Теплота характеризует передачу энергии вследствие разницы температур.
Внутренняя энергия системы увеличивается при совершении над ней работы внешними силами, либо при передаче ей тепла из вне. Подчеркнем, что внутренняя энергия системы является функцией состояния p, V, T и не зависит от способа, которым это состояние было достигнуто.
На основании многочисленных опытов установлен закон сохранения энергии применительно к термодинамике- первое начало термодинамики:
![]()
![]()
![]() .
(2.1.4).
.
(2.1.4).
Тепло, подведенное к замкнутой системе, расходуется на повышение ее внутренней энергии и работу, производимую системой против внешних сил.
Пример 10. Определить совершенную работу и изменение внутренней энергии 1 кг воды, когда она полностью выкипает и превращается в пар при температуре 100 0С. Давление равно 1 атм.
Решение. Объем воды при температуре 100 0С равен 1·10-3 м3. Пар массой 1 кг при 1000С занимает объем 1,67 м3.(см. таблицу плотности жидкостей и газов). Следовательно, совершенная работа
A=p(V2-V1)=1,01105 Н/м2(1,б7 - 110-3)м3=1,69105 Дж
Количество теплоты, необходимое для вскипания 1 кг воды равно теплоте испарения.
Q=Lm=22,6105 Дж
Согласно первому началу термодинамики,.
U=Q - A =20,9105 Дж.
Значит 8% переданной воде теплоты идет на совершение работы, а 92% на изменение внутренней энергии воды.
