
- •ВСТУП
- •2. ТЕОРЕТИЧНІ ОСНОВИ ОРГАНІЧНОЇ ХІМІЇ
- •2.1. Типи хімічних зв’язків
- •2.2. Характеристики ковалентного зв’язку
- •2.3. Будова атома карбону
- •2.4. Метод валентних зв’язків
- •2.5. Метод МО ЛКАО
- •2.6. Класифікація органічних реакцій
- •2.7. Проміжні частинки в органічних реакціях. Взаємний вплив атомів у молекулах
- •3. АЛКАНИ
- •4. АЛКЕНИ
- •6. АЛКАДІЄНИ
- •7. ЦИКЛОАЛКАНИ
- •8. АРОМАТИЧНІСТЬ
- •9. АРЕНИ
- •11. БАГАТОЯДЕРНІ АРОМАТИЧНІ СПОЛУКИ
- •12. ГАЛОГЕНОПОХІДНІ ВУГЛЕВОДНІВ
- •13. ЕЛЕМЕНТООРГАНІЧНІ СПОЛУКИ
- •14. СУЛЬФОКИСЛОТИ
- •15. СПИРТИ
- •16. ФЕНОЛИ
- •17. ЕТЕРИ. ЕПОКСИСПОЛУКИ
- •18. ТІОСПИРТИ. ТІОЕТЕРИ
- •19. АЛІФАТИЧНІ АЛЬДЕГІДИ ТА КЕТОНИ
- •20. АРОМАТИЧНІ АЛЬДЕГІДИ І КЕТОНИ
- •21. АЛІФАТИЧНІ НІТРОСПОЛУКИ
- •22. АРОМАТИЧНI НIТРОСПОЛУКИ
- •23. АЛІФАТИЧНІ АМІНИ
- •24. АРОМАТИЧНІ АМІНИ
- •25. ДІАЗО– І АЗОСПОЛУКИ
- •26. МОНОКАРБОНОВІ КИСЛОТИ
- •27. ДИКАРБОНОВІ КИСЛОТИ
- •28. АРОМАТИЧНІ КАРБОНОВІ КИСЛОТИ
- •29. ЗАМІЩЕНІ КИСЛОТИ
- •29.1. ГАЛОГЕНЗАМІЩЕНІ КИСЛОТИ
- •29.2. АМІНОКИСЛОТИ
- •29.3. ГІДРОКСИКИСЛОТИ
- •30. АЛЬДЕГІДОКИСЛОТИ І КЕТОКИСЛОТИ
- •31. ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
- •31.1. КЛАСИФІКАЦІЯ ТА НОМЕНКЛАТУРА ГЕТЕРОЦИКЛІЧНИХ СПОЛУК
- •31.2. П’ЯТИЧЛЕННІ ГЕТЕРОЦИКЛІЧНІ СПОЛУКИ
- •31.3. ШЕСТИЧЛЕННІ ГЕТЕРОЦИКЛИ
- •31.4. КОНДЕНСОВАНІ ГЕТЕРОЦИКЛИ
- •31.5. ПОЛІГЕТЕРОЦИКЛИ
- •32. ВУГЛЕВОДИ
- •32.1. МОНОСАХАРИДИ
- •32.2. ПОЛІСАХАРИДИ
- •СПИСОК ЛІТЕРАТУРИ

|
|
Cl |
|
|
NaOH |
|
H2SO4 |
|
Cl2 |
|
NaOH |
H2SO4 |
||||
|
|
|
|
|
|
А |
|
|
||||||||
CH3 |
CH2 |
CH |
|
CH3 |
||||||||||||
|
|
|
|
|
Б |
|
В |
|
|
Г |
||||||
|
водн. р-н |
|
|
|
водн. р-н |
|||||||||||
ДCH3OH Е Na Ж CH3I З
15.31.Пояснити, чому метанол має вищу температуру кипіння в порівнянні з метилхлоридом та етаном (молярні маси останніх двох продуктів більші). Чим пояснюється висока розчинність нижчих спиртів у воді?
15.32.Ізомасляний альдегід отримують в промисловості з ізобутилену за схемою:
|
CH3 |
Cl2 |
|
H2O |
|
t0 |
O |
|
|
CH3 |
|
|
|||
CH2 |
C |
|
CH3 |
А |
Б |
|
C |
|
CH |
|
CH |
|
|||
|
|
Ca(OH)2 |
H+ |
H |
|
|
3 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Заповнити схему перетворень, навести можливий механізм останньої стадії.
15.33.Пояснити різні напрямки перебігу реакцій нуклеофільного заміщення:
CH2 CH CH2 CH2 OH + HBr -H2O  CH2 CH CH2 CH2 Br
CH2 CH CH2 CH2 Br
CH3 |
CH |
|
CH |
|
CH2 |
OH + HBr |
|
|
CH3 |
|
|
CH |
|
|
CH |
|
|
CH2 |
|
Br (85%) |
||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
Br |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
-H2O |
|
CH |
|
|
|
|
CH |
|
|
CH |
|
(15%) |
|||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
16. ФЕНОЛИ
Питання для самопідготовки
Класифікація та номенклатура. Фізічні властивості. Кислотність фенолів. Вплив будови на кислотність фенолів. Особливості реакцій електрофільного заміщення фенолів. Реакції окиснення. Хінони.
Контрольні завдання
16.1.Пояснити, чим зумовлені кислотні властивості фенолу? Порівняти та пояснити кислотні властивості фенолу (рКа=10,0), оцтової (рКа=4,7) та карбонатної (рКа=6,36) кислот. Яка сполука утворюється при пропусканні карбону діоксиду через водний розчин феноляту натрію? Навести рівняння відповідних реакцій та якісних реакцій на феноли.
16.2.Заповнити схему перетворень та назвати продукти:
HO |
H2SO4 |
А |
NaOH |
Б |
NaOH |
В |
(H+) |
Г |
[O] |
Д |
HBr |
Е |
|
1000C |
(H |
O) |
сплавляння |
|
|
|
|||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
Пояснити будову сполуки Д і навести механізм перетворення Д в Е.
16.3.Заповнити схему перетворень і назвати продукти:
SO3Na |
2NaOH |
|
HCl |
|
|
|
A |
Б |
|||
|
(сплавляння |
) |
|
||
|
98 |
|
|
|
|
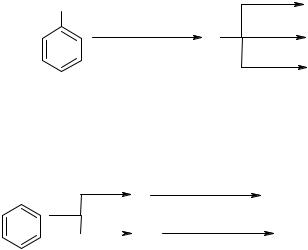
Пояснити будову сполуки Б і порівняти відношення цієї сполуки та циклогексанолу до дії: а) HВr ; б) оцтової кислоти. Відповідь обґрунтувати.
16.4.Навести схему перетворень і назвати продукти:
NH2 |
|
HCN Б |
|
[O] |
А |
NaHSO3 |
В |
(хроматна кислота) |
|
||
|
NH2OH |
|
|
|
|
Г |
|
|
|
|
|
Пояснити будову сполуки А та її реакційну здатність. Пояснити загальний механізм реакцій: А Б, А В, А Г.
16.5.Заповнити схему перетворень і назвати всі сполуки:
CH |
3 |
|
(h ) |
|
H O, (NaOH), t0 |
|
||
|
|
|
|
|
А |
2 |
Б |
|
|
|
|
Cl2 |
H2O, (NaOH), t0 |
||||
|
|
|
|
|
|
|||
|
|
|
|
(FeCl ) |
|
|
|
|
|
|
|
3 |
|
В, Г |
|
Д, Е |
|
|
|
|
|
|
|
P, каталізатор |
||
|
|
|
|
|
|
|
|
|
Навести реакції, за допомогою яких можна розрізнити сполуки Б, Д, Е. Пояснити відмінності у властивостях цих речовин.
16.6.Навести схеми реакцій, які відбуваються при послідовній дії на фенол таких речовин: а) розведеної нітратної кислоти; б) диметилсульфату в лужному середовищі; в) заліза в присутності хлоридної кислоти; г) ацетилхлориду. Назвати продукти, навести і пояснити механізм реакції г).
16.7.Навести структурну формулу сполуки С8Н10О, яка дає солі з лугами і метилюється диметилсульфатом в лужному середовищі. При окисненні продукту метилювання утворюється п-метоксибензойна кислота. Назвати сполуку С8Н10О і навести схеми всіх реакцій. Навести і пояснити схему добування сполуки С8Н10О з бензолу.
16.8.Порівняти способи добування, будову і властивості п-крезолу та ізомерного йому бензилового спирту. Відповідь обгрунтувати за допомогою відповідних реакцій.
16.9.Навести структурну формулу сполуки С6Н6О6S2, яка при дії водного розчину лугу утворює речовину С6Н4О6S2Nа2, яка при сплавлянні з лугом і наступному підкисленні утворює резорцин. Навести і пояснити схеми відповідних реакцій.
16.10.Сполука С7Н8О взаємодіє з лугом, при додаванні розчину хлориду заліза(III) дає блакитне забарвлення, а при дії діазометану утворює сполуку С8Н10О, продуктом окиснення якого є п-метоксибензойна кислота. Навести структурну формулу речовини С7Н8О, назвати її. Пояснити схему реакцій добування сполуки С7Н8О з бензолу.
16.11.Заповнити схему перетворень і назвати продукти:
99
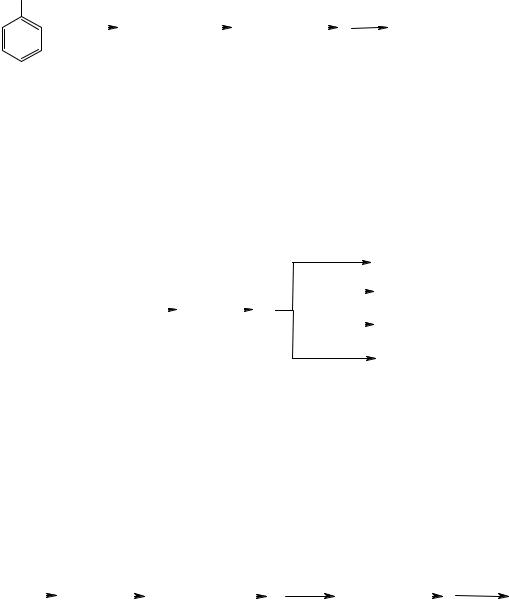
OH
H2SO4 |
A |
NaOH |
|
Б |
NaOH (тв) |
В |
(H+) |
Г |
200C |
(водн. розчин) |
(сплавляння) |
|
|||||
Для сполуки Г навести схеми реакцій: а) з ацетатом плюмбуму (ІІ); б) з ацетилхлоридом; в) окиснення. Назвати всі продукти.
16.12.Навести способи добування резорцину. Порівняти та пояснити: кислотні властивості резорцину і фенолу; швидкість реакції нітрування резорцину і фенолу; характер взаємодії з воднем резорцину і фенолу.
16.13.Заповнити схему перетворень і назвати продукти:
|
|
|
|
|
Na (метал) В |
||
|
1Cl |
|
H O, t0 |
|
NaOH |
|
Г |
|
|
|
|
|
|||
о-крезол |
2 |
A |
2 |
Б |
CH3COCl |
|
|
h |
|
|
Д |
||||
|
|
|
|
|
|
||
CH3COOH Е
Відповідь обґрунтувати.
16.14.Пояснити, чому на відміну від фенолу, 2,4-динітрофенол і 2,4,6-тринітрофенол розчинні у водному розчині гідрокарбонату натрію. Навести схеми відповідних реакцій. Пояснити механізм. Навести схеми добування 2,4,6-тринітрофенолу, використовуючи як вихідну речовину бензол. Пояснити умови перебігу реакцій.
16.15.Заповнити схему послідовних перетворень і назвати всі сполуки:
|
CH3I |
|
|
Fe+HCl |
|
NaNO |
+2HCl |
|
H |
O, t0 |
|
С |
H |
COCl |
|
H |
O, t0 |
|
о-нітрофенол |
|
А |
Б |
2 |
|
В |
2 |
|
Г |
6 |
5 |
|
Д |
2 |
|
Е |
||
(NaOH) |
|
00C |
(H+) |
(піридин) |
(H+) |
|||||||||||||
|
|
|
|
|
|
|
|
|||||||||||
16.16.Із бензолу добути п-нітрофенол. Порівняти та пояснити кислотні властивості фенолу і п- нітрофенолу. Отримати етер та естер п-нітрофенолу. Навести і пояснити механізми цих реакцій.
16.17.Навести структурну формулу сполуки С6Н6О6S2, яка при дії водного розчину гідроксиду натрію дає сполуку С6Н4О6S2Nа2, при нагріванні якої до температури 300 оС з твердим NaOH та підкисленні утворює сполуку С6Н6О2, яка при взаємодії з розчином ацетату плюмбуму (ІІ) утворює осад. Навести схеми відповідних реакцій та назвати всі сполуки. Для сполуки С6Н6О2 навести схеми реакцій: а) окиснення; б) з метилйодидом в лужному середовищі; в) ацилювання.
16.18.Здійснити перетворення і назвати всі процеси і сполуки:
100

|
|
|
|
|
|
|
хлорид бензолдіазонію В |
|
хлорбензол |
HNO ! |
А |
(H |
O),to |
Б |
ацетилхлорид |
Г |
|
H SO ! |
2 |
|
|
|||||
|
|
3 |
|
|
|
|
|
|
|
2 |
4 |
|
|
|
|
Fe + HCl Д [O] Е |
|
|
|
|
|
|
|
|
||
Пояснити умови перебігу реакції Б В.
16.19. Навести приклади таких сполук: а) заміщеного фенолу, який реагує з содою; б) заміщеного фенолу, який не реагує з НNО2 і не вступає в реакцію азосполучення ; в) двохатомного фенолу , при окисненні якого утворюється хінон. Відповідь обґрунтувати. Навести схеми відповідних реакцій.
16.20.Визначити будову сполуки складу С7Н8О , яка розчиняється у водному розчині лугу, але
нерозчинна у водному розчині гідрокарбонату натрію, а з бромною водою дає сполуку С7Н5ОВr3 . Назвати ці сполуки, навести схеми реакцій, та рівняння реакції С7Н8О з ацетилхлоридом.
16.21.Навести промислові методи добування фенолу та запропонувати схеми перетворення його: а) в поліамідну смолу "найлон"; б) в поліамідну смолу "капрон"; в) в фенолформальдегідні смоли.
16.22.Навести схеми реакцій добування фенолу а) із бензолсульфокислоти; б) із хлорбензолу; в) із ізопропілбензолу. Пояснити механізм реакцій б) і в). Які переваги перед іншими має спосіб в)? Написати реакції фенолу в присутності NaOH: а) з CH3I; б) з C2H5Br. Пояснити механізм і назвати продукти реакції.
16.23.Навести схеми добування п-бензохінону у промисловості і в лабораторії. Написати рівняння реакцій бензохінону: а) з НСN; б) з ізопреном; в) з CH3MgBr; г) гідрування. Пояснити механізми реакцій.
16.24.Добути феноли лужним гідролізом сполук а)-г), дати назви сполукам:
|
|
|
Cl |
|
|
Cl |
а) |
Cl |
б) |
в) |
Cl |
г) O2N |
NO2 |
|
|
|
NO2 |
NO2 |
|
|
|
|
|
|
|
|
NO2 |
В якій сполуці найлегше заміщується атом хлору на гідроксигрупу? Пояснити причину і механізм реакції гідролізу. Для фенолу навести реакції бромування у водному та неводному середовищах, пояснити їх відмінності.
101

16.25.Заповнити схему перетворень, назвати всі сполуки:
CH CH |
CH |
|
|
|
|
|
|
CO2 |
|
Г |
3 |
|
3 |
|
|
|
|
|
P , t0 , кат. |
||
|
|
|
|
|
|
|
|
|
||
|
|
O2 |
А |
нагрівання |
Б |
NaOH |
В |
|
|
|
|
|
(каталіз) |
(Н+) |
|
|
C2H5I |
Д |
|
||
|
|
|
|
|
|
|
|
NaOH |
|
|
Навести механізм перетворення сполуки (А) в сполуку (Б) і перетворення (В) в сполуку (Г). Пояснити використання продуктів Г і Д.
16.26.Здійснити перетворення, назвати всі сполуки:
п-нітрохлорбензол |
гідроліз |
|
відновлення |
|
окиснення |
|
4Cl2 Г |
|
А |
Б |
В |
HCl |
|
||||
|
(Fe + HCl) |
|
Д |
|||||
|
|
|
|
|
|
|
|
|
Де використовується сполука Г? Навести і пояснити механізм добування сполук А і Б.
16.27.Здійснити перетворення, назвати всі процеси і сполуки:
|
|
|
|
|
HNO3 |
В |
CH3 |
CH CH2 |
A |
[O] |
|
H2SO4 |
Г |
Б |
[O] |
|
||||
H3PO4 |
|
Д |
||||
|
|
|
||||
Zn  Е
Е
Навести і пояснити механізм добування сполуки Б.
16.28.Здійснити перетворення, назвати всі процеси і сполуки:
|
|
|
|
HNO3 |
В |
|
|
|
|
|
|
Cl |
|
|
|
H2SO4 |
Г |
2NaOH |
|
CH3I |
|
O |
|
A |
Б |
|
|||
C C Cl |
|
||||
t |
|
|
|||
|
|
H |
|
||
|
|
|
3 |
|
Д |
|
|
|
|
AlCl3 |
|
|
|
|
|
|
|
|
|
|
|
Cl2 |
Е |
|
|
|
|
AlCl3 |
|
|
|
|
|
|
Пояснити механізм утворення сполуки Д.
16.29.Назвати та розташувати сполуки а)-є) за зменшенням кислотних властивостей:
а) |
OH б) |
OH в) |
OH |
г) |
OH |
д) |
OH |
|
е) |
OH |
|
|
|
CH3 |
|
|
NO2 |
|
NO2 |
O2N |
NO2 |
|
|
CH3 |
CH3 |
|
|
|
NO2 |
|
|
NO2 |
Відповідь обгрунтувати. З бензолу добути п-крезол в кілька стадій.
102
