
- •Фізична хімія
- •Розчини електролітів. Електрохімія
- •Основні поняття, рівняння і символи
- •Приклади розв’язку типових задач
- •Завдання для самостійної роботи Задача 1.1
- •Варіанти завдань до задачі 1.1
- •Приклад розв’язку задачі 1.1
- •А) Розв’язок задачі для слабкого електроліту.
- •Значення питомої і молярної електропровідності
- •Б) Приклад розв’язку задачі для сильного електроліту
- •Контрольні задачі
- •Хімічна кінетика
- •Основні рівняння і символи
- •Приклади розв’язку типових задач
- •0.25 Моль/л
- •Задачі для самостійної роботи Задача 2.1
- •Варіанти завдань до задачі 2.1
- •Задача 2.2
- •Варіанти завдань до задачі 2.2
- •Задача 2.3
- •Варіанти завдань до задачі 2.3
- •Задача 2.4
- •Варіанти завдань до задачі 2.4
- •Вихідні дані до задачі 2.4
- •Приклад розв’язку задачі 2.1
- •Експериментальні значення кінетичних досліджень
- •Результати розрахунку констант швидкості
- •Дані для побудови графіків
- •Приклад розв’язку задачі 2.2
- •Приклад розв’язку задачі 2.3
- •Константи швидкості та термодинамічні параметри реакції
- •Приклад розв’язку задачі 2.4
- •Вихідні дані до задачі 2.4
- •Результати розрахунку квантового виходу реакції
- •Контрольні задачі
- •Список літератури
- •Фізична хімія
Константи швидкості та термодинамічні параметри реакції
|
T, K |
k0, м3/(моль·с) |
ΔH≠, Дж/моль |
ΔS≠, Дж/(моль·К) |
|
325 |
5,825∙1014 |
97706 |
20,95 |
|
335 |
5,229∙1014 |
97623 |
19,26 |
|
345 |
5,602∙1014 |
97540 |
19,59 |
|
355 |
5,878∙1014 |
97457 |
19,75 |
|
365 |
6,200∙1014 |
97373 |
19,96 |
Приклад розв’язку задачі 2.4
Необхідні для розв’язку дані знаходимо в таблицях завдань до задачі 2.4:
Реакція:
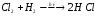
Речовина, з якою взаємодіє квант світла: Cl2;
Вільні радикали, на яких відбувається обрив ланцюга: Cl●
Таблиця 2.19
Вихідні дані до задачі 2.4
|
, нм |
N10-18 |
Е1, Дж/с |
Z, с |
Е2, Дж |
β |
|
170 173 175 178 |
11,34 21,25 17,18 12,38 |
0,510-3 |
330 |
387 |
0,095 |
1.
Механізм протікання реакції

можна представити наступним чином:
Зародження ланцюга

Ріст
ланцюга
(обов'язковою умовою є наявність активної
частинки, що присутня на початку ланцюга,
в кінці ланцюга. В даному випадку -
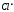 )
)

Обрив
ланцюга 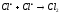
2. Квантовий вихід реакції розраховуємо за рівнянням:
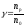 ,
,
де nр – кількість молекул, які прореагували під дією світла; n0 – кількість поглинених квантів світла.
Кількість квантів світла, що поглинаються системою за 1 секунду, розраховуємо за рівнянням:
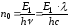 ,
,
де стала Планка h = 0,6610-33 Дж/с; швидкість світла с = 3,0108 м/с; Е1 – кількість енергії, яка поглинається системою за 1 секунду; - довжина світлової хвилі.
Кількість молекул вихідної речовини, які прореагували за 1 секунду, рівна:
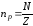
За умовою задачі Е1= 0,510-3Дж/с, Z = 330 c. Розрахуємо кількість квантів світла за умови, що = 170 нм:
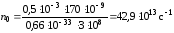
Кількість молекул Cl2, які при даній довжині хвилі вступили в реакцію за 1 секунду, дорівнює:
nP = 11,341018/330 = 34,41015 c-1
Квантовий вихід реакції за даної довжини хвилі становить:
= 34,41015/42,91013 = 0,80102
Результати розрахунку кількості квантів світла, які при певній довжині хвилі поглинаються реакційною сумішшю за 1 секунду, кількості проредагованих за 1 секунду молекул та квантового виходу упорядковуємо у таблиці.
Таблиця 2.20
Результати розрахунку квантового виходу реакції
|
, нм |
N10-18 |
nP 1015 с-1 |
n01013 , c-1 |
102 |
|
170 |
11,34 |
34,4 |
42,9 |
0,80 |
|
173 |
21,25 |
64,4 |
43,7 |
1,47 |
|
175 |
17,18 |
52,1 |
44,2 |
1,18 |
|
178 |
12,38 |
37,5 |
44,9 |
0,83 |
3. Максимальному квантовому виходу реакції утворення хлористого водню = 1,47102 відповідає довжина хвилі = 173 нм.
Розрахуємо кількість молекул Cl2, які за максимального квантового виходу вступили в реакцію взаємодії з воднем при поглинанні системою Е2 = 387 Дж світлової енергії:
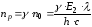
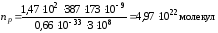
Вихід продукту реакції з врахуванням того, що при поглинанні одного кванту радіації утворюються дві молекули НСІ, становить:
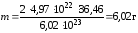

4. Кількість енергії, яку необхідно затратити за максимального квантового виходу, щоб отримати 100г продукту HCl:
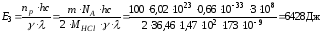
Довжину кінетичного ланцюга розраховуємо за рівнянням:

= 1/0,095 = 10,5
