
Лабораторные / Молекулярка / Лаб 2_4_мал_ОК
.pdf
|
Л А Б О Р А Т О Р Н А Я |
Р А Б О Т А |
№ 2.4 |
(состояние 4 - р0 ,Т1). Если сразу после открывания снова закрыть кран, то |
||||||||||
|
|
|
|
|
давление внутри сосуда начнет возрастать вследствие того, что |
|||||||||
|
ОПРЕДЕЛЕНИЕ ОТНОШЕНИЯ УДЕЛЬНЫХ |
охладившийся при расширении воздух в сосуде начнет снова нагреваться. |
||||||||||||
|
ТЕПЛОЕМКОСТЕЙ ГАЗОВ |
|
|
Возрастание давления прекратится, когда температура воздуха в сосуде |
||||||||||
|
|
|
|
|
сравняется с внешней температурой Т0. При этом давление станет равным р2 |
|||||||||
ЦЕЛЬ РАБОТЫ: Измерить отношение удельных теплоемкостей |
(состояние 5 - р2 ,Т0). |
|
|
|
|
|
|
|
|
|||||
воздуха cp/сv. |
|
|
|
|
|
p2 = p0 + p2 , |
p2 = g h2 . |
|||||||
Способ определения отношения cp/сv = прост. Пусть мы имеем |
При переходе из состояния 3 в 4: |
|
|
|
|
|
|
|||||||
|
|
(T0 ) |
= ( p1 ) 1, |
|
|
|
||||||||
стеклянный сосуд А, соединенный с манометром М. Посредством кранов |
|
|
|
|
(1) |
|||||||||
сосуд может соединяться с атмосферой и насосом (рис.2.4.1). |
|
|
|
T1 |
p0 |
|
|
|
|
|||||
Накачаем насосом воздух в сосуд А (процесс 1-2) (рис.2.4.2), через |
где = cp/cv. |
|
|
|
|
|
|
|
|
|
||||
некоторое время изохорически (процесс 2-3) его температура станет равной |
При переходе из состояния 4 в 5 состояние (V = const): |
|||||||||||||
температуре окружающей среды, а давление р1 = р0 + р1 (состояние 3-p1, T0) |
|
|
|
T1 |
p0 . |
|
|
|
|
|||||
отнасоса |
|
|
2 |
|
|
|
|
|
|
|
(2) |
|||
|
p |
|
|
|
|
T0 |
p2 |
|
|
|
|
|
||
|
|
|
|
Подставляя р1 = gh1 |
|
|
|
|
|
|
||||
|
|
3 |
|
|
в (1) , получим |
|
|
|
|
|
||||
|
|
|
|
|
|
p0 p1 -1 |
T0 |
|
|
|
||||
|
|
p1 |
|
|
|
( |
) |
|
, |
|||||
|
|
|
|
|
p0 |
) |
= ( |
|
|
|||||
|
|
|
|
T0 |
|
|
|
T1 |
|
|
|
|||
|
|
|
|
|
(1+ |
p1 |
-1 |
T0 T1 |
|
|||||
|
|
|
|
|
|
p0 |
) |
= (1+ |
T1 |
|
|
) . |
||
|
|
p2 |
|
5 |
|
|
|
|
|
|
|
|
||
А |
М |
p0 |
|
1 |
т.к. p1 и T0 |
T1 - величины малые, то, разлагая обе части равенства по |
||||||||
|
|
|
|
4 |
p0 |
T1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
биному Ньютона и ограничиваясь членами I порядка малости, получим: |
|||||||||
|
|
|
|
V |
|
1 + ( - 1) p1 = 1 + T0 T1 , |
||||||||
|
|
|
|
|
|
|||||||||
Рис.2.4.1 |
|
Рис. 2.4.2 |
|
|
T |
p0 |
1 |
|
|
T1 |
||||
Изменение давления р в сосуде регистрируется жидкостным |
|
|
T |
|
|
|
|
|||||||
манометром М по разности высот h |
|
|
|
откуда |
p0 |
0 |
1 |
= |
p1 . |
|
(3) |
|||
|
р = gh , |
|
|
|
|
T1 |
|
|
|
|
|
|
||
где - плотность жидкости в манометре. |
|
|
|
Подставляя р2 = р0 + р2 в (2) , получим |
p0 |
|
|
|
|
|||||
Если быстро открыть кран, то воздух в сосуде будет расширяться |
|
|
p0 p2 = |
, |
|
|
|
|||||||
адиабатически, пока давление его не станет равным р0 , при этом он |
|
|
|
|
|
|||||||||
охладится от |
температуры окружающего воздуха |
Т0 |
до температуры T1 |
|
|
|
T0 |
|
T1 |
|
|
|
|
|
4 5
2 |
1 |
3 |
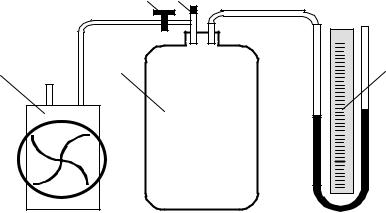
Рис. 2.4.3
отсюда |
p2 = p0 |
T0 |
T1 |
. |
(4) |
|
|
||||
|
|
|
T |
|
|
|
|
|
1 |
|
|
Подставляя (4) в (3), получим
2.Закрыть клапан 4 и выждать 3-4 минуты (температура воздуха в баллоне должна стать равной температуре окружающего воздуха, при этом давление в баллоне должно стабилизироваться).
Произвести измерения разности уровней в манометре h1 = l1 - l2 , где l1 , l2 - уровни жидкости в коленах манометра.
3.Полностью открыть клапан 5 на максимально короткое время, соединив баллон с атмосферой.
Через 3-4 минуты (давление в баллоне должно стабилизироваться)
определить l1’ и l2’и найти h2 ; h2 = l1’- l2’.
4.Повторить опыты (п.п. 1-3) не менее 5 раз.
5.Рассчитать по формуле (5).
6.Оценить погрешность .
7.Результаты измерений и расчетов занести в таблицу:
№ |
h1, |
h2, |
γi |
γ |
Примечание |
мм.вод.ст. |
мм.вод.ст. |
||||
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
|
|
… |
|
|
|
|
|
|
|
|
|
1 |
|
|
КОНТРОЛЬНЫЕ ВОПРОСЫ |
|
||
|
h2 = |
|
|
h1 , |
|
|
|
|||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
Почему в газах возникает внутреннее трение? |
|
||
тогда |
= |
|
|
h1 |
. |
(5) |
Каков физический смысл коэффициента внутреннего трения |
|||
|
|
|
|
газа? |
|
|||||
h1 h2 |
|
|||||||||
|
|
|
|
От чего зависят значения коэффициента внутреннего трения |
||||||
|
|
|
|
|
|
|
|
|
и длина свободного пробега молекул < > газа? |
|
|
ОПИСАНИЕ ЭКСПЕРИМЕНТАЛЬНОЙ УСТАНОВКИ |
|
Оцените численные значения коэффициента |
внутреннего |
||||||
|
|
трения и длины свободного пробега молекул газа |
< > по |
|||||||
|
Экспериментальная установка (рис.2.4.3) состоит из баллона 1, |
|||||||||
|
теоретическим формулам (1.3), (1.7) и сравните их с измеренными. |
|||||||||
соединенного с манометром 3 и насосом 2. С помощью клапана 4 баллон |
||||||||||
можно отсоединить от насоса, клапан 5 предназначен для соединения |
Что изменится в Ваших измерениях, если диаметр капилляра |
|||||||||
баллона с атмосферой. |
|
|
|
|
|
увеличить в 2 раза? |
|
|||
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ 1. Открыв клапан 4, накачать насосом воздух в баллон так, чтобы
разность уровней жидкости в манометре 3 стала равной 250-300 мм.
