
2013.Термодинамика / Paskal / 2011_09_27 / 2011_09_27 / IMG_0036-88-89
.docГЛАВА ТЕРМОДИНАМИКА МЯОГОКОШЮНЕНТНМУ СИСТЕМ
5l» С о с т а в многокомпонентной системы
Состав
многокомпонентной
системы.![]() -го
компонента составляют
-го
компонента составляют![]() молей соответственно. Это те количества
чистых компонентов, которые необходимо
взять для изготовления данной
многокомпонентной системы посредством
растворения или перемешивания. Общее
количество вещества в системе равно
молей соответственно. Это те количества
чистых компонентов, которые необходимо
взять для изготовления данной
многокомпонентной системы посредством
растворения или перемешивания. Общее
количество вещества в системе равно
![]() (2.1.1)
(2.1.1)
Таким
образом, химический состав системы
может быть задан К
независимыми
величинами
![]() •
Однако термодинамические свойства
системы
не зависят от общего количества вещества
в ней (если при изменении
•
Однако термодинамические свойства
системы
не зависят от общего количества вещества
в ней (если при изменении
![]() система
остается макроскопической). Отвлекаясь
от общего количества вещества в системе
(и, следовательно, от её размеров),
химический состав системы можно задать
мольными (грамм-атомными)
или молекулярными (атомными) концентрациями
система
остается макроскопической). Отвлекаясь
от общего количества вещества в системе
(и, следовательно, от её размеров),
химический состав системы можно задать
мольными (грамм-атомными)
или молекулярными (атомными) концентрациями
![]() (2.1.2)
(2.1.2)
(.![]() -
число атомов (молекул) данного компонента
-
число атомов (молекул) данного компонента
![]() -
общее число атомов (молекул) в системе;
.
-
общее число атомов (молекул) в системе;
.![]() ,где
,где![]() -
число Авгадро
-
число Авгадро![]() )
Очевидно, что
)
Очевидно, что![]()
![]() (2.1.3)
(2.1.3)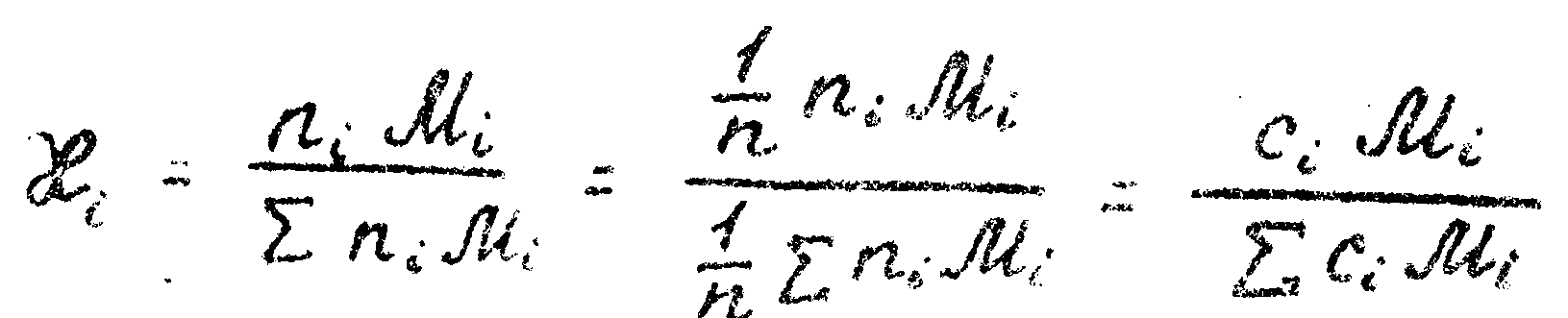
- 89 -
Из
всех![]() концентраций
независимыми являются
концентраций
независимыми являются
![]() .
К величин
.
К величин
![]() можно
заменить, таким образом,
можно
заменить, таким образом,
![]() концентрациями
концентрациями
![]() и
и
одной
величиной![]() ,и
наоборот.
,и
наоборот.
Химический
состав системы можно изменять, изменяя
![]() ,т.е.
добавляя к системе или изымая из неё
определенное количество вещества тех
или иных компонентов. Такого же изменения
химического состава (т.е. изменения
набора
,т.е.
добавляя к системе или изымая из неё
определенное количество вещества тех
или иных компонентов. Такого же изменения
химического состава (т.е. изменения
набора![]() ,
поскольку только он, а не
,
поскольку только он, а не![]() ,
определяет термодинамические свойства
системы) можно добиться, заменяя
некоторое количество вещества (некоторое
число атомов или грам-атомов, молекул
или молей) одного компонента тем же
количеством вещества другого компонента.
В последнем случае
,
определяет термодинамические свойства
системы) можно добиться, заменяя
некоторое количество вещества (некоторое
число атомов или грам-атомов, молекул
или молей) одного компонента тем же
количеством вещества другого компонента.
В последнем случае
![]() .Нередко
в
расчетах и в большей мере на практике
вводятся другие характеристики
химического состава. Так, весовые
концентрации определяются следующим
образом:
.Нередко
в
расчетах и в большей мере на практике
вводятся другие характеристики
химического состава. Так, весовые
концентрации определяются следующим
образом:
![]() (2.1.4)
(2.1.4)
Где
![]() -
вес
совокупности
атомов (молекул) данного компонента,
-
вес
совокупности
атомов (молекул) данного компонента,
![]() (2.1.5)
(2.1.5)
общий лес системы»
Легко установить связь между мольными щ веоовшн концентрациями, подставляя в(2.1.4) выражения (2.1.5) и
, (2.1.6)
где![]() –
атомный (молекулярный) вес компонента.
–
атомный (молекулярный) вес компонента.
При такой подстановке
(2.1.7)
Наоборот, подставляй в. (2.1.2) выражения (2.1.3) и (2.1.6) в виде
