
- •Методическое пособие по педиатрии
- •Часть I. Болезни детей младшего и старшего возраста
- •Глава I. Аномалии конституции
- •Глава II. Аллергические заболевания
- •Глава III. Заболевания органов дыхания
- •Таб.1. 23.Этиология внебольничных пневмоний у детей
- •Глава IV. Белково-энергетическая недостаточность
- •Глава V. Рахит, нарушение фосфорно-кальциевого обмена
- •Глава VI. Болезни почек и мочевых путей
- •Чрнс и гзнс
- •Прекратить вводить антибиотики IV поколения. Назначение антибиотиков для орального применения на 1-4 недели. Выписка.
- •Гипотрофия III степени.
- •Классификация дискинезий желчевыделительной системы
- •Глава IX. Заболевания сердечно-сосудистой системы
- •Врожденные пороки сердца бледного типа
- •Врожденные пороки сердца с препятствием к выбросу из желудочков
- •Врожденные пороки сердца с цианозом
- •Часть II. Неонатология
- •Часть II. Неонатология
- •Глава VIII. Болезни системы крови железодефицитные состояния у детей
- •Основные этапы патогенеза
- •Краткая информация о тромбоцитах, дифференцировке мегакариоцитарного ростка
- •Дифференциальный диагноз итп проводят с острым лейкозом, апластическими анемиями, наследственными тромбоцитопатиями, симптоматическими тромбоцитопеническими пурпурами.
- •Задачи лечения:нормализация уровня тромбоцитов в крови, купирование проявлений итп.
- •Спленэктомия показана при итп не поддающейся коррекции базисными препаратами, при угрожающих жизни кровотечениях, хронизации процесса, но не ранее чем через 1 год с момента дебюта заболевания.
- •Прогноз при итПдля жизни благоприятный. Летальность не превышает 2-3%.
- •Часть 2
- •Глава I. Введение в неонатологию
- •Глава II. Организация медицинского обслуживания новорожденных в родильном доме
- •Глава III. Адаптация, пограничные состояния
- •Глава IV. Задержка внутриутробного развития
- •Глава V. Гипоксия плода и асфиксия новорожденного
- •Тактика ведения новорожденных после завершения первичных реанимационных мероприятий
- •Глава VI. Родовая травма. Интранатальные повреждения нервной системы
- •Глава VII. Недоношенные дети
- •Причины рождения недоношенных детей:
- •Энтеральное питание
- •Возможные варианты питания ребенка в зависимости от гестационного возраста и наличия заболеваний:
- •2. Этап полного (сбалансированного) зондового питания
- •3. Этап отмены зондового питания
- •Глава VIII. Гемолитическая болезнь новорожденных
- •Глава IX. Инфекционные заболевания новорожденных
- •Глава IX. Неинфекционные заболевания системы дыхания
- •Глава X. Болезни кожи и пупочной ранки
- •Глава XI. Геморрагическая болезнь новорожденного
Глава IV. Белково-энергетическая недостаточность
ГИПОТРОФИЯ (Г) - хроническое расстройство питания, характеризующееся дефицитом массы по отношению к росту. В настоящее время для обозначения этого состояния все чаще употребляются термины: белково-энергетическая недостаточность, синдром недостаточности питания.
Эпидемиология Г изучена недостаточно. Частота Г зависит от экономического развития страны. В России тяжелая Г диагностируется у 2% детей. Легкие формы Г часто пропускаются.
Классификация. По времени возникновения различают пренатальную (внутриутробную, врождённую) и постнатальную (приобретенную) Г.
По степени тяжести выделяют Г первой, второй и третьей степени. При Г I степени дефицит фактической массы по отношению к долженствующей с учётом роста ребенка составляет 10-20%, при Г II степени - 20-30%, при Г III степени - больше 30%.
Период заболевания: начальный, прогрессирования, реконвалесценции.
Первичные Г имеют в своей основе белково-энергетическая недостаточность. Вторичные Г сопровождают врожденные и приобретенные заболевания.
Гипостатура – вариант дистрофии с равномерным отставанием массы тела и роста от возрастных норм.
Основными клинико-патогенетическими вариантами Г являются: алиментарный маразм, квашиоркор, маразм-квашиоркор.
Этиология. К развитию Г могут привести различные экзогенные и эндогенные факторы, которые, как правило, сочетано, обуславливают либо недостаточное поступление пищи в организм, либо недостаточное её усвоение. Этиологические факторы зависят от времени возникновения и соответственно формы Г: пренатальной или постнатальной.
Причины развития пренатальной Г, условно, можно разделить на три группы:
1. Преплацентарные: конституциональные особенности матери (инфантилизм, астеническое телосложение, возраст моложе 18 лет или старше 35 лет); сердечно-сосудистые, почечные, эндокринные и другие заболевания матери; токсикозы беременности; предшествующие медицинские аборты; недостаточное питание матери во время беременности; неблагоприятные социально-экономические, производственные или экологические условия, вредные привычки матери (курение, алкоголизм, наркомания); аномалии васкуляризации матки.
2. Плацентарные: тромбозы, гематомы, инфаркты плаценты, её гипоплазия, кальциноз, фиброз, плацентит.
3. Постплацентарные: аномалии пуповины, многоплодная беременность, врождённые пороки развития плода, внутриутробная инфекция, наследственные факторы (хромосомные заболевания, моногенные синдромы, семейная аутосомно-доминантная предрасположенность к гипотрофии).
Многие этиологические факторы (преплацентарные и плацентарные) реализуются через хроническую плацентарную недостаточность, которая приводит к развитию хронической гипоксии плода и задержке физического развития.
Среди экзогенных факторов, вызывающих развитие постнатальной Г, существенное значение имеют алиментарные факторы - количественный недокорм.
Не менее важную роль в возникновении Г играют и качественные нарушения питания (качественный «недокорм»): дефицит витаминов и микроэлементов, недостаток или избыток какого-либо пищевого вещества (белка, жира или углеводов). При повышенной белковой нагрузке снижается утилизация белка, в организме накапливаются азотистые продукты, аминокислоты, аммиак, возникает ацидоз, что ведёт к появлению дистрофических изменений в мозговой ткани и паренхиматозных органах.
Особенно неблагоприятен избыток белка на фоне недостатка углеводов. Последнее наблюдается при длительном кормлении молочными смесями и известно как «молочное расстройство питания». Злоупотребление кашами может стать причиной так называемого «мучного расстройства питания», которое проявляется либо в виде паратрофии (пастозная форма), либо Г (атрофическая и гипертонически-спастическая формы). Иногда Г является следствием длительного водного голодания.
К развитию Г часто ведут острые и хронические инфекционные заболевания (вирусные инфекции, сепсис, кишечные инфекции, отоантрит, и т.д.); существенное значение имеет дисбиоз кишечника. Вредное влияние на питание ребёнка оказывают нарушение режима и дефекты ухода.
Причинами развития наиболее тяжелых форм пренатальной Г в настоящее время чаще являются эндогенные факторы: синдром мальабсорбции, пороки развития желудочно-кишечного тракта и других органов, наследственные нарушения обмена веществ (галактоземия, фруктоземия, некоторые аминоацидопатии и т.д.), иммунодефицитные состояния, эндокринные заболевания (адреногенитальный синдром), патология центральной нервной системы.
Патогенез
Основой патогенеза Г является хроническая стрессовая реакция (Е. В. Неудахин, 1992).
У детей с пренатальной Г повышено образование стресс-реализующих гормонов: адреналина, СТГ, глюкокортикоидов. Однако при тяжёлой степени Г появляются признаки истощения коры надпочечников. Продукция инсулина и минералокортикоидов снижена. Увеличение синтеза глюкокортикоидов и снижение минералокортикоидов и инсулина характерно для хронической стрессовой реакции. При этом быстро расходуются углеводы, а для энергетического обеспечения механизмов долговременной адаптации более активно используются липиды. По данным исследований В.Ф. Дёмина у новорожденных с пренатальной Г отмечается продолжительная гиперлипидемия за счёт нейтрального жира, эфиров холестерина и фосфолипидов. Эфиры холестерина необходимы для продукции ряда биологически активных веществ, в том числе – глюкокортикоидов; фосфолипиды - для образования клеточных мембран и сурфактанта.
Характер эндокринных и метаболических изменений, типичных для хронической стрессовой реакции, делает обоснованным понятие «стрессовый плод» по отношению к плоду с пренатальной Г. Хроническая стрессовая реакция у плода и новорожденного с пренатальной Г обуславливает гиповолемию, централизацию кровообращения и гипердинамическую реакцию миокарда, гипогликемию, уменьшение содержания гликогена в печени и сердце, гипокальциемию и гипомагниемию, метаболический ацидоз, накопление продуктов перекисного окисления липидов, полицитемию и повышение уровня гематокрита, гиперкоагуляционный синдром (у этих детей более высокий риск развития ДВС-синдрома), нарушение микрогемоциркуляции, возникновение иммунодепрессии.
Хронический стресс уменьшает опасность развития у новорожденных с пренатальной Г I и II степени синдрома дыхательных расстройств вследствие усиленного образования сурфактанта, но повышает риск возникновения кровоизлияний в мозг и лёгкие, а также некротического энтероколита.
У детей раннего возраста с постнатальной (приобретённой) и смешанной (пренатально-постнатальной) Г также определяются изменения, характерные для хронической стрессовой реакции. Результаты исследования вегетативного гомеостаза свидетельствуют о стадийности и зависимости выраженности изменений от степени Г: при I и II степенях отмечается нарастающая симпатикотония и усиливающаяся активность центрального контура регуляции, при III степени – «срыв адаптации», децентрализация регуляции с переходом на автономные уровни и преобладание парасимпатических влияний. Для детей с Г I и II степеней характерна дисфункция коры надпочечников с повышенной продукцией глюкокортикоидных фракций и пониженной - проминералокортикоидных (маркёр хронической стрессовой реакции). У детей с Г III степени наблюдается гипофункция (истощение) коры надпочечников.
О состоянии хронического стресса свидетельствует и переход обмена веществ с преимущественно углеводного на преимущественно липидный, в результате чего используется нейтральный жир подкожно-жировой клетчатки для энергетического обеспечения функций организма и образования фосфолипидов, необходимых клеточным мембранам. Для сердечно-сосудистой системы у детей раннего возраста с Г характерна склонность к централизации кровообращения на фоне гиповолемии, гипердинамическая реакция миокарда, лёгочная гипертензия, спастическое состояние прекапиллярных артериол, нарушение микрогемоциркуляции с развитием «сладж»-синдрома в микрососудах. Гемодинамические расстройства патогенетически связаны с хронической стрессовой реакцией. Стрессовым влиянием можно объяснить и развитие гиперкоагуляции и иммунодепрессии.
Т.О., Г - это проявление патофизиологической (хронической стрессовой) реакции организма, в связи с чем она должна рассматриваться как клиническим синдромом, а не как нозологическая единица.
Анамнез, клиника
Основными клиническими синдромами при Г являются: недостаточная упитанность, трофические расстройства, снижение пищевой толерантности, изменение функционального состояния ЦНС, нарушение иммунологической реактивности.
Г I степени проявляется умеренным похуданием ребёнка (дефицит массы тела 10-20%), что выражается в истончении подкожного жирового слоя, прежде всего на туловище. У детей отмечается бледность кожных покровов и слизистых оболочек, снижение тургора тканей и мышечного тонуса. Рост не нарушается. Аппетит и стул обычно остаются нормальными. Функции внутренних органов и психомоторное развитие не изменяются.
При Г II степени заметно ухудшается состояние ребёнка. Кожные покровы приобретают сероватый оттенок, становятся сухими. Из-за низкой эластичности кожа легко собирается в складки, особенно на внутренней поверхности бёдер. Тургор тканей и тонус мышц снижены. Подкожный жировой слой отсутствует на туловище и конечностях. Дефицит массы (20-30%) сопровождается отставанием в росте на 1-3 см. У детей плохой аппетит, снижена толерантность к пище. Они раздражительны или беспокойны. Обращают на себя внимание задержка в психомоторном развитии. У больных легко возникают инфекционно-воспалительные очаги в ушах, зеве, легких. Часто наблюдается анемия. Характер стула зависит от особенностей питания.

Рис. 1.16. Схема патогенеза гипотрофии
Белковый стул (при перекорме молоком, творогом) обычно скудный, сухой, плотный, крошковатый с гнилостным запахом и щелочной реакцией, состоит в основном из известковых и магнезиевых солей.
Мучнистый стул обычно жидкий с кислой реакцией, с примесью зелени и слизи. При копрологическом исследовании определяется много внеклеточного крахмала, перевариваемой клетчатки, нейтрального жира и жирных кислот, слизи и лейкоцитов.
Голодный стул скудный, сухой, иногда крошковидный, обесцвеченный с гнилостным, зловонным запахом. В копрограмме много слизи, лейкоцитов, внеклеточного крахмала, нейтрального жира и жирных кислот. Часто развивается дисбиоз кишечника.
При Г III степени состояние ребёнка тяжёлое. Подкожный жировой слой отсутствует везде, даже на лице (дефицит массы тела более 30%). Лицо треугольной формы («лицо Вольтера»). Кожа с серовато-цианотичным оттенком, сухая, иногда с трещинами. Эластичность кожи и тургор тканей резко снижены. Может появиться пастозность тканей. Дефицит роста достигает 4-6 см. У многих детей имеются признаки стоматита, молочницы. Функции внутренних органов (лёгких, сердца, печени, почек) значительно нарушены. Аппетит отсутствует, отмечается выраженная жажда. Терморегуляция расстроена. У больных часто возникают гнойно-воспалительные очаги, могут развиваться септические состояния. Стул «голодный». Значительно угнетены функции центральной нервной системы.
При пренатальной Г отмечается дефицит массы тела по отношению к длине и массе соответственно сроку гестации.
Гипостатура в последние годы стала встречаться значительно чаще. Эта форма Г развивается у детей с врожденными и наследственными заболеваниями, а так же в тех случаях, когда повреждающие факторы оказывали длительное воздействие на организм ребенка. Возможно формирование гипостатуры с момента рождения.
Заболевание проявляется бледностью и сухость кожных покровов, снижением тургора тканей. Главной отличительной особенностью гипостатуры является пропорциональное отставание массы тела и роста по отношению к возрасту. Трофические нарушения кожи и подкожно-жировой клетчатки выражены значительно слабее, чем у детей с Г при аналогичном дефиците массы тела.
Как и при Г при гипостатуре имеет место проявления поражения ЦНС, признаки нарушения обмена веществ, метаболический ацидоз, снижение защитных реакций организма. При гипостатуре организму ребенка в большей степени, чем при Г удается приспособиться к существованию в новых условиях. В тоже время обменные нарушения, патология со стороны нервной системы имеют более стойкий характер, что проявляется плохими результатами лечения.
Квашиоркор – вариант Г, возникающий после отлучения ребенка от груди и переводе на растительную пищу, в результате чего развивается белковое голодание. Квашиоркор встречается на 2-4 году жизни.



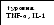








Рис. 1.17. Схема патогенеза квашиоркора (Педиатрия, национальное руководство, 2009)
Основными особенностями квашиоркора являются: атрофия мышц с сохранением подкожно-жирового слоя, депигментация и посеребрение волос, выпадение волос, генерализованные отеки (лунообразное лицо), увеличенный в размерах живот, гепатоспленомегалия. Характерны выраженная задержка физического и психического развития, проявления рахита. При лабораторном исследовании выявляют тяжелую анемию, гипопротеинемию.
Диагноз Г у детей базируется на данных клиники, оценке показателей дефицита массы тела с учётом роста. Дефицит массы определяется по формуле:
Д = (ДМ – ФМ)/ДМ × 100, где Д - дефицит массы тела в %; ДМ - долженствующая масса с учётом роста; ФМ - фактическая масса.
Для оценки степени Г можно пользоваться таблицами центильных распределений массы по длине тела. При диагностике пренатальной Г используются данные клиники, оценочные таблицы Г. М. Дементьевой, В. Н. Ильина. На практике пренатальная Г у доношенных новорожденных часто диагностируется по массо-ростовому показателю, который в норме должен быть в пределах от 60 до 80; при Г I степени - 59-55; при II степени - 54-50; при III степени - меньше 50. Помимо выявления Г, определения степени её тяжести, при осмотре ребёнка в большинстве случаев приходится решать вопрос: синдромом какого заболевания является Г у данного ребёнка? От этого зависит организация лечения.
Лабораторные критерии Г
Полицитемия, гиперкоагуляционный синдром, компенсированный (при Г I-II ст.) и декомпенсированный при Г III ст.
Гипогликемия, гипокальциемия и гипомагниемия, гипокалиемия, склонность к гипернатриемии.
Дислипидемия (гиперлипидемия за счет триглицеридов, фосфолипидов и эфиров холестерина при гипотрофии I-II ст. и за счет триглицеридов и НЭЖК при гипотрофии III ст.).
Повышение в моче уровней глюкокортикоидных гормонов и снижение минералокортикоидных при Г I-II ст.; снижение глюкокортикоидов и минералокортикоидов при Г III ст.
Гиперкатехоламинемия, гипоинсулинемия.
Угнетение иммунитета: уменьшение Т-лимфоцитов, повышение фагоцитарной активности нейтрофилов при I-II ст. Г и снижение – при III ст.
Изменения копрограммы: при молочном расстройстве питания: щелочная реакция кала, повышение уровня кальция и магния.
При мучном расстройстве: кислая рН кала, повышение уровня внеклеточного крахмала, перевариваемой клетчатки, жирных кислот, слизи и лейкоцитов; признаки дисбиоза кишечника.
ЭКГ: метаболические нарушения в миокарде желудочков.
КИГ: признаки симпатикотонии при Г I-II ст. и ваготонии – при Г III ст.
ЭХО КГ: компенсаторное увеличение сократительной способности миокарда при Г I-II ст. снижение сократительной способности миокарда при Г III ст.
В качестве скрининга Г используют показатели белкового обмена: протеинограмму (снижение белка и альбумина), уровень мочевины в крови (снижение), абсолютное количество лимфоцитов в периферической крови (снижение).
Дифференциальный диагноз Г проводят с гипостатурой, квашиоркором, нанизмом, конституциональной низкорослостью.
Табл. 1.36. Дифференциальный диагноз гипотрофии
|
Признак |
Гипотрофия |
Гипостатура |
Квашиоркор |
Нанизм |
|
Дефицит массы тела |
есть |
есть |
есть |
есть |
|
Дефицит длины тела |
При Г 2-3 ст. |
Выражен |
есть |
есть |
|
Подкожно-жировой слой |
истончен |
Истончен в меньшей степени, чем дефицит массы |
нет |
нет |
|
Тургор тканей |
Изменен согласно степени Г |
Изменен в меньшей степени, чем дефицит массы |
Часто сохранен |
Не изменен |
|
Трофика тканей |
Нарушена в зависимости от степени Г |
Выражена меньше, чем степень дефицита массы тела |
Нарушена |
Не нарушена |
|
Мышечный тонус |
Снижен с соответствии со степенью Г |
Снижен меньше, чем дефицит массы |
Атрофия мышц |
Нет |
|
Психомоторное развитие (п/мр) |
Нарушено в зависимости от степени Г |
Изменено в меньшей степени, чем дефицит массы |
Отставание в п/мр. развитии |
Нет |
|
Гепатомегалия |
При Г 3-й ст. |
редко |
Часто |
нет |
|
Отеки |
Редко |
Редко |
Характерно |
Нет |
|
Поражение внутренних органов |
В зависимости от степени Г |
Изменены в меньшей степени, чем дефицит массы |
Встречаются |
нет |
|
Отслойка эпидермиса, депигментация волос |
Не характерно |
Не характерно |
характерно |
Нет |
Лечение, задачи лечения: восстановление дефицита массы тела, купирование клинических и параклинических проявлений Г, предупреждение развития осложнений.
Схема лечения. Обязательное лечение: диета, уход, режим, коррекция водно-электролитных нарушений, витаминотерапия, стимулирующее лечение, ферментотерапия.
Вспомогательное лечение: частичное парентеральное питание, биопрепараты, β-адреноблокаторы, анаболические гормоны, санация очагов хронической инфекции, борьба с гиподинамией.
Показания для госпитализации: При Г I степени лечение обычно проводится в амбулаторных условиях, а при Г II и III степени - в стационаре.
В первую очередь осуществляются мероприятия по установлению причин, приведших к развитию Г (инфекционные, хронические заболевания ЖКТ, наследственные и врожденные энзимопатии, эндокринные заболевания, органические заболевания ЦНС). Большое внимание должно уделяться организации правильного режима дня, уходу за ребёнком. Для детей с Г наиболее оптимальной является температура воздуха 24-25 °C при относительной влажности 60-70%.
Согласно рекомендациям ВОЗ (2003) выделяется 10 шагов по выхаживанию детей с Г:
предупреждение/лечение гипогликемии;
предупреждение/лечение гипотермии;
предупреждение/лечение дегидратации;
коррекция электролитного баланса;
предупреждение/лечение инфекции;
коррекция дефицита микронутриентов;
осторожное начало кормления;
обеспечение прибавки массы тела и роста;
обеспечение сенсорной стимуляции и эмоциональной поддержки;
дальнейшая реабилитация.
Табл.1.37. Этапы выхаживания детей с белково-энергетической недостаточностью
|
Шаги |
Ф А З А | ||
|
стабилизация |
реабилитация | ||
|
1-2 день |
3-7 день |
2-6 неделя | |
|
1. гипогликемия |
ХХХХХХ |
|
|
|
2. гипотермия |
ХХХХХХ |
|
|
|
3. дегидратация |
ХХХХХХ |
|
|
|
4. электролиты |
ХХХХХХ |
ХХХХХХ |
ХХХХХХХХ |
|
5. инфекция |
ХХХХХХ |
|
|
|
6. микронутриенты |
Без железа |
С железом | |
|
7. осторожное питание |
ХХХХХХ |
ХХХХХХ |
|
|
8. прибавка массы |
|
|
ХХХХХХХХ |
|
9. сенсорный стимул |
ХХХХХХ |
ХХХХХХ |
ХХХХХХХХ |
|
10. реабилитация |
|
|
ХХХХХХХХ |
Первый шаг. При сохраненном сознании и уровне глюкозы в крови менее 3 ммоль/л ребенку вводят 50 мл 10% раствора глюкозы через зонд и орально. Кормление начинают с 25% от обычного разового объема питания каждые 30 минут на протяжении 2-х часов. При наличии нарушения сознания (или гипогликемические судороги) внутривенно водят 10% раствор глюкоза из расчета 5 мл/кг. Всем детям с гипогликемией назначают антибиотики широкого спектра действия.
Второй шаг. Согревание ребенка начинают при ректальной температуре ниже 35,5 0С (лучистое тепло, теплая одежда).
Третий шаг. При наличии выраженных проявлений эксикоза начинают оральную регидратацию раствором ReSoMal (с пониженным содержание натрия) из расчета 5 мл/кг каждые 30 минут в течение 2 часов. В последующие 4-10 часов раствор вводят по 5-10 мл/кг/час, постепенно заменяя его на грудное молоко или молочную смесь. Кормление проводят каждые 2 часа без ночного перерыва.
Общее количество вводимой ребенку жидкости составляет 130 мл/кг/сутки, а при выраженных отеках – 100 мл/кг/сутки.
Количество жидкости, необходимой для внутривенного введения, будет равно: СЖП + жидкость возмещения обезвоживания минус (количество съеденной пищи + объем выпитой жидкости).
Основная часть жидкости вводится внутривенно в виде 10% раствора глюкозы.
Четвертый шаг. Коррекция гипокалиемии проводится из расчета 3-4 ммоль/кг/сутки; магния – 0,4-0,6 ммоль/кг/сутки. При возможности для коррекции электролитов следует использовать специальный электролитно-минеральный раствор.
Пятый шаг. Своевременное предупреждение и лечение инфекции, которое проводится по общим принципам.
Шестой шаг. Коррекция дефицита железа начинается не ранее 2-й недели лечения в дозе 3 мг/кг/сутки. Доза цинка – 2 мг/кг/сутки; меди – 0,3 мг/кг/сутки; фолиевой кислоты – 5 мг (в первый день), затем – 1 мг/сутки. В последующем переходят на витамино-минеральные комплексы. Возможно отдельное назначение витаминных препаратов: С, У, кальция пантотената, пиридоксина, ретинола.
Седьмой и восьмой шаги. Парентеральное питание на первом этапе лечения представлено препаратами аминокислот (Аминон, Альвезин), и концентрированными растворами глюкозы. Жировые эмульсии (Интралипид, Липофундин) начинают применять с 5-7 дня лечения в дозе 10-15 мл/кг/сут. При тяжелых формах гипотрофии энтеральное питание начинают с кормления через зонд со скоростью поступления смеси не более 3 мл/мин (калорийная нагрузка не более 1 ккал/мл). Вначале следует использовать смеси на основе полного гидролиза белка (Алфаре, Нутрамиген, Прогестермил). Смеси (при тяжелой Г) должны содержать небольшое количество лактозы. Длительность периода зондового питания в зависимости от пищевой толерантности продолжается от нескольких дней до нескольких недель. Зондовое кормление постепенно отменяют и оставляют его только на ночное время. При достижении объема дневного кормления в 50-70% постоянное зондовое кормление отменяют.
При Г I и II степени диетотерапия проводится с выделением:
а) адаптационного периода (определение толерантности к пище);
б) репарационного периода (промежуточный, этап коррекции);
в) периода усиленного питания;
г) переход на рациональное питание.
Диета является основой рационального лечения Г у детей раннего возраста. При её осуществлении необходимо соблюдать следующие принципы:
1. Использование на начальных этапах лишь легко усвояемой пищи (женское молоко, адаптированные смеси);
2. Систематический контроль питания с расчётом объёма пищи и пищевой нагрузки по белкам, жирам, углеводам и калориям.
этап диетотерапии: определение толерантности ребенка к пище (адаптационный период, этап разгрузки, этап минимального питания).
Задачи этапа диетотерапии:
- определение толерантности ребенка к пище;
- выведение из организма токсинов и недоокисленных продуктов обмена.
Суточный объем питания в первый день диетотерапии уменьшается от 20 до 80% в зависимости от степени Г (чем больше степень Г, тем с меньшего объема пищи начинается кормление на данном этапе).
При III степени Г продолжительность адаптационного периода может колебаться от 10 до 14 дней. Если разовая доза становится больше 50 мл, переходят на 8-разовое кормление (см. «первый» и «третий» шаги). Адаптационный период заканчивается увеличением суточного объёма пищи до необходимого количества (1/5 массы).
В качестве основной смеси используют или грудное молоко (донорское молоко) или адаптированную смесь. Все виды прикормов и иных пищевых добавок на этом этапе кормления отменяют.
Количество кормлений увеличивают (см. «первый» и «третий» шаги) в зависимости от степени Г и аппетита.
Продолжительность этапа определения толерантности ребенка к пище составляет 3-5-7-10 дней (в зависимости от степени Г). Чем выше степень Г - тем длительнее этот этап кормления.
На протяжении данного этапа постепенно (за 3-5-7-10 дней) увеличивается количество вводимой пищи, и к окончанию этапа доводят его до полного объема (рассчитанного тем или иным методом).
Недостающая часть питания возмещается глюкозо-солевыми растворами. В связи с тем, что ежедневное количество молока (смеси) увеличивается, количество вводимой жидкости постепенно уменьшается.
К моменту окончания этапа минимального питания ребенок должен получить полный необходимый объем пищи и прекратить получать внутривенные вливания и потребление жидкости через рот.
Полный объем пищи дается ребенку еще в течение 2-3 дней, после чего переходят ко этапу лечебного питания.
этап диетотерапии - промежуточный этап (этап коррекции дефицита основных пищевых ингредиентов).
П и т а н и
е
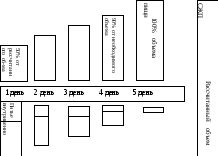
Ж и д к о с т ь
Рис.1. 18. Схема питания и восполнения объема жидкости при гипотрофии 2-й степени на Ι этапе диетотерапии (пример)
Задачи этапа: восполнение дефицита в питании у больного недостающих пищевых ингредиентов.
Методика проведения 2-го этапа. Для определения дефицита пищевых ингредиентов необходимо провести расчет питания.
Принципы расчета питания.
На 1-й неделе переходного периода количество белков и углеводов рассчитывается на фактическую массу +5% от нее, а жиры – на фактическую массу тела.
На 2-й неделе белки и углеводы рассчитываются на фактическую массу +10% от нее, а жиры – на фактическую массы тела.
На 3-й неделе белки и углеводы рассчитываются на фактическую массу тела +15% от нее, а жиры – на фактическую массу тела.
На 4-й неделе белки и углеводы рассчитываются на приблизительно долженствующую массы тела (фактическая + 20% от нее), а жиры на фактическую массы тела.
Недостающее количество белка, жира, углеводов вводится постепенно (в течение 5-7 дней - для каждого ингредиента) в следующей последовательности: белки углеводы жиры.
Дефицит белка компенсируется: смесями с повышенным содержанием белка, творогом, белковыми модулями; дефицит жиров: жировыми модульными эмульсиями, сливками, растительным или сливочным маслом; углеводов – сахарным сиропом, кашами. Все пищевые добавки применяют в соответствии с возрастом.
После ликвидации дефицита всех ингредиентов, ребенку можно ввести положенные по возрасту (отмененные ранее) прикормы.
В периоде усиленного питания содержание белков и углеводов постепенно увеличивается и их начинают рассчитывать на долженствующую массу тела, а жиры на среднюю между фактической и долженствующей. При Г II ст. диета омолаживается (на 2-3 месяца).
Для расчета питания необходимо воспользоваться следующей таблицей:
Табл. 1.38. Расчет питания
|
Показатель |
Белки |
Жиры |
Углеводы |
Калории |
|
Должен получать на 1 кг массы тела |
|
|
|
|
|
Должен получать всего |
|
|
|
|
|
Получает всего |
|
|
|
|
|
Дефицит |
|
|
|
|
Для заполнения первой строки таблицы необходимо воспользоваться данные таблицы потребности в пищевых ингредиентах детей при Г (табл. 1.39).
Для заполнения строки 3 необходимо высчитать количество белка, жира, углеводов, содержащихся в получаемом ребенке суточном объеме смеси.
«Дефицит» - разность данных строки 2 и 3.
Табл. 1.39. Схема диетотерапии больного с гипотрофией (Баранов А.А. с соавт, 1997)
|
Задачи этапов диеты |
Разгрузка и минимальное питание |
диетотерапии - промежуточный этап |
Усиленное питание | ||
|
Коррекция белка |
Коррекция углеводов |
Коррекция жиров | |||
|
Длительность этапа в днях |
3-5-7-10 (в зависимости от степени Г) |
5-7 |
5-7 |
5-7 (всего 15-20 дней) |
До выведения из Г |
|
Количество пищи от суточного объема (1) |
1/3-1/2-2/3-3/4-1 (в зависимости от степени Г) |
1 |
1 |
1 |
1 |
|
Потребность в белках (г/кг) |
0,7-1,5-2,0 (в зависимости от степени Г) |
4,0 |
4,0 |
4,0-4,5 |
4,0-4,5 |
|
Потребность в жирах (г/кг) |
2,0-3,0-4,0 (в зависимости от степени Г) |
4,0-4,5 |
5,0-6,0 |
5,0-6,0 |
6,0-6,5 |
|
Потребность в углеводах (г/кг) |
8,0-10,0-11,0 (в зависимости от степени Г) |
11,0-12,0 |
12,0-13,0 |
13,0-14,0 |
15,0-16,0 |
|
Калорийность (ккал/кг) |
60-80-100 |
100-110 |
110-120 |
120-130 |
130-140 |
этап диетотерапии – этап усиленного питания продолжается до выведения ребенка из состояния Г. На выведение ребенка из Г уходит несколько недель.
Каждую неделю необходимо проводить коррекцию диеты, которая приближается к норме за счёт постепенного расширения ассортимента продуктов, увеличения суточного объёма, уменьшения числа кормлений.
Девятый шаг – сенсорная стимуляция и эмоциональная поддержка. Дети с Г нуждаются в хорошем уходе, ласковом обращении, массаже, ЛФК, регулярном купании, прогулках на свежем воздухе.
Десятый шаг - дальнейшая длительная реабилитация - предусматривает возвращение к рациональному питанию, согласно возрасту и утвержденных рекомендаций. В этом периоде необходимо продолжить сенсорную и эмоциональную поддержку, адекватную иммунопрофилактику, витаминную и минеральную коррекцию, по показаниям проводить стимулирующую терапию.
Большое внимание уделяется ферментотерапии. Используется Креон, абомин, панкреатин, фестал, панзинорм, мексаза и другие ферменты. Назначаются препараты, обладающие анаболическим эффектом: рибоксин, оротат калия, L-карнитин, перитол, анаболические гормоны (последние, под контролем костного возраста), апилак в свечах, инсулин с глюкозой. Среди лекарственных негормональных средств с анаболическим эффектом особое место занимают препараты, содержащиеL-карнитин. Препарат применяется за 30 минут до еды детям до 1 года по 0,03-0,075 г 3 раза в сутки, от 1 года до 6 лет – по 0,1 г 2-3 раза в сутки. Продолжительность курса – 1 месяц.
При сопутствующем дисбиозе кишечника применяются биопрепараты: Биовестин, Ацилакт, Аципол, Бактиспорин, Бактисубтил, Биобактон, Биоспорин, Биофруктолакт, Бифацид, Бифидумбактерин сухой, Бифидумбактерин-форте, Бификол, Бифилин, Бифиформ, Дюфалак, Колибактерин, Линекс, Лактофильтрум, Примадофилюс, Нутрилин-В, Флонивин БС.
В комплексном лечении этих детей используются витамины (особенно токоферол, фолиевая кислота, один из препаратов витамина В12 - кобамамид);
витамино-минеральные комплексы: Алвитал, Алфавит, Биовиталь гель, Веторон Вибовит, Бэби Мультитабс, Бэби Мультитабс Малыш, Пангексавит, Пиковит, Центрум детский + Са, Центрум детский- экстраватамин С, Юникап Ю.
Осложнения. Задержка физического и нервно-психического развития ребенка. Инфекционные осложнения (пневмонии, бронхиты, ОРИ, кишечные инфекции, отиты и др.), баллонная и жировая дистрофия печения, развитие мальдигистии и мальабсорбции, гиповолемический шок, сердечно-сосудистая недостаточность, синдром внезапной смерти.
Профилактика Г у детей должна начинаться с укрепления здоровья женщины до беременности и во время беременности. При развитии Г у плода проводится её лечение с использованием сигетина, β-симпатомиметиков, эстрогенов, диатермии, сосудорасширяющих препаратов, улучшающих маточно-плацентарное кровообращение, а также мембраностабилизирующих средств. В профилактике постнатальной Г большое значение имеет рациональное естественное вскармливание, организация правильного режима и ухода за ребёнком, предупреждение и своевременное лечение заболеваний, осложняющихся развитием Г. Г – социальная болезнь, и, следовательно, для ее профилактики важны повышение уровня жизни населения и доступность медицинской помощи для всех слоев населения.
Вопросы к экзамену.
Хронические
расстройства питания. Классификация.
Этиология. Патогенез. Клиническая
картина. Диагностика. Дифференциальный
диагноз. Осложнения. Лечение. Диетотерапия.
Использование специальных лечебных
продуктов питания. Профилактика.
