
- •2. Гетеротрофные и аутотрофные организмы: различия по питанию и источникам энергии. Катаболизм и анаболизм.
- •3. Многомолекулярные системы (метаболические цепи, мембранные процессы, системы синтеза биополимеров, молекулярные регуляторные системы) как основные объекты биохимического исследования.
- •4. Уровни структурной организации живого. Биохимия как молекулярный уровень изучения явлений жизни. Биохимия и медицина (медицинская биохимия).
- •5. Основные разделы и направления в биохимии: биоорганическая химия, динамическая и функциональная биохимия, молекулярная биология.
- •6. История изучения белков. Представление о белках как важнейшем классе органических веществ и структурно-функциональном компоненте организма человека.
- •7. Аминокислоты, входящие в состав белков, их строение и свойства. Пептидная связь. Первичная структура белков.
- •8. Зависимость биологических свойств белков от первичной структуры. Видовая специфичность первичной структуры белков (инсулины разных животных).
- •9. Конформация пептидных цепей в белках (вторичная и третичная структуры). Слабые внутримолекулярные взаимодействия в пептидной цепи; дисульфидные связи.
- •11. Доменная структура и её роль в функционировании белков. Яды и лекарства как ингибиторы белков.
- •12.Четвертичная структура белков. Особенности строения и функционирования олигомерных белков на примере гемсодержащего белка - гемоглобина.
- •13.Лабильность пространственной структуры белков и их денатурация. Факторы, вызывающие денатурацию.
- •14.Шапероны - класс белков, защищающий другие белки от денатурации в условиях клетки и облегчающий формирование их нативной конформации.
- •15.Многообразие белков. Глобулярные и фибриллярные белки, простые и сложные. Классификация белков по их биологическим функциям и по семействам: (сериновые протеазы, иммуноглобулины).
- •17.Физико-химические свойства белков. Молекулярный вес, размеры и форма, растворимость, ионизация, гидратация
- •18.Методы выделения индивидуальных белков: осаждение солями и органическими растворителями, гель-фильтрация, электрофорез, ионообменная и аффинная хроматография.
- •19.Методы количественного измерения белков. Индивидуальные особенности белкового состава органов. Изменения белкового состава органов при онтогенезе и болезнях.
- •21 .Классификация и номенклатура ферментов. Изоферменты. Единицы измерения активности и количества ферментов.
- •22.Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов (на примере витаминов в6, рр, в2).
- •23.Ингибиторы ферментов. Обратимое и необратимое ингибирование. Конкурентное ингибирование. Лекарственные препараты как ингибиторы ферментов.
- •25.Регуляция активности ферментов путем фосфорилирования и дефосфорилирования. Участие ферментов в проведении гормонального сигнала.
- •26.Различия ферментного состава органов и тканей. Органоспецифические ферменты. Изменение ферментов в процессе развития.
- •27.Изменение активности ферментов при болезнях. Наследственные энзимопатии. Происхождение ферментов крови и значение их определения при болезнях.
- •29.Обмен веществ: питание, метаболизм и выделение продуктов метаболизма. Органические и минеральные компоненты пищи. Основные и минорные компоненты.
- •30.Основные пищевые вещества: углеводы, жиры, белки, суточная потребность, переваривание; частичная взаимозаменяемость при питании.
- •31 .Незаменимые компоненты основных пищевых веществ. Незаменимые аминокислоты; пищевая ценность различных пищевых белков. Линолевая кислота - незаменимая жирная кислота.
- •32.История открытия и изучения витаминов. Классификация витаминов. Функции витаминов.
- •34.Минеральные вещества пищи. Региональные патологии, связанные с недостаточностью микроэлементов в пище и воде.
- •35.Понятие о метаболизме и метаболических путях. Ферменты и метаболизм. Понятие о регуляции метаболизма. Основные конечные продукты метаболизма у человека
- •36.Исследования на целых организмах, органах, срезах тканей, гомогенатах, субклеточных структурах и на молекулярном уровне
- •37.Эндэргонические и экзэргонические реакции в живой клетке. Макроэргические соединения. Примеры.
- •39.Окислительное фосфорилирование, коэффициент р/о. Строение митохондрий и структурная организация дыхательной цепи. Трансмембранный электрохимический потенциал.
- •40.Регуляция цепи переноса электронов (дыхательный контроль). Разобщение тканевого дыхания и окислительного фосфорилирования. Терморегуляторная функция тканевого дыхания
- •42.Образование токсических форм кислорода, механизм их повреждающего действия на клетки. Механизмы устранения токсичных форм кислорода.
- •43.Катаболизм основных пищевых веществ - углеводов, жиров, белков. Понятие о специфических путях катаболизма и общих путях катаболизма.
- •44.Окислительное декарбоксилирование пировиноградной кислоты. Последовательность реакций. Строение пируватдекарбоксилазного комплекса.
- •45.Цикл лимонной кислоты: последовательность реакций и характеристика ферментов. Связь между общими путями катаболизма и цепью переноса электронов и протонов.
- •46.Механизмы регуляции цитратного цикла. Анаболические функции цикла лимонной кислоты. Реакции, пополняющие цитратный цикл
- •47.Основные углеводы животных, их содержание в тканях, биологическая роль. Основные углеводы пищи. Переваривание углеводов
- •48.Глюкоза как важнейший метаболит углеводного обмена. Общая схема источников и путей расходования глюкозы в организме
- •49. Аэробный распад — основной путь катаболизма глюкозы у человека и других аэробных организмов. Последовательность реакций до образования пирувата (аэробный гликолиз).
- •50.Распространение и физиологическое значение аэробного распада глюкозы. Использование глюкозы для синтеза жиров в печени и в жировой ткани.
- •52. Биосинтез глюкозы (глюконеогенез) из аминокислот, глицерина и молочной кислоты. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
- •54. Свойства и распространение гликогена как резервного полисахарида. Биосинтез гликогена. Мобилизация гликогена.
- •55. Особенности обмена глюкозы в разных органах и клетках: эритроциты, мозг, мышцы, жировая ткань, печень.
- •56. Представление о строении и функциях углеводной части гликолипидов и гликопротеинов. Сиаловые кислоты
- •57. Наследственные нарушения обмена моносахаридов и дисахаридов: галактоземия, непереносимость фруктозы и дисахаридов. Гликогенозы и агликогенозы
- •Глицеральдегид -3 –фосфат
- •58. Важнейшие липиды тканей человека. Резервные липиды (жиры) и липиды мембран (сложные липиды). Жирные кислоты липидов тканей человека.
- •Состав жирных кислот подкожного жира человека
- •59. Незаменимые факторы питания липидной природы. Эссенциальные жирные кислоты: ω-3- и ω-6-кислоты как предшественники синтеза эйкозаноидов.
- •60.Биосинтез жирных кислот, регуляция метаболизма жирных кислот
- •61.Химизм реакций β-окисления жирных кислот, энергетический итог.
- •62. Биосинтез и использование кетоновых тел в качестве источников энергии
- •6З.Пищевые жиры и их переваривание. Всасывание продуктов переваривания. Нарушение переваривания и всасывания. Ресинтез триацилглицеринов в стенке кишечника.
- •64.Образование хиломикронов и транспорт жиров. Роль апопротеинов в составе хиломикронов. Липопротеинлипаза.
- •65.Биосинтез жиров в печени из углеводов. Структура и состав транспортных липопротеинов крови.
- •66. Депонирование и мобилизация жиров в жировой ткани. Регуляция синтеза и мобилизации жиров. Роль инсулина, глюкагона и адреналина.
- •67.Основные фосфолипиды и гликолипиды тканей человека (глицерофосфолипиды, сфингофосфолипиды, гликоглицеролипиды, гликосфиголипиды). Представление о биосинтезе и катаболизме этих соединений.
- •68.Нарушение обмена нейтрального жира (ожирение), фосфолипидов и гликолипидов. Сфинголипидозы
- •Сфинголипиды, метаболизм: заболевания сфинголипидозы, таблица
- •69.Строение и биологические функции эйкозаноидов. Биосинтез простагландинов и лейкотриенов.
- •70.Холестерин как предшественник ряда других стероидов. Представление о биосинтезе холестерина. Написать ход реакций до образования мевалоновой кислоты. Роль гидроксиметилглутарил-КоА-редуктазы.
- •71.Синтез желчных кислот из холестерина. Конъюгация желчных кислот, первичные и вторичные желчные кислоты. Выведение желчных кислот и холестерина из организма.
- •72.Лпнп и лпвп - транспортные, формы холестерина в крови, роль в обмене холестерина. Гиперхолестеринемия. Биохимические основы развития атеросклероза.
- •73. Механизм возникновения желчнокаменной болезни (холестериновые камни). Применение хенодезокеихолевой кислоты для лечения желчнокаменной болезни.
- •74. Общая схема источников и путей расходования аминокислот в тканях. Динамическое состояние белков в организме.
- •75. Переваривание белков. Протеиназы - пепсин, трипсин, химотрипсин; проферменты протеиназ и механизмы их превращения в ферменты. Субстратная специфичность протеиназ. Экзопептидазы и эндопептидазы.
- •76. Диагностическое значение биохимического анализа желудочного и дуоденального сока. Дать краткую характеристику состава этих соков.
- •77. Протеиназы поджелудочной железы и панкреатиты. Применение ингибиторов протеиназ для лечения панкреатитов.
- •78. Трансаминирование: аминотрансферазы; коферментная функция витамина в6. Специфичность аминотрансфераз.
- •80. Окислительное дезаминирование аминокислот; глутаматдегидрогеназа. Непрямое дезаминирование аминокислот. Биологическое значение.
- •81. Основные источники аммиака в организме. Роль глутамата в обезвреживании и транспорте аммиака. Глутамин как донор амидной группы при синтезе ряда соединений.
- •82. Глутаминаза почек; образование и выведение солей аммония. Активация глутаминазы почек при ацидозе.
- •83. Биосинтез мочевины. Связь орнитинового цикла с цтк. Происхождение атомов азота мочевины. Нарушения синтеза и выведения мочевины. Гипераммонемии.
- •84. Обмен безазотистого остатка аминокислот. Гликогенные и кетогенные аминокислоты. Синтез глюкозы из аминокислот. Синтез аминокислот из глюкозы.
- •85. Трансметилирование. Метионин и s-аденозилметионин. Синтез креатина, адреналина и фосфатидилхолинов
- •86. Метилирование днк. Представление о метилировании чужеродных и лекарственных соединений.
- •87. Источники и образование одноуглеродных групп. Тетрагидрофолиевая кислота и цианкобаламин и их роль в процессах трансметилирования.
- •88. Антивитамины фолиевой кислоты. Механизм действия сульфаниламидных препаратов.
- •89. Обмен фенилаланина и тирозина. Фенилкетонурия; биохимический дефект, проявление болезни, методы предупреждения, диагностика и лечение.
- •90. Алкаптонурия и альбинизм: биохимические дефекты, при которых они развиваются. Нарушение синтеза дофамина, паркинсонизм.
- •91. Декарбоксилирование аминокислот. Структура биогенных аминов (гистамин, серотонин, γ-аминомасляная кислота, катехоламины). Функции биогенных аминов.
- •92. Дезаминирование и гидроксилирование биогеных аминов (как реакции обезвреживания этих соединений).
- •93. Нуклеиновые кислоты, химический состав, строение. Первичная структура днк и рнк, связи, формирующие первичную структуру
- •94. Вторичная и третичная структура днк. Денатурация, ренативация днк. Гибридизация, видовые различия первичной структуры днк.
- •95. Рнк, химический состав, уровни структурной организации. Типы рнк, функции. Строение рибосомы.
- •96. Строение хроматина и хромосомы
- •97. Распад нуклеиновых кислот. Нуклеазы пищеварительного тракта и тканей. Распад пуриновых нуклеотидов.
- •98. Представление о биосинтезе пуриновых нуклеотидов; начальные стадии биосинтеза (от рибозо-5-фосфата до 5-фосфорибозиламина).
- •99. Инозиновая кислота как предшественник адениловой и гуаниловой кислот.
- •100. Представление о распаде и биосинтезе пиримидиновых нуклеотидов.
- •101. Нарушения обмена нуклеотидов. Подагра; применение аллопуринола для лечения подагры. Ксантинурия. Оротацидурия.
- •102. Биосинтез дезоксирибонуклеотидов. Применение ингибиторов синтеза дезоксирибонуклеотидов для лечения злокачественных опухолей.
- •103. Биосинтез днк, субстраты, источники энергии, матрица, ферменты. Понятие о репликативном комплексе. Этапы репликации.
- •104. Синтез днк и фазы клеточного деления. Роль циклинов и циклинзависимых протеиназ в продвижении клетки по клеточному циклу.
- •105. Повреждение и репарация днк. Ферменты днк-репарирующего комплекса.
- •106. Биосинтез рнк. Рнк полимеразы. Понятие о мозаичной структуре генов, первичном транскрипте, посттранскрипционном процессинге.
- •107. Биологический код, понятия, свойства кода, коллинеарность, сигналы терминации.
- •108. Роль транспортных рнк в биосинтезе белков. Биосинтез аминоацил-т-рнк. Субстратная специфичность аминоацил-т-рнк-синтетаз.
- •109. Последовательность событий на рибосоме при сборке полипептидной цепи. Функционирование полирибосом. Посттрансляционный процессинг белков.
- •110. Адаптивная регуляция генов у про- и эукариотов. Теория оперона. Функционирование оперонов.
- •111. Понятие о клеточной дифференцировке. Изменение белкового состава клеток при дифференцировке (на примере белкового состава полипептидных цепей гемоглобина).
- •112. Молекяулрные механизмы генетической изменчивости. Молекулярные мутации: типы, частота, значение
- •113. Генетическая гетерогенность. Полиморфизм белков в популяции человека (варианты гемоглобина, гликозилтрансферазы, группоспецифических веществ и др).
- •114. Биохимические основы возникновения и проявления наследственных болезней (разнообразие, распространение).
- •115. Основные системы межклеточной коммуникации: эндокринная, паракринная, аутокринная регуляция.
- •116. Роль гормонов в системе регуляции метаболизма. Клетки-мишени и клеточные рецепторы гормонов
- •117. Механизмы передачи гормональных сигналов в клетки.
- •118. Классификация гормонов по химическому строению и биологическим функциям
- •119. Строение, синтез и метаболизм иодтиронинов. Влияние на обмен веществ. Изменение метаболизма при гипо- и гипертиреозе. Причины и проявление эндемического зоба.
- •120. Регуляция энергетического метаболизма, роль инсулина и контринсулярных гормонов в обеспечении гомеостаза.
- •121. Изменения метаболизма при сахарном диабете. Патогенез основных симптомов сахарного диабета.
- •122. Патогенез поздних осложнений сахарного диабета (макро- и микроангиопатии, нефропатия, ретинопатия, катаракта). Диабетическая кома.
- •123. Регуляция водно-солевого обмена. Строение и функции альдостерона и вазопрессина
- •124. Система ренин-ангиотензин-альдостерон. Биохимические механизмы возникновения почечной гипертонии, отеков, дегидратации.
- •125. Роль гормонов в регуляции обмена кальция и фосфатов (паратгормон, кальцитонин). Причины и проявления гипо- и гиперпаратироидизма.
- •126. Строение, биосинтез и механизм действия кальцитриола. Причины и проявление рахита
- •127. Строение и секреция кортикостероидов. Изменения катаболизма при гипо- и гиперкортицизме.
- •128. Регуляция синтезами секреции гормонов по принципу обратной связи.
- •129. Половые гормоны: строение, влияние на обмен веществ и функции половых желез, матки и молочных желез.
- •130. Гормон роста, строение, функции.
- •131. Метаболизм эндогенных и чужеродных токсических веществ: реакции микросомального окисления и реакции конъюгации с глутатионом, глюкуроновой кислотой, серной кислотой.
- •132. Металлотионеин и обезвреживание ионов тяжелых металлов. Белки теплового шока.
- •133. Токсичность кислорода: образование активных форм кислорода (супероксид анион, перекись водорода, гидроксильный радикал).
- •135. Биотрансформация лекарственных веществ. Влияние лекарств на ферменты, участвующие в обезвреживании ксенобиотиков.
- •136. Основы химического канцерогенеза. Представление о некоторых химических канцерогенах: полициклические ароматические углеводороды, ароматические амины, диоксиды, митоксины, нитрозамины.
- •137. Особенности развития, строения и метаболизма эритроцитов.
- •138. Транспорт кислорода и диоксида углерода кровью. Гемоглобин плода (HbF) и его физиологическое значение.
- •139. Полиморфные формы гемоглобинов человека. Гемоглобинопатии. Анемические гипоксии
- •140. Биосинтез гема и его регуляция. Нарушения синтеза тема. Порфирии.
- •141. Распад гема. Обезвреживание билирубина. Нарушения обмена билирубина—желтухи: гемолитическая, обтурационная, печеночно-клеточная. Желтуха новорожденных.
- •142. Диагностическое значение определения билирубина и других желчных пигментов в крови и моче.
- •143. Обмен железа: всасывание, транспорт кровью, депонирование. Нарушение обмена железа: железодефицитная анемия, гемохроматоз.
- •144. Основные белковые фракции плазмы крови и их функции. Значение их определения для диагностики заболеваний. Энзимодиагностика.
- •145. Свертывающая система крови. Этапы образования фибринового сгустка. Внутренний и внешний пути свертывания и их компоненты.
- •146. Принципы образования и последовательность фукционирования ферментных комплексов прокоагулянтного пути. Роль витамина к в свертывании крови.
- •147. Основные механизмы фибринолиза. Активаторы плазминогена как тромболитические средства. Основаные антикоагулянты крови: антитромбин III, макроглобулин, антиконвертин. Гемофилии.
- •148. Клиническое значение биохимического анализа крови.
- •149. Основные мембраны клетки и их функции. Общие свойства мембран: жидкостность, поперечная асимметрия, избирательная проницаемость.
- •150. Липидный состав мембран (фосфолипиды, гликолипиды, холестерин). Роль липидов в формировании липидного бислоя.
- •151. Белки мембран - интегральные, поверхностные, «заякоренные». Значение посттрансляционных модификаций в образовании функциональных мембранных белков.
- •153. Трансмембранная передача сигнала. Участие мембран в активации внутриклеточных регуляторных систем - аденилатциклазной и инозитолфосфатной в передаче гормонального сигнала.
- •154. Коллаген: особенности аминокислотного состава, первичной и пространственной структуры. Роль аскорбиновой кислоты в гидоксилировании пролина и лизина.
- •155. Особенности биосинтеза и созревания коллагена. Проявления недостаточности витамина с.
- •156. Особенности строения и функции эластина.
- •157. Гликозаминогликаны и протеогликаны. Строение и функции. Роль гиалуроновой кислоты в организации межклеточного матрикса.
- •158. Адгезивные белки межклеточного матрикса: фибронектин и ламинин, их строение и функции. Роль этих белков в межклеточных взаимодействиях и развитии опухолей.
- •159. Структурная организация межклеточного матрикса. Изменения соединительной ткани при старении, коллагенозах. Роль коллагеназы при заживлении ран. Оксипролинурия.
- •160. Важнейшие белки миофибрилл: миозин, актин, актомиозин, тропомиозин, тропонин, актинин. Молекулярная структура миофибрилл.
- •161. Биохимические механизмы мышечного сокращения и расслабления. Роль градиента одновалентных ионов и ионов кальция в регуляции мышечного сокращения и расслабления.
- •162. Саркоплазматические белки: миоглобин, его строение и функции. Экстрактивные вещества мышц.
- •163. Особенности энергетического обмена в мышцах. Креатинфосфат.
- •164. Биохимические изменения при мышечных дистрофиях и денервации мышц. Креатинурия.
- •165. Химический состав нервной ткани. Миелиновые мембраны: особенности состава и структуры.
- •166. Энергетический обмен в нервной ткани. Значение аэробного распада глюкозы.
- •167. Биохимия возникновения и проведения нервного импульса. Молекулярные механизмы синаптической передачи
- •168. Медиаторы: ацетилхолин, катехоламины, серотонин, γ-аминомаслянная кислота, глутаминовая кислота, глицин, гистамин.
- •169. Нарушения обмена биогенных аминов при психических заболеваниях. Предшественники катехоламинов и ингибиторы моноаминооксидазы в лечении депрессивных состояний.
- •170. Физиологически активные пептиды мозга.
- •Биохимические показатели биологических жидкостей человека
27.Изменение активности ферментов при болезнях. Наследственные энзимопатии. Происхождение ферментов крови и значение их определения при болезнях.
В основе многих заболеваний лежат нарушения функционирования ферментов в клетке - энзимопатии. Различают первичные (наследственные) и вторичные (приобретённые) энзимопатии. Приобретённые энзимопатии, как и вообще протеинопатии, по-видимому, наблюдают при всех болезнях.
При первичных энзимопатияхдефектные ферменты наследуются, в основном, по аутосомнорецессивному типу. Гетерозиготы, чаще всего, не имеют фенотипических отклонений. Первичные энзимопатии обычно относят к метаболическим болезням, так как происходит нарушение определённых метаболических путей. При этом развитие заболевания может протекать
по одному из ниже перечисленных "сценариев". Рассмотрим условную схему метаболического пути:
![]()
Вещество А в результате последовательных ферментативных реакций превращается в продукт Р. При наследственной недостаточности какого-либо фермента, например фермента Е3, возможны разные нарушения метаболических путей:
Нарушение образования конечных продуктов. Недостаток конечного продукта этого метаболического пути (Р) (при отсутствии альтернативных путей синтеза) может приводить к развитию клинических симптомов, характерных для данного заболевания:
![]()
Клинические проявления. В качестве примера можно рассмотреть альбинизм. При альбинизме нарушен синтез в меланоцитах пигментов - меланинов. Меланин находится в коже, волосах, радужке, пигментном эпителии сетчатки глаза и влияет на их окраску. При альбинизме наблюдают слабую пигментацию кожи, светлые волосы, красноватый цвет радужки глаза из-за просвечивающих капилляров. Проявление альбинизма связано с недостаточностью фермента тирозингидроксилазы (тирозиназы) - одного из ферментов, катализирующего метаболический путь образования меланинов
Накопление субстратов-предшественников. При недостаточности фермента Е3 будут накапливаться вещество С, а также во многих случаях и предшествующие соединения. Увеличение субстратов-предшественников дефектного фермента - ведущее звено развития многих заболеваний:
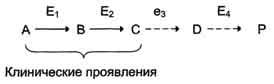
Клинические проявления. Известно заболевание алкапгонурия, при котором нарушено окисление гомогентизиновой кислоты в тканях (гомогентизиновая кислота - промежуточный метаболит катаболизма тирозина). У таких больных наблюдают недостаточность фермента окисления гомогентизиновой кислоты - диоксигеназы гомогентизиновой кислоты, приводящей к развитию заболевания. В результате увеличиваются концентрация гомогентизиновой кислоты и выведение её с мочой. В присутствии кислорода гомогентизиновая кислота превращается в соединение чёрного цвета - алкаптон. Поэтому моча таких больных на воздухе окрашивается в чёрный цвет. Алкаптон также образуется и в биологических жидкостях, оседая в тканях, коже, сухожилиях, суставах. При значительных отложениях алкаптона в суставах нарушается их подвижность.
Нарушение образования конечных продуктов и накопление субстратов предшественников. Отмечают заболевания, когда одновременно недостаток продукта и накопление исходного субстрата вызывают клинические проявления.
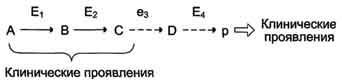
Клинические проявления. Например, у людей с болезнью Гирке (гликогеноз I типа) наблюдают снижение концентрации глюкозы в крови (гипогликемия) в перерывах между приёмами пищи. Это связано с нарушением распада гликогена в печени и выходом из неё глюкозы вследствие дефекта фермента глюкозо-6-фосфатфосфатазы. Одновременно у таких людей увеличиваются размеры печени (гепатомегалия) вследствие накопления в ней не используемого гликогена.
Особый интерес для клиники представляет исследование активностииндикаторныхферментоввсыворотке крови, так как по появлению вплазмеилисыворотке кровиряда тканевыхферментовв повышенных количествах можно судить о функциональном состоянии и поражении различных органов (например,печени, сердечной и скелетной мускулатуры). При остром инфаркте миокарда особенно важно исследоватьактивностькреатинкиназы, АсАТ, ЛДГ и оксибутиратдегидрогеназы. При заболеванияхпечени, в частности при вирусном гепатите (болезнь Боткина), всыворотке кровизначительно увеличиваетсяактивностьАлАТ и АсАТ, сорбитолдегидрогеназы,глутаматдегидрогеназыи некоторых другихферментов. озрастаниеактивности ферментовсыворотки кровипри многих патологических процессах объясняется прежде всего двумя причинами: 1) выходом в кровяное руслоферментовиз поврежденных участков органов илитканейна фоне продолжающегося ихбиосинтезав поврежденныхтканях; 2) одновременным повышением каталитическойактивностинекоторыхферментов, переходящих вкровь. Возможно, что повышениеактивности ферментовпри «поломке» механизмов внутриклеточной регуляцииобмена веществсвязано с прекращением действия соответствующих регуляторов иингибиторов ферментов, изменением под влиянием различных факторов строения и структурымакромолекулферментов.
28.Применение ферментов для лечения болезней. Применение ферментов как аналитических реагентов при лабораторной диагностике (определении глюкозы, этанола, мочевой кислоты и т.д.). Иммобилизованные ферменты
Второе направление медицинской энзимологии – энзимодиагностика– развивается по двум путям. Один путь – использованиеферментовв качестве избирательныхреагентовдля открытия и количественного определения нормальных или аномальных химическихвеществвсыворотке крови,моче, желудочном соке и др. (например, выявление при помощиферментовглюкозы,белкаили другихвеществвмоче, в норме не обнаруживаемых). Другой путь – открытие и количественное определение самихферментовв биологическихжидкостяхпри патологии. Оказалось, что рядферментовпоявляется всыворотке кровипри распадеклеток(отсюда их название «некротическиеферменты»). Для диагностики органических и функциональных поражений органов итканейшироко применяются отдельные ферментныетесты, выгодно отличающиеся от других химических диагностическихтестов, используемых в клинике, высокой чувствительностью испецифичностью. Известно около 20тестов, основанных на количественномопределении активности ферментов(иизоферментов), главным образом вкрови(реже вмоче), а также в биоптатах (кусочкитканей, полученные прибиопсии). Следует отметить, что из огромного числаферментов(более 3500), открытых в природе (частично и ворганизмечеловека), в диагностической энзимологии используется лишь ограниченный наборферментови для весьма небольшого числа болезней (гепатиты, инфаркт миокарда, органические поражения почек, поджелудочной железы,печении др.). Так, уровеньлипазы,амилазы,трипсинаихимотрипсинавкровирезко увеличен присахарном диабете, злокачественных поражениях поджелудочной железы, болезняхпечении др. Резко повышается всыворотке кровиуровень двух аминотрансфераз, креатинкиназы (и ее изоформ) илактатдегидрогеназы(и ее изоформ) при инфаркте миокарда; умеренно повышено их содержание при пораженияхтканеймозга ипечени. Определяют, кроме того,активностькислой фосфатазы(уровень повышен прикарциномепредстательной железы), щелочнойфосфатазы, холинэсте-разы и некоторых других органоспецифическихферментов(например, гистидазы, уроканиназы, глицинамидинотрансферазы) всыворотке кровипри патологиикостной ткани,печени, метастатическихкарциномахи т. д. Доказано, что органы итканичеловека характеризуются специфическим ферментным и изоферментным спектром, подверженным не только индивидуальным, но и суточным колебаниям. Существует большой градиентконцентрацииферментовмежду внутриклеточными и внеклеточными частями тела. Поэтому любые, даже незначительные, поврежденияклеток(иногда функциональные расстройства) приводят к выделениюферментовво внеклеточное пространство, откуда они поступают вкровь. Механизм гиперферментации (повышенное содержаниеферментоввкрови) до конца не расшифрован. Повышение уровня внутриклеточныхферментоввплазме кровипрямо зависит от природы повреждающего воздействия, времени действия и степени повреждения биомембранклетоки субклеточных структур органов. В оценке ферментныхтестовдля диагностических целей особое значение имеет знание периода полужизни (полураспада) вплазме кровикаждого из диагностическихферментов, что делает важным выбор точного времени для ферментного анализакрови. Весьма существенным является также знание особенностей распределения (топографии)ферментовв индивидуальных органах итканях, а также их внутриклеточной локализации.
В последнее время стали применять ферментырестрикции– специфическиеэндонуклеазыкатализирующие разрывы межнуклео-тидных связейДНК, для диагностикифенилкетонурии, α- и β-талассемии и другихнаследственныхболезней человека. Метод основан наполиморфизмерестрикционных фрагментовДНК.
Из представленных данных следует, что диагностическая энзимология может служить основой не только для постановки правильного и своевременного диагноза болезни, но и для проверки эффективности применяемого метода лечения.
Дальнейшее развитие диагностической энзимологии преимущественно идет по двум перспективным направлениям медицинской энзимологии: по пути упрощения и рациональной модификации уже испытанных методов и по пути поиска новых органоспецифических (тканеспецифических) ферментовиизоферментов.
Третье направление медицинской энзимологии – энзимотерапия, т.е. использованиеферментови модуляторов (активаторовиингибиторов) действияферментовв качествелекарственных средств, имеет пока небольшую историю. Досихпор работы в этом направлении почти не выходят за рамки эксперимента. Исключение составляют некоторые про-теиназы:пепсин,трипсин,химотрипсини их смеси (абомин,химопсин), которые применяют для лечения ряда болезней пищеварительного тракта. Помимо протеиназ, ряд другихферментов, в частностиРНКаза, ДНКаза, гиалуронидаза,коллагеназы, эластазы, отдельно или в смеси с протеина-зами используются при ожогах, для обработки ран, воспалительных очагов, устранения отеков, гематом, келоидных рубцов, кавернозных процессов при туберкулезе легких и др.Ферментыприменяются также для лечения сердечно-сосудистых заболеваний,растворениясгустковкрови. В нашей стране разработан первый в мире препарат иммобилизованной стрептокина-зы, рекомендованный для лечения инфаркта миокарда. Калликреины –ферментыкининовой системы используются для снижения кровяногодавления.
Важной и многообещающей областью энзимотерапии является применение ингибиторов ферментов. Так, естественныеингибиторыпротеиназ (α1-трипсин, α1-химотрипсин, α-макроглобулин) нашли применение в терапии острых панкреатитов, артритов, аллергических заболеваний, при которых отмечается активацияпротеолизаифибринолиза, сопровождающаяся образованием вазоактивныхкининов.
В последнее время получило признание применение в онкологической клинике ферментовбактериальной природы в качествелекарственных средств. Широко используется L-аспарагиназа (выпускается в промышленных количествах и L-глутамин(аспарагин)азадля лечения острых и хронических формлейкозовилимфогранулематозов. Более десятка описанных в литературе бактериальныхферментовиспытаны в основном на животных с перевивнымиопухолямиили на раковыхклеткахопухолейчеловека и животных, выращенных вкультуре ткани. Основными постулатамиприменения ферментовв онкологии являются различия вметаболизмеклетокопухолейпо сравнению с обменом в нормальной, здоровой,клетке. В частности, современные стратегия и тактика энзимотерапии опухолевых поражений учитывают разную чувствительность нормальных и опухолевыхклетокк недостатку (дефициту) незаменимых (так называемых эссенциальных) факторов роста. К таким ростстимулирующим факторам относятся не только пищевые факторы (витамины, незаменимыеаминокислоты, макро- имикроэлементы), но и ряд так называемых заменимыхвеществ, включая заменимыеаминокислоты, к недостатку которых опухолеваяклеткаоказывается в силу особенностей ее обмена более чувствительной, чем нормальная. Лечебный эффект, например, L-аспарагиназы и L-глутамин (аспа-рагин)азыприлейкозах, вероятнее всего, объясняется необратимым распадом какглутамина, так иаспарагина. Оказалось, что опухолевыеклеткидля своего роста и размножения нуждаются ваминокислотахизорганизма, поскольку сами лишены способности синтезировать амидыаминокислот, в то время как нормальныеклеткинаделены этой способностью. Был сделан вывод о том, что амидныйазотглутаминаиаспарагинавыполняет вклеткахряд уникальных функций, которые лучше выяснены для глута-мина. В частности, амидныйазотглутаминаоказался абсолютно необходимым и не заменимым другимиаминокислотамиисточникоматомаазотаминимум в 10реакцияхсинтеза, например, пуриновых и пиримидиновыхнуклеотидов, соответственноДНКиРНК,АТФ, ге-ксозаминов,гистидинаи др. Таким образом, не лишенаоснованиягипотеза, что любойферментили агент, катализирующий необратимое расщепление незаменимого для опухолевойклеткипищевого фактора (включаяаминокислоты), может в принципе быть применен в энзимотерапииопухолей, если будут устранены ограничения, связанные с белковойприродой фермента. В оценке эффективностиферментовв экспериментальной и клинической онкологии имеется немало противоречий и очень много пробелов. Положительные результаты, отмеченные в ряде случаев, вселяют надежду, что приготовление стандартных ферментных препаратов (включая создание иммобилизованных форм) в промышленных масштабах и их разумное применение в клинике, организованное на строгой научной основе, несомненно дадут в руки врачей еще одно ценное оружие в борьбе с опухолевыми заболеваниями человека.
Идея применения ферментовв качествелекарственных средств(фармакологииферментов) всегда казалась заманчивой. Однако их нестабильность, короткий период полураспада, нежелательные антигенные свойства, связанные с белковойприродой ферментови опасностью развития аллергическихреакций, трудности доставки к пораженным органам итканям(мишеням) существенно ограничивали возможности использования ферментных препаратов. В разработке методовиммобилизацииферментовнаметились конкретные пути преодоления указанных трудностей: применение водорастворимых, биосовместимыхносителей, например полимолочнойкислоты(легко разлагается ворганизме), использование методов химической модификации имикрокапсулирования, приготовление моно- и поликлональныхантители ферментсодержащих липосом и т.д.
В последнее время интенсивно разрабатываются методы направленного транспорта ферментов, заключенных в своеобразные микроконтейнеры (тениэритроцитов,липосомыи др.), к внешней поверхности которых могут быть прикреплены адресные (векторные) белковыемолекулы(например,иммуноглобулины–антителапротив специфических компонентов органа или ткани-мишени, в частностиопухоли).Иммобилизованные ферментыв качествелекарственных средствначали применять в специальных колонках для экстракорпоральной перфузиикрови(типа искусственной почки). Такое лечение полностью исключает нежелательные воздействия наорганизмчужеродногобелкаи может проводиться длительное время.
