
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
Ростовская-на-Дону государственная академия
сельскохозяйственного машиностроения
Кафедра «Электротехника и техническая кибернетика» Атомная и ядерная физика. Элементы квантовой механики
Методические указания к типовому расчету по физике
для студентов 2-го курса специальностей 280102, 140604, 140607,
220201, 230201, 110304, 190206, 151001, 150201, 150202, 150502
всех форм обучения
Ростов-на-Дону
2008
Составители:
|
кандидат физико-математических наук, доцент кандидат педагогических наук, доцент кандидат физико-математических наук, доцент |
|
В.В. Шегай И. И. Джужук Н.В. Дорохова |
УДК 537.8
|
|
|
Атомная и ядерная физика. Элементы квантовой механики: Метод. указания к типовому расчету по физике / РГАСХМ ГОУ, Ростов н/Д, 2008. — 31 с. |
Методические указания представляют собой практическое руководство к выполнению типового расчета в третьей части курса физики. Оно включает краткие теоретические сведения, справочные данные и задачи для самостоятельного решения по темам: теория атома Бора, волны де Бройля, соотношение неопределенностей Гейзенберга, стационарное уравнение Шредингера, теория атомного ядра.
Предназначены для студентов 2-го курса специальностей 280102, 40604, 140607, 220201, 230201, 110304, 190206, 151001, 150201, 150202, 150502 всех форм обучения.
|
Печатается по решению редакционно-издательского совета академии |
|
Рецензент |
кандидат физико-математических наук, доцент |
В. А. Ваган |
|
Научный редактор |
Кандидат физико-математических наук, доцент |
В. В. Шегай |
|
Ó |
Государственное образовательное учреждение высшего профессионального образования Ростовская-на-Дону государственная академия сельскохозяйственного машиностроения, 2008 |
Введение
1. Теория атома Бора основана на трех постулатах:
1) Существуют стационарные состояния атома, находясь в которых атом не излучает и не поглощает энергию.
2) При переходе атома из одного стационарного состояния в другое испускается или поглощается квант электромагнитной энергии (фотон):
![]() ,
,
где h — постоянная Планка; ν — частота излучения; Еm, Еk — энергия атома в разных стационарных состояниях (m, k номера стационарных состояний).
Если Еm > Ек , то фотон излучается , если Еm < Ек , то фотон поглощается.
3) Момент импульса электрона в атоме в стационарном состоянии
![]()
где m — масса электрона, vn — его линейная скорость, rn — радиус орбиты электрона в стационарном состоянии, n номер стационарного состояния (n = 1,2,…).
Для водородоподобного атома, т.е. атома, имеющего один электрон:
1) радиус стационарной орбиты электрона:
![]() ,
,
где ε0 — электрическая постоянная; Z — порядковый номер элемента в таблице Менделеева; e — заряд электрона;
2) Еk кинетическая энергия электрона:
![]()
3) Еp потенциальная энергия электрона:
![]()
4) Еполн полная энергия электрона:
![]()
Состояние атома, соответствующее n = 1, называется основным состоянием.
Энергия ионизации — это минимальная энергия, которую нужно сообщить электрону, чтобы удалить его из атома:
Еион = – Еполн
Потенциал ионизации это отношение полной энергии электрона в атоме к заряду электрона:
φион = Еполн/e.
Частота излучения водородоподобного атома определяется по формуле Бальмера - Ритца:
![]() ,
,
где R — постоянная Ридберга; n, m — номера стационарных орбит электрона.
Для атома водорода (Z = 1) при n = 1 образуется спектральная серия Лаймана; при n = 2 — серия Бальмера; при n = 3 — серия Пашена; при n = 4 — серия Бреккета.
2. Волна де Бройля это волна, соответствующая любой материальной частице. Длина волны де Бройля:
![]() ,
,
где р= mv — импульс; m — масса; v — скорость частицы.
3. Соотношение неопределенностей Гейзенберга для координаты x и проекции px импульса частицы на ось X:
Δx Δpx ≥ h/2π.
Соотношение неопределенностей Гейзенберга для энергии E и времени t жизни частицы:
ΔEΔt ≥ h/2π.
4. Стационарное уравнение Шредингера для частицы, совершающей движение вдоль оси Х:
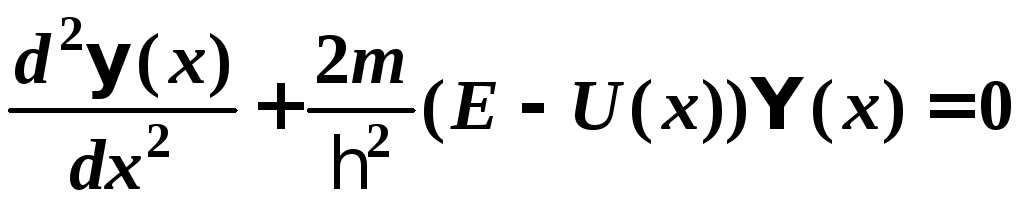 ,
,
где ψ(x) — координатная часть волновой функции; Е — полная и U(x) — потенциальная энергии частицы; ћ = h/2π, m — масса частицы.
Вероятность обнаружения частицы, находящейся в стационарном состоянии на интервале a≤ x≤ b:
![]() P(a,b)=
P(a,b)=![]() .
.
Волновая функция, описывающая одномерное движение свободной частицы:
![]()
где A амплитуда волны де Бройля; p импульс; Е энергия частицы.
Собственная волновая функция частицы, находящейся в бесконечно глубоком одномерном потенциальном ящике шириной L:
ψn(x)
=
![]() ·
·![]() ,n=
1,2,3,…
,n=
1,2,3,…
Собственное значение энергии частицы, находящейся в бесконечно глубоком одномерном потенциальном ящике шириной L:
En
=
![]() .
.
5. Ядерная физика.
Нуклонная модель ядра.
Ядро состоит из протонов и электрически нейтральных частиц нейтронов. Массы протона и нейтрона практически одинаковы. Поэтому они имеют общее название — нуклоны.
Зарядовое число Z (заряд ядра) — это число протонов в ядре. Зарядовое число совпадает с порядковым номером соответствующего элемента в таблице Менделеева.
Массовое число M — это число нуклонов в ядре:
M = Z + N,
где Z — число протонов; N — число нейтронов.
Ядро атома Х
принято обозначать
![]() .
Например, ядро атома гелия (α-частица)
— это
.
Например, ядро атома гелия (α-частица)
— это![]() .
Оно содержитZ
= 2 протона и N
= 2 нейтрона.
.
Оно содержитZ
= 2 протона и N
= 2 нейтрона.
Изотопы — это атомы, ядра которых содержат одинаковое число протонов Z, но разное число нейтронов N. Поэтому изотопы имеют одинаковые зарядовые, но разные массовые числа. Например, изотопы водорода:
![]() (водород),
(водород),
![]() (дейтерий),
(дейтерий),![]() (тритий).
(тритий).
Ядерные реакции.
Ядерными реакциями называются превращения атомных ядер, вызванные их взаимодействием с различными частицами или друг с другом.
Закон сохранения суммарного заряда Z и массового числа А в ядерных реакциях. Общий заряд частиц и общее число нуклонов до и после реакции должно быть одинаково.
Дефект массы в ядерных реакциях:
Δm= ∑mi1∑mk2,
где ∑mi1 суммарная масса частиц до реакции; ∑mk2суммарная масса частиц после реакции.
Согласно специальной теории относительности Эйнштейна каждая материальная частица обладает полной энергией, равной
E = mc2,
где m — масса частицы; c — скорость света.
Энергия связи атомных ядер равна разности между энергией ядра и энергией составляющих ядро нуклонов в свободном состоянии.
Энергия связи может выделяться или поглощаться в ядерных реакциях. Величину этой энергии можно найти по формуле:
ΔE= Δmc2.
Радиоактивность самопроизвольное превращение одних атомных ядер в другие.
Закон радиоактивного распада.
Число радиоактивных N ядер убывает с течением времени t по закону:
![]() ,
,
где N0 — число ядер в момент времени t = 0; e @ 2,72 основание натуральных логарифмов; l (с1) — радиоактивная постоянная (постоянная распада).
Период полураспада Т (с), — время в течение которого распадается половина первоначального количества радиоактивных ядер.
Связь между периодом полураспада и радиоактивной постоянной:
![]() .
.
Активность радиоактивного вещества равна числу ядер, распадающихся за единицу времени:
A = lN.
Радиоактивность сопровождается испусканием a -, b - частиц и g - лучей (радиоактивным излучением). a-частицы — ядра гелия; b - частицы — электроны, g-лучи — электромагнитное излучение (фотоны).
