
06-09-2014_00-25-24 (1) / Лекция 17
.docxЛекция №17.
Оценка допустимости применения континуального приближения
Допустимость применения континуального приближения оценивается по критерию Кнудсена
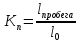
-
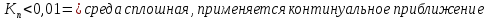
-
0,01
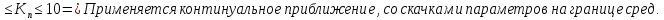
Скачки температур, скоростей, концентраций, давлений учитываются в граничных условиях.
-
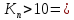 молекулярное
течение, все уравнения переноса берутся
из статической физики –
молекулярное
течение, все уравнения переноса берутся
из статической физики –

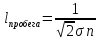 ,
,
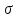 –
эффективное сечение столкновения
молекул,
–
эффективное сечение столкновения
молекул,
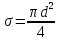 ,
n
,
n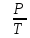 – число молекул,
– число молекул,
d =r1+r2 – эффективный диаметр молекул при столкновении
Течение со скачками

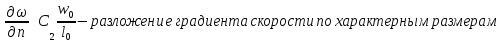
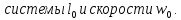
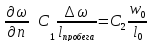
« »
значения скачков параметров определяются
знаком производной параметрической
зависимости.
»
значения скачков параметров определяются
знаком производной параметрической
зависимости.
Приравнивая уравнения, получаем выражения для расчета скачков параметров:
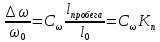

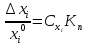
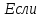 0,01
0,01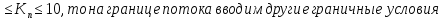
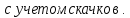
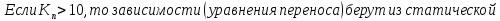
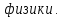
Критерий
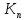 для
газов
для
газов
Только
в газах и вакууме возможно, что
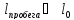
Кинематическая
вязкость:
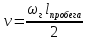 ,
,
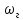 – скорость движения молекул в газе
(скорость звука в газе)
– скорость движения молекул в газе
(скорость звука в газе)
Вязкое течение:
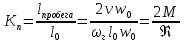
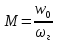 -
критерий
Маха – отношение характерной скорости
к скорости звука.
-
критерий
Маха – отношение характерной скорости
к скорости звука.

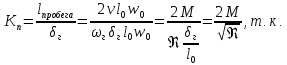

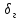 -
толщина
гидродинамического слоя
-
толщина
гидродинамического слоя
Практические задачи в процессах переноса массы
Процессы разделения в процессах массопереноса
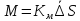
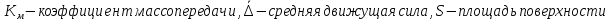
Условия для процесса разделения:
-
Необходимо иметь 2 фазы и межфазную границу, через которую проходит перенос вещества;
-
Необходимо различие равновесных концентраций компонента в фазах.
«Равновесие в системе пар – жидкость»
1.Идеальная смесь «пар – жидкость» - это смесь, подчиняющаяся законам Рауля и Дальтона
Закон Рауля: парциальное давление равно упругости паров смеси, умноженного на концентрацию смеси.
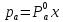 -
парциальное давление компонента
-
парциальное давление компонента
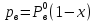
Закон Дальтона: общее давление в системе равно сумме парциальных давлений компонентов в ней:
Р=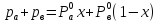
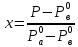 -
концентрация компонента в бинарной
жидкой фазе.
-
концентрация компонента в бинарной
жидкой фазе.
Концентрация компонента а в парах:
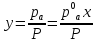 ,
график y=f(Р)
– гипербола
,
график y=f(Р)
– гипербола
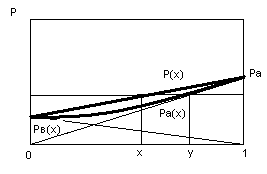
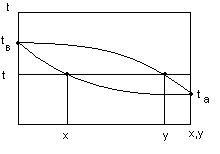
Легкокипящий компонент – компонент, упругость паров которого больше при данной температуре.
Закон Коновалова: пар обогащен легколетучим компонентом.
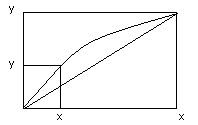
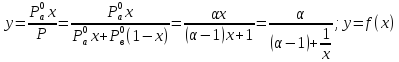 -гиперболическая
зависимость
-гиперболическая
зависимость
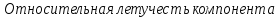 :
:
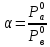
Гипербола ( x, y- диаграмма) выше диагонали, тогда выполняется закон Коновалова.
Реальные смеси.
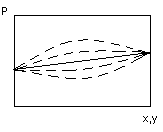
В точках экстремума возникают азеотропные точки (состав пара и жидкости в них одинаков)

Поэтому разделить такие смеси в процессе испарения – конденсации не возможно.
на диаграмме Р, ху – минимум на диаграмме Т, ху.
В азеотропной точке нельзя просто разделить азеотропные смеси.
Дистилляция
Дистилляция – разделение жидких смесей на отличающиеся по составу фракции. Она основана на различии в составах жидкости и образующегося пара на основе первого закона Коновалова. Процесс осуществляется испарением жидкости и последующей конденсацией пара.
Процесс дистилляции

Расчет процесса непрерывной дистилляции
Баланс по потокам:
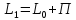
Баланс по компоненту:
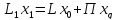
y
= f(x)
– 3
уравнения и 3 неизвестных
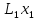 и одна из концентраций или один из
выходных потоков известен. Мы им задаемся.
Система замкнута.
и одна из концентраций или один из
выходных потоков известен. Мы им задаемся.
Система замкнута.
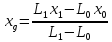
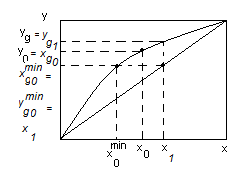
 .
При
.
При
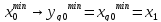 ,
т.е. при дальнейшей перегонке будет
ухудшаться состав дистиллята по отношению
к х.
,
т.е. при дальнейшей перегонке будет
ухудшаться состав дистиллята по отношению
к х.
Баланс тепла по контуру

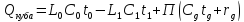
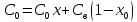 -
теплоемкость смеси подчиняется закону
аддитивности
-
теплоемкость смеси подчиняется закону
аддитивности
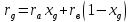 -
скрытая теплота смеси подчиняется
закону аддитивности
-
скрытая теплота смеси подчиняется
закону аддитивности
Тепловой
баланс конденсатора:
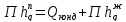
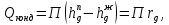
 теплота
конденсации паров
теплота
конденсации паров
Поверхность куба определяется из основного уравнения теплопередачи:
 ,
где
,
где
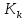 – коэффициент теплопередачи при
кипении.
– коэффициент теплопередачи при
кипении.
Расчет процесса периодической дистилляции
Материальный баланс по компоненту из – за изменения концентрации и количества смеси в кубе записывается в дифференциальной форме:


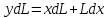
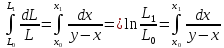 – закон,
связывающий количество жидкости L
в кубе и текущую концентрацию вещества
в кубе х:
– закон,
связывающий количество жидкости L
в кубе и текущую концентрацию вещества
в кубе х: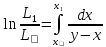 .
Интеграл берется графически с
использованием х – у – диаграммы:
.
Интеграл берется графически с
использованием х – у – диаграммы:
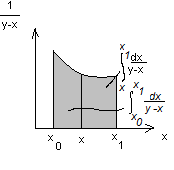
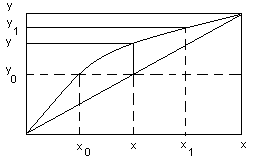
Стадия нагревания смеси в кубе. Баланс из – за меняющейся температуры в кубе записывается в дифференциальной форме:

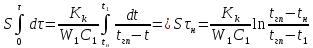
Стадия кипения (дистилляции):
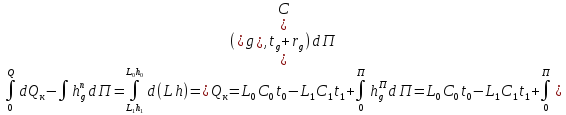
Алгоритм
определения связи между
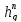 и П приведен ниже:
и П приведен ниже:
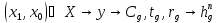


L 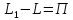

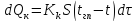
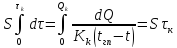
Задается
промежуточная концентрация
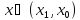 ,
определяется текущее L
и П, y
=
,
определяется текущее L
и П, y
=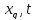 ,
затем текущее Q
и
,
затем текущее Q
и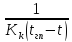 .
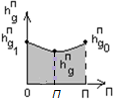
Строится кривая и вычисляется зачерненная
площадь. Она равна некому интегралу.
.
Строится кривая и вычисляется зачерненная
площадь. Она равна некому интегралу.
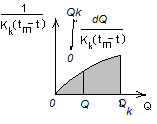
 ,
при фиксированной S
,
при фиксированной S
Перегонка с водяным паром
Применяется для вещества, которое нежелательно нагревать до высоких температур, т.к. они разлагаются при кипении под атмосферном давлением. Для понижения температуры кипения к целевому компоненту добавляют несмешивающееся вещество (чаще всего воду).
Вода – бензол
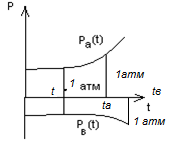 P
=
P
=
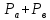 - по закону Дальтона
- по закону Дальтона
Надо смешать «б» и «в» в таких количествах, чтобы они выкипели одновременно:
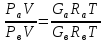
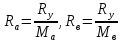
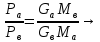 соотношение,
определяющее расходы компонентов.
соотношение,
определяющее расходы компонентов.

