
ЛР металлургия / 2.Скорость окисления углерода / Теория
.docЛАБОРАТОРНАЯ РАБОТА 2
КИНЕТИЧЕСКИЕ ОСОБЕННОСТИ ОКИСЛЕНИЯ УГЛЕРОДА
(2 часа)
-
Цель работы.
Проведение плавки железоуглеродистого сплава в печи Тамма с целью установления кинетических закономерностей окисления углерода при его различных содержаниях в металле.
II. Теоретическое введение
Процесс окисления углерода обычно рассматривается как совокупность последовательных стадий переноса реагентов, адсорбции реагентов и продуктов и собственно химических превращений. Параллельные ему процессы окисления шлакообразующих примесей металлического расплава (кремния, марганца и др.), а также самого железа для упрощения не учитывается.
Реакция окисления углерода
(2.1)
является гетерогенной и развивается на поверхности окислительный газ - жидкий металл либо на поверхности восстановительный, нейтральный или слабоокислительный газ - жидкий металл. Протекание реакции требует одновременного присутствия на межфазной границе углерода и кислорода. Этот процесс можно представить в виде следующих стадий:
1 - перенос кислорода в газовой фазе - внешнедиффузионная стадия;
2 - перенос углерода в металлической фазе - внутридиффузионная стадия;
3 - собственно химическое взаимодействие углерода и кислорода - кинетическая стадия;
- кроме того, в ряде случаев выделяют также стадию зарождения новой фазы (продуктов реакции) и удаление продуктов реакции из реакционной зоны.
Скорость всего процесса ограничивается самой медленной стадией, получившей название лимитирующей.
Выделить лимитирующую стадию процесса обезуглероживания можно, сравнив потоки реагентов к реакционной поверхности. Впервые это было сделано С.И.Филипповым, что позволило ему развить на этой основе теорию критических концентраций.
Скорость переноса O и C углерода к реакционной поверхности можно записать:

Рис. 2.1. Диффузионные потоки окислителя и окисляемого элемента.
Сравнение диффузионных потоков при постоянных условиях их подвода к реакционной поверхности приведено на рис 2.1.
Поток кислорода на этом рисунке показан горизонтальными прямыми линиями, так как он зависит от условий подвода к расплаву и не зависит от концентрации углерода. Поток углерода выражается прямыми, выходящими из начала координат, так как поток углерода также зависит от условий подвода (2.3) и (2.4) и прямо пропорционален его концентрации в металле.
В области повышенных концентраций углерода его диффузионный поток больше потока кислорода. Следовательно, лимитирующей стадией процесса является перенос кислорода, т.е. внешнедиффузионная стадия.
В области низких концентраций углерода его диффузионный поток меньше потока кислорода. Следовательно, в этом случае лимитирующей стадией процесса является перенос углерода, т.е. внутридиффузионная стадия.
Концентрации углерода, соответствующие точкам пересечения линий диффузионных потоков окислителя и окисляющегося элемента, называются критическими концентрациями ([С]). Таким образом, критические концентрации характеризуют переход процесса окисления углерода от внешнедиффузионного режима к внутридиффузионному.
Существуют экспериментальные методы, позволяющие подтвердить описанные выше теоретические положения. Одним из них является продувка железоуглеродистого расплава кислородом при постоянной температуре с периодическим отбором проб металла для определения содержания в нем углерода. По результатам химического анализа определяется скорость окисления углерода и строятся графики зависимости:
-
содержания углерода в металле от времени;
-
скорости окисления углерода от его содержания в расплаве.
Как следует из теории, при лимитировании процесса внешнедиффузионным звеном скорость окисления углерода не зависит от его содержания в расплаве и, следовательно, массовая доля углерода должна со временем убывать по линейному закону. При лимитировании же процесса внутридиффузионным звеном, скорость окисления углерода, как это следует из уравнения (2.3), должна линейно убывать с уменьшением массовой доли углерода, а последняя должна изменяться во времени по логарифмическому закону. Скорость переноса углерода (2.3) будет, естественно, аналогом скорости его окисления. Утверждение о логарифмическом характере зависимости [С] = f(т) следует из решения дифференциального уравнения (2.3) после разделения переменных при условии постоянства значений … и ….
Если подобный эксперимент провести хотя бы при двух разных температурах, то можно определить энергию активации процесса, а по ней установить его лимитирующее звено. Зависимость энергии активации процесса от температуры описывается уравнением:
где К - константа скорости окисления; Еа - энергия активации процесса, Дж/моль; R - универсальная газовая постоянная; Т - температура, К.
III. Лабораторная установка.
Лабораторная установка (рис 2.2) для проведения данной работы представляет собой печь сопротивления (печь Таммана), в высокотемпературной зоне которой находится тигель с металлом. Подвод газообразного окислителя к поверхности жидкого металла осуществляется через кварцевую трубку (фурму) диам. 3 - 5 мм. Поддержание необходимой температуры металла осуществляется путем регулирования электрического режима печи, а контроль температуры осуществляется термопарой ТВР (измерительный прибор - КСП-4).
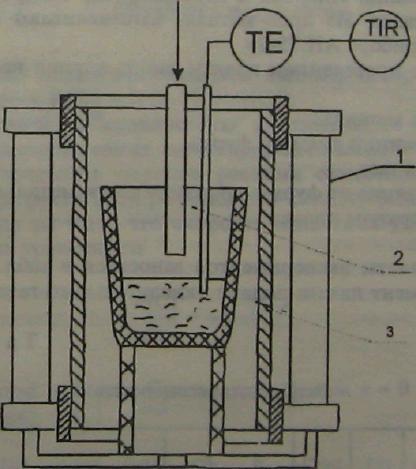
Рис. 2.2. Схема установки
1 - печь сопротивления Таммана; 2 - кварцевая трубка; 3 - тигель с металлом; ТЕ - термопара; TIR- измерительный прибор, показывающий, регистрирующий
IV. Порядок проведения работы и правила техники безопасности.
Тигель с 250 - 300 г синтетического чугуна (сплав железо - углерод, предварительно выплавленного путем науглероживания кипящего армко-железа) помещают в печь и включают нагрев металла. После расплавления и достижения заданной температуры эксперимента фурму спускают в печь таким образом, чтобы нижний ее срез находился на расстоянии 40 мм от поверхности металла. После этого устанавливают заданный расход окислительного газа (около 0,4 - 1 л/мин).
По ходу проведения эксперимента через каждые 3-5 мин. отбирают пробу металла кварцевой трубкой для определения содержания углерода и периодически контролируют температуру металла. Из проб металла изготавливают образцы для анализа на приборе АН.75-29.
Перед проведением плавки записываются исходные данные:
Масса металла...
Внутренний диаметр фурмы...
Расход газа...
Расстояние от фурмы до поверхности металла...
Температура плавки....
Результаты экспериментов заносятся в табл. 2.1 (начало расчета - момент начала подачи окислительного газа).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
