
- •Метод МО Хюккеля
- •π–электроны химически гораздо активнее, чем σ–электроны, поэтому метод Хюккеля оказывается
- •Уравнения Хартри-Фока-Рутана
- •Основные проблемы метода МО связаны с необходимостью процедуры самосогласования, включающей многократные вычисления интегралов
- •3. Недиагональные интегралы Fij разделяются на два типа.
- •Гетероатомные молекулы в методе МОХ
- •Система параметров Стрейтвизера
- •Атом
- •Значения параметров h связаны с электро- отрицательностями атомов (способностью захватывать и удерживать электроны)
- •Малеиновый
- •Домашнее задание
- •Алгоритм решения хюккелевской задачи
- •ЭТИЛЕН СС
- •Уравнение Хюккеля
- •Корреляционная диаграмма
- •АЛЛИЛ
- •Уравнение Хюккеля
- •Уравнение Хюккеля
- •Корреляционная диаграмма
- •Общие решения
- •Линейные полиены
- •Коэффициенты МО
- •Аллил
- •Домашнее задание
- •Циклические полиены (аннулены)
- •Характеристическое
- •Корреляционная диаграмма
- •Общие решения для аннуленов Орбитальные энергии
- •Циклобутадиен
- •Циклопентадиенил-анион
- •Бензол
- •Число связывающих МО всегда нечетно и его можно выразить формулой
- •Циклопропенил-катион
- •Циклопропенил-анион
- •Циклооктатетраен
- •Максимальный выигрыш в энергии наблюдается тогда, когда все связывающие МО полностью заселены, а
- •Коэффициенты МО
- •Атомные
- •Процедура преобразования к действительному базису возможна для любого аннулена
- •Бензол
- •Гетероатомные молекулы
- •Характеристическое уравнение
- •Коэффициенты МО
- •Атомно-молекулярная матрица
- •ЭТИЛЕН
- •ФОРМАЛЬДЕГИД
- •Винилхлорид
- •Корреляционная диаграмма
- •Реальная структура
- •Величина ЕRes показывает, насколько велики отклонения от предсказаний классической теории строения молекул
- •Амидная группа
- •Молекулярная диаграмма (реальная структура)
- •Реальная структура
- •Сероокись углерода
- •Молекулярная диаграмма (реальная структура)
- •Реальная структура
- •Молекулярная диаграмма (реальная структура)
- •Реальная структура
- •Задача 8.3.
- •МОЛЕКУЛЫ
- •В четных АУ нециклического типа величины Х имеют вид Хk , т.е. встречаются
- •Четные АУ
- •Для нециклических альтернантных молекул все величины Х различны между собой; все энергетические уровни
- •Альтернантные Альтернантные Неальтернантные нециклические циклические циклические

Метод МО Хюккеля |
(МОХ) |
|
σ- и π - электроны |
+ |
+ |
|
– |
|
|
|
|
Вследствие ортогональности волновых функций σ- и π – электроны не могут обмениваться
состояниями и поэтому ведут себя как независимые электронные подсистемы.
| = 0
Метод МО Хюккеля предназначен для описания только π – электронных подсистем
π–электроны химически гораздо активнее, чем σ–электроны, поэтому метод Хюккеля оказывается
особенно полезным для решения проблем реакционной способности молекул
C C C
C C O C
O C N
N
Алкены и диены |
Альдегиды, кетоны, |
Имины |
|
сложные эфиры и др. |
|
N O
Арены |
Гетероциклы |

φ = С1 ψ1 + С2 ψ2 + … + Сn ψn
молекулярная |
Базисный набор |
орбиталь |
(атомные орбитали) |
Матрично-векторная форма:
φ1 |
|
С11 |
С12 |
… С1n |
|
ψ1 |
φ2 |
= |
С21 |
С22 |
… С2n |
• |
ψ2 |
… |
|
………………. |
|
… |
||
φn |
|
Сn1 Сn2 … Сnn |
|
ψn |
||

Уравнения Хартри-Фока-Рутана
F – S |
F – S . |
. |
F n – S n |
С |
|
F – S |
F – S . |
. |
F n – S n |
С |
|
. . . . . . . . . |
• . |
= 0 |
|||
. . . . . . . . . |
. |
|
|||
Fn – Sn |
Fn – Sn . |
|
. Fnn – Snn |
Сn |
|
F — матричные элементы оператора Фока, характеризующие
либо энергию электрона в изолированном атоме с номером (при = ), либо изменение энергии
электрона при его обобществлении двумя атомами с номерами и (при ),
S — интегралы перекрывания для базисных АО с номерами
и ,
— энергия МО с коэффициентами {С С … Сn }.

Основные проблемы метода МО связаны с необходимостью процедуры самосогласования, включающей многократные вычисления интегралов типа F и S
1.Метод Хюккеля — ПОЛУЭМПИРИЧЕСКИЙ, поскольку ни один из этих интегралов не вычисляется — они определяются на основании экспериментальных данных (спектральные, калориметрические и т.д.).
2. Fii = Fjj = (т.е. предполагается, что молекулы образованы
из одинаковых по природе атомов)
 С
С С С
С С С
С
3. Недиагональные интегралы Fij разделяются на два типа.
Первый тип относится к парам атомов, соединенных между собой химическими связями. Для таких пар атомов принимается следующее условие:
Fij = (резонансный интеграл).
Второй тип относится к парам атомов, которые не связаны между собой химически; для них
Fij = 0.
Разделение недиагональных интегралов Fij на два типа
(нулевые и ненулевые) осуществляется исключительно на химической основе — по химической структурной формуле
(т о п о л о г и ч е с к и е |
варианты метода МО). |
|||||
4. Приближение нулевого |
Sij |
= |
1 |
( i |
= |
j ) |
дифференциального |
0 |
( i |
≠ |
j ) |
||
перекрывания (НДП) |
|
|
|
|
|
|
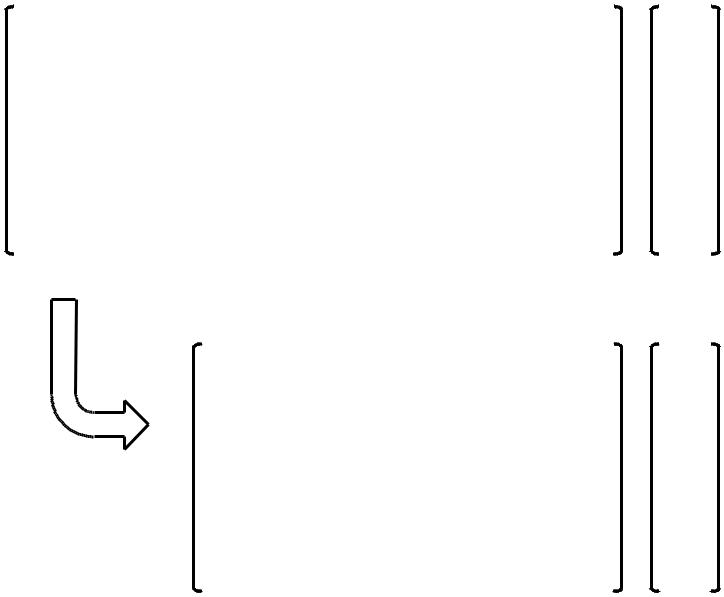
F – S |
F – S . . |
F n – S n |
С |
|
F – S |
F – S . . |
F n – S n |
С |
|
. . . . |
. . . |
. . |
• . |
|
. . . . |
. . . |
. . |
. |
|
Fn – Sn |
Fn – Sn . |
. Fnn – Snn |
Сn |
|
|
|
Уравнение Хартри-Фока-Рутана |
||
|
α – β . . |
0 |
С |
|
|
β |
α – . . . |
С |
|
|
. . . . . . |
• . |
||
|
. . . . . . |
. |
||
|
0 . . . |
. α – |
Сn |
|
=0
=0
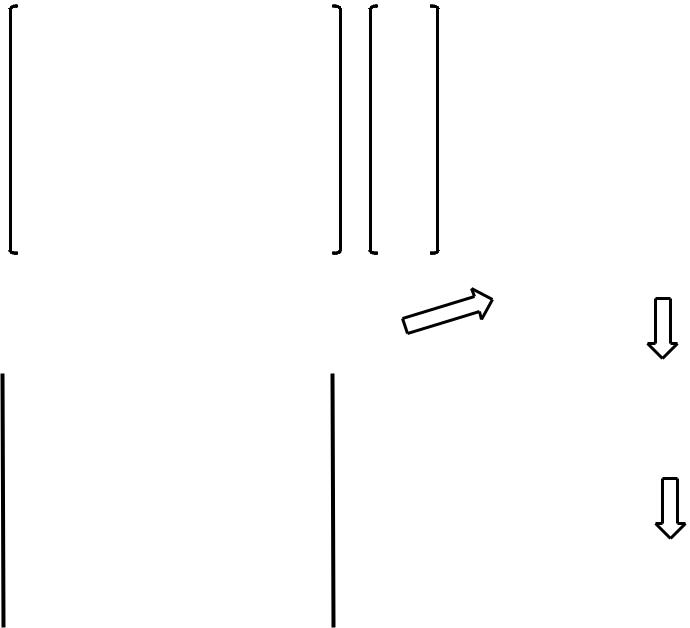
Уравнение Хюккеля
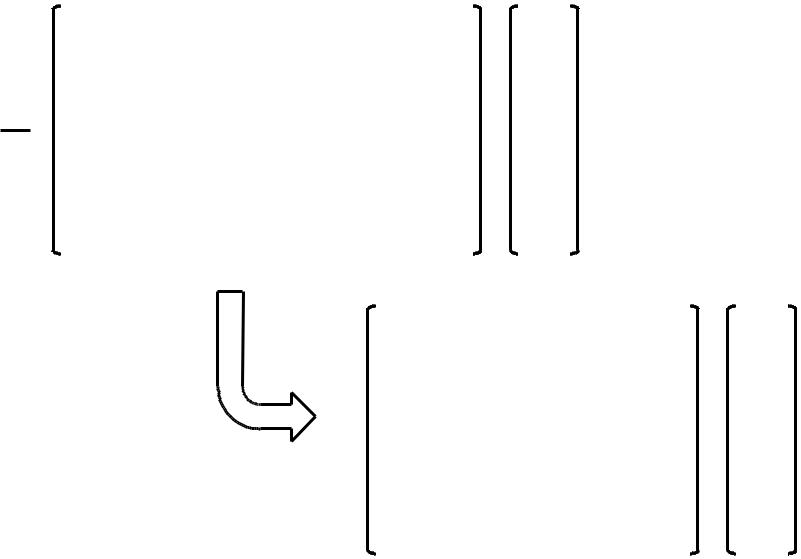
|
α – |
β . . |
0 |
С |
1 |
β |
α – . . . |
С |
|
|
|
|
• . = 0 |
|
β . . . . . . |
||||
|
. . . . . . |
. |
||
|
0 . |
. . |
. α – |
Сn |
|
Х |
1 . |
. |
0 |
С |
|
1 |
Х . . . |
С |
||
|
. . . . . |
• . = 0 |
|||
|
. . . . . |
. |
|||
α – ε |
0 |
. |
. |
. Х |
Сn |
Х = ——— |
|
|
|
|
|
β |
|
|
|
|
|
Х |
1 . |
. |
0 |
С |
1 |
Х . . . |
С |
||
. . . . . |
• . |
|||
. . . . . |
. |
|||
0 |
. . |
. |
Х |
Сn |
Условие разрешимости
Х |
1 . |
. |
0 |
1 |
Х . . . |
||
. |
. . |
. |
. = 0 |
. . . . . |
|||
0 |
. . |
. |
Х |
Уравнение
Хюккеля
= 0
Характеристическое
уравнение
Корни
{ X1, X2, … , Xn }
Энергии МО
εi = α – βXi
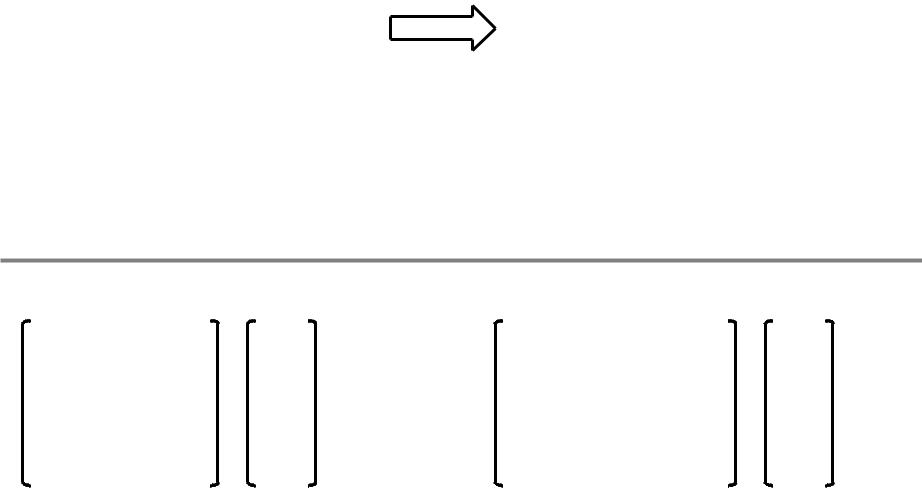
Гетероатомные молекулы в методе МОХ
—С—С—С—
С X
X = С + h CС
Х |
1 |
. 0 |
|
С |
|
1 |
Х . . |
|
С |
= 0 |
|
. . . . |
• |
. |
|||
0 |
. |
. Х |
|
Сn |
|
—С—Х—С—
CC CX
CХ = K CС
Х |
K . 0 |
|
С |
|
K |
Х+h . . |
|
С |
= 0 |
. . . . |
• |
. |
||
0 . . |
|
Сn |
|
|
Х |
|
|
|
|
