
Добавил:
Upload
Опубликованный материал нарушает ваши авторские права? Сообщите нам.
Вуз:
Предмет:
Файл:биочемистри1 / Lect6.ppt
X
- •Значения KM некоторых ферментов
- •Преобразования уравнения Михаэлиса - Ментен : двойной обратный график ( уравнение Lineweaver- Burk)
- •График Корниш-Боудена
- •ИНГИБИРОВАНИЕ ФЕРМЕНТОВ
- •I. НЕОБРАТИМОЕ ИНГИБИРОВАНИЕ
- •II. Обратимое ингибирование: конкурентное, неконкурентное, бесконкурентное, смешанное
- •1. КОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ
- •Сульфаниламиды – структурные аналоги п-аминобензойной кислоты
- •Кинетический тест для определения механизма ингибирования
- •2. БЕСКОНКУРЕНТНОЕ (UNCOMPETIVE) ИНГИБИРОВАНИЕ
- •Кинетический тест для определения механизма ингибирования
- •3. НЕКОНКУРЕНТНОЕ (NONCOMPETIVE) ИНГИБИРОВАНИЕ
- •3. НЕКОНКУРЕНТНОЕ (NONCOMPETIVE) ИНГИБИРОВАНИЕ
- •Кинетический тест для определения механизма ингибирования
- •ОСНОВНЫЕ СТРАТЕГИИ ФЕРМЕНТАТИВНОГО КАТАЛИЗА
- •Функции аминокислотных остатков в активном центре фермента
- •Сближение субстрата с активным центром фермента и его ориентация относительно каталитического центра
- •Общий кислотно-основной катализ
- •Аминокислотные остатки, участвующие в общем кислотно-основном катализе
- •Гексокиназа
- •Индуцированное соответствие в гексокиназе
- •Механизм действия лизоцима – пример общего кислотно-основного катализа
- •Пептидогликан
- •Лизоцим расщепляет связь между N-
- •Связывание гекса-N-ацетилглюкозамина с
- •Относительная скорость расщепления лизоцимом олигомеров N-ацетилглюкозамина
- •Структура части активного центра лизоцима
- •SN1-механизм
- •Стабильная форма интермедиата - полукресло
- •Водородные связи между субстратом и аминокислотными остатками в активном центре лизоцима
- •SN2-механизм
- •Ковалентный
- •Второй продукт
- •Химотрипсин – эндопептидаза
- •Гидролиз пептидной связи химотрипсином: ковалентный катализ
- •Схема активного центра химотрипсина
- •Модельная реакция: расщепление нитрофенилацетата
- •Последовательные этапы каталитического действия химотрипсина
- •1 стадия: образование фермент- субстратного комплекса
- •2 стадия: освобождение 1-го продукта
- •3 стадия: образование ацилфермента
- •4 стадия: связывание воды
- •5 стадия: деацилирование
- •6 стадия: образование свободного фермента
- •Катализ с участием ионов металлов
- •Структура активного центра енолазы
- •Механизм двуступенчатой реакции, катализируемой енолазой
- •Регуляция активности ферментов
- •Изменение конформации аллостерических ферментов при связывании модуляторов
- •Аспартат транскарбамоилаза
- •Регуляция по принципу обратной связи
- •Кинетика аллостерических ферментов
- •Эффект позитивных и негативных модуляторов
- •Примеры ковалентных модификаций ферментов
- •Регуляция активности фосфорилазы гликогена путем фосфорилирования
- •Протеолитическая активация пепсина
Регуляция активности ферментов
изменение активности фермента при его постоянной концентрации;
Связывание активаторов и ингибиторов: аллостерическая регуляцияОбратимая ковалентная модификация
Протеолитическая активация
изменение концентрации фермента, обычно в результате ускорения (индукции) или торможения (репрессии) синтеза фермента
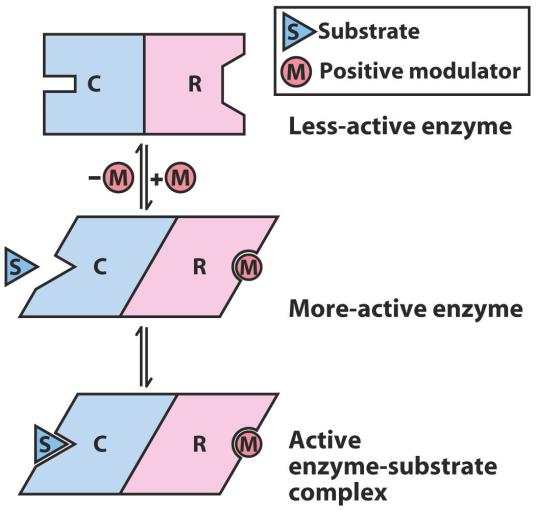
Изменение конформации аллостерических ферментов при связывании модуляторов

Аспартат транскарбамоилаза
(регуляторный фермент): мультисубъединичный

Регуляция по принципу обратной связи
Allosteric Enzyme
Allosteric modulator

Кинетика аллостерических ферментов
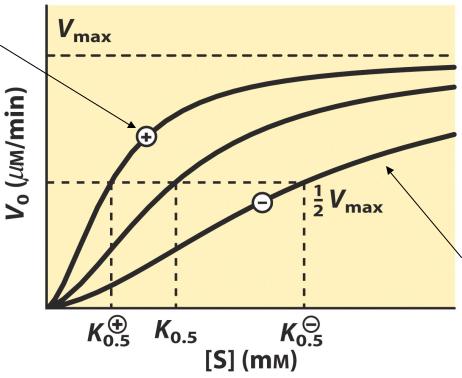
Эффект позитивных и негативных модуляторов
Positive modulator
Negative modulator
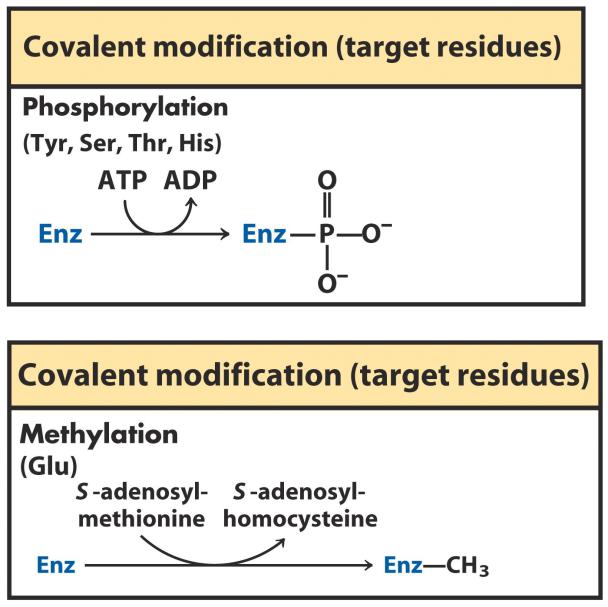
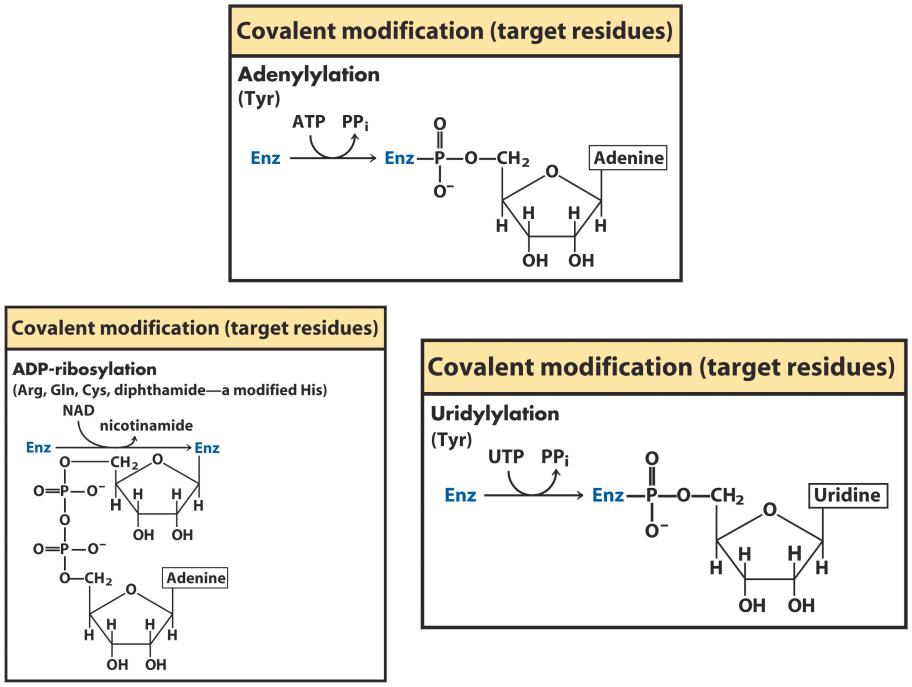
Примеры ковалентных модификаций ферментов
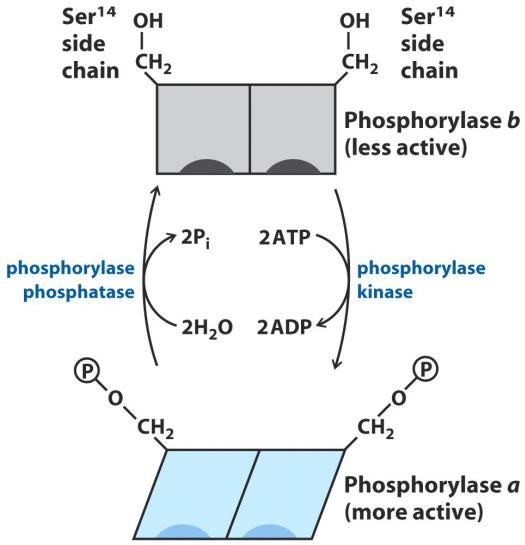
Регуляция активности фосфорилазы гликогена путем фосфорилирования
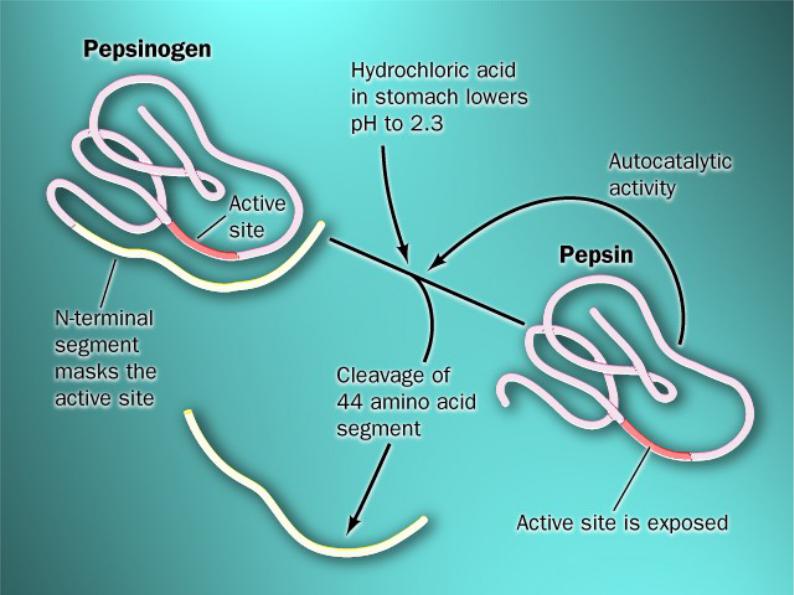
Протеолитическая активация пепсина
Соседние файлы в папке биочемистри1
