
Ф изика термодинамика бля лекции и вопросы / OF3_7_Realnye_gazy_mini_1
.pdf
Изотермы реального газа
© А.В. Бармасов, 2006-2013 |
21 |
12+ |
|

Теоретические и экспериментальные изотермы реального газа
© А.В. Бармасов, 2006-2013 |
22 |
12+ |
|
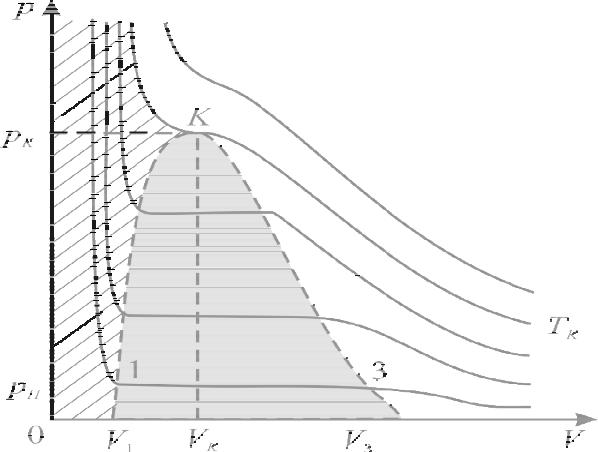
Семейство изотерм реального газа для нескольких температур
© А.В. Бармасов, 2006-2013 |
23 |
12+ |
|
Критическое состояние газа
(Gas critical state)
Критическое состояние – предельное состояние равновесия двухфазной системы, в котором обе сосуществующие фазы становятся тождественными по своим свойствам . На диаграммах состояния критическому состоянию соответствуют предельные точки на кривых равновесия фаз – критические точки. Значения параметров состояния системы, соответствующие критическим состояниям называют критическими – критическое давление, критическая температура и т.п.
С приближением к критическому состоянию различия в плотности, составе и других свойствах сосуществующих фаз, а также теплота фазового перехода и межфазное поверхностное натяжение уменьшаются и в критической точке эти различия равны нулю.
© А.В. Бармасов, 2006-2013 |
24 |
12+ |
|
Насыщенный пар
(Saturated vapour)
Опыт показывает, что при изотермическом сжатии реального газа до объёма V3, соответствующего на изотерме точке 3, газ начинает конденсироваться в жидкость.
При дальнейшем сжатии его давление перестаёт изменяться, и по мере уменьшения объёма всё бó льшая часть газа переходит в жидкое состояние. При сжатии газа до объёма V1 (точка 1) процесс конденсации газа заканчивается, и из газа получается жидкость. Последующее сжатие этой жидкости сопровождается значительным увеличением давления. Таким образом, участок 1-3 опытной изотермы соответствует сосуществованию жидкой и газообразной фаз.
Газ, находящийся в равновесии со своей жидкостью, называется насыщенным паром. Давление pН называется
давлением насыщенного пара при данной температуре.
© А.В. Бармасов, 2006-2013 |
25 |
12+ |
|
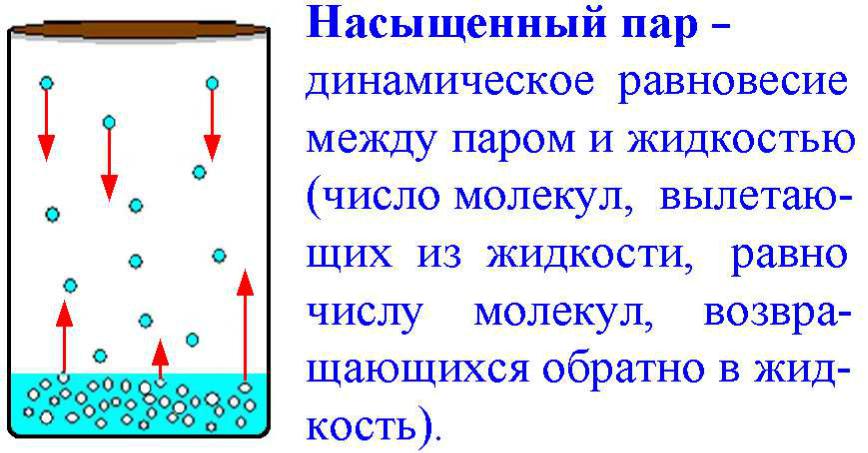
Насыщенный пар
(Saturated vapour)
© А.В. Бармасов, 2006-2013 |
26 |
12+ |
|
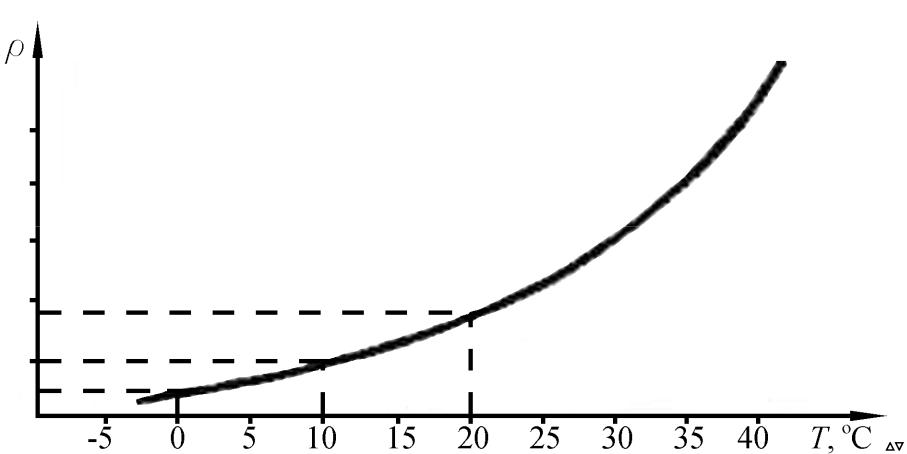
Зависимость плотности насыщенного пара от температуры
© А.В. Бармасов, 2006-2013 |
27 |
12+ |
|
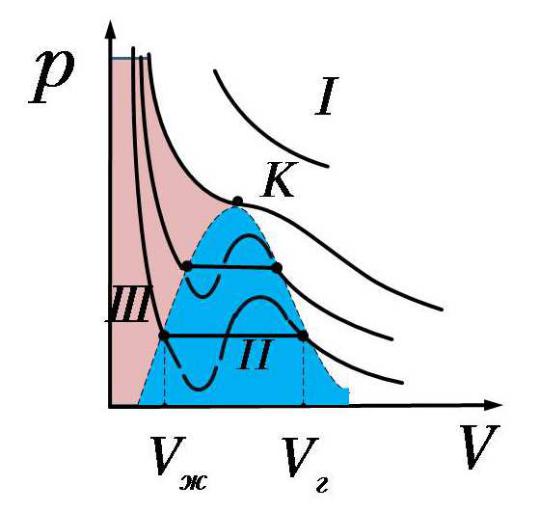
Изотермы Ван-дер-Ваальса
© А.В. Бармасов, 2006-2013 |
28 |
12+ |
|
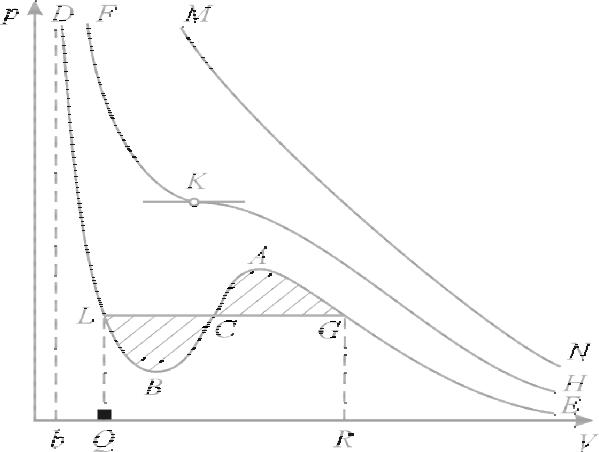
Изотермы Ван-дер-Ваальса
© А.В. Бармасов, 2006-2013 |
29 |
12+ |
|
Пересыщенный пар
(Supersaturated vapour)
При некоторых условиях можно опытным путём получить состояния, соответствующие участкам G-C и C-L изотермы Ван-дер-Ваальса. Это можно сделать, если тщательно очистить газ от включений и сжимать его до объёма, меньшего, чем объём насыщенного пара и, соответственно, до давления, большего, чем pН насыщенного пара при данной температуре T. Такой пар называется пересыщенным. Состояние пересыщенного пара, соответствующее участку G-C изотермы, является неустойчивым. Достаточно попасть в насыщенный пар капельке или пылинке, чтобы в нём началась конденсация пара в жидкость, сопровождающаяся падением давления до величины pН. Подобным же образом при изотермическом увеличении объёма сжатой жидкости на участке L-C возникает другое нестабильное состояние с давлением p < pН. Это состояние называют состоянием растянутой жидкости.
© А.В. Бармасов, 2006-2013 |
30 |
12+ |
|
