
General Physics - Thermodinamics archive / Молекулярная физика, 01-04
.pdfМинистерство образования РФ
Омский государственный университет
Кафедра общей физики
Методические указания к выполнению лабораторных работ
по курсу «Молекулярная физика и термодинамика».
Часть I.
Омск – 2004
Методические указания к выполнению лабораторных работ по курсу «Молекулярная физика и термодинамика», часть I, студентами физического и химического факультетов Омского государственного университета.
Исправленное и дополненное издание.
Переработано и дополнено: Г.И. Косенко, В.В. Михеев.
Омский госуниверситет. Омск, 2004.
Предлагаются методические указания к выполнению студентами физического и химического факультетов цикла из 4-х лабораторных работ по курсу «Молекулярная физика и термодинамика», часть I.
2
Работа №1. Определение влажности воздуха.
Цель работы: определение относительной и абсолютной влажности воздуха. Приборы и принадлежности: психрометр Ассмана, резиновая пипетка.
Водяной пар является одной из важных составных частей атмосферы. Его большее или меньшее количество в воздухе определяет влажность или сухость климата, условия жизни человека и произрастания растений, поглощая излучение земной поверхности и излучая тепло, водяной пар атмосферы повышает температуру ее нижних слоев и создает более теплый климат. Сгущение водяного пара дает начало облакам и осадкам – явлениям, от которых также зависит во многих отноше-
ниях хозяйственная деятельность человека. Конденсация и испарение сопровождаются выделением и поглощением большого количества тепла, и поэтому пар играет большую роль в энергетике атмосферы.
Знание свойств водяного пара, знакомство с процессами его превращения совершенно необходимо при рассмотрении всех динамических и термодинамических явлений в атмосфере, а также для прогноза погоды.
Характеристика водяного пара.
Парциальное давление водяного пара (упругость водяного пара). По закону Дальтона давление атмосферы составлено из суммы парциальных давлений газов и паров, входящих в состав атмосферы:
n |
|
pa pi , |
(1) |
i 1
где pa - атмосферное давление; pi - парциальное давление компонента смеси. Наблюдения показывают, что происходящие в атмосфере процессы очень часто близки к адиабатическим.
Если водяной пар далек от насыщения, то его состояние описывается уравнением Менделеева-Клайперона
P |
|
RT |
(2) |
|
|
||||
|
|
|
||
или |
|
|
|
|
P |
|
RT , |
(3) |
|
|
||||
|
|
|
где - парциальное давление пара (в СИ измеряется в паскалях - Па); ρ - плотность водяного пара; µ - молярная масса; T - температура по шкале Кельвина; R - универсальная газовая постоянная. Плотность водяного пара ρ носит название в метеороло-
гии абсолютной влажности.
Абсолютная влажность (парциальная плотность водяного пара) - масса водяного пара, заключенного в единице объема. В СИ единицей измерения абсолютной влажности является кг/м3. В природе имеет место переход ненасыщенных паров в насыщенные. Для последних парциальное давление Pн при данной температуре есть величина постоянная, а следовательно, постоянна и абсолютная влажность насыщенных паров ρн. Для этих величин составлены таблицы зависимости от температуры.
3

Эмпирически получена формула, описывающая зависимость парциального давления насыщенных паров от температуры в пределах от -20°С до +30°С:
7.6t
Pн 6.11·10242 t ,
где t - температура по шкале Цельсия.
Переход парциального давления насыщенных паров к плотности (парциальной) насыщенных паров по формуле (3) невозможен, если насыщенный пар недостаточно разрешен и есть сконденсированная из пара жидкость.
Величиной, показывающей насколько данный пар далек от насыщения, служит относительная влажность. Относительная влажность f - отношение парциального давления пара, имеющегося в воздухе при данной температуре к парциальному
давлению насыщенных паров при этой температуре, |
выраженное в процентах: |
||
f |
P |
100 %, |
(4) |
|
|||
|
Pн |
|
|
где величина Pн берется из таблицы для данной температуры.
На практике часто (с небольшой погрешностью для комнатных температур) принимают
f |
|
100 %, |
(5) |
||
|
|
||||
|
н |
||||
|
|
|
|||
Температура, при которой пар, имеющий данное парциальное давление, становится насыщенным, называется точкой росы.
Имеются и другие менее важные характеристики водяного пара в атмосфере. Решите предлагаемые уравнения, пользуясь таблицами 1, 2 и 3.
1.Определить по таблице 1 парциальное давление и плотность (абсолютную влажность) насыщенных паров при t=-2°C, t=°C, t=30°C.
2.Рассчитать парциальное давление водяного пара и его плотность, если при t=18°C, относительная влажность f= 25% (таблица 2).
Описание психрометра Ассмана.
Приборы, позволяющие измерять влажность воздуха, называются гигрометрами. Существуют четыре основных типа этих приборов: весовые, конденсационные, волосяные и психрометры.
Психрометр состоит из двух термометров: сухого (Сх) и влажного (смоченного) (Вл) (рис. 1).
4
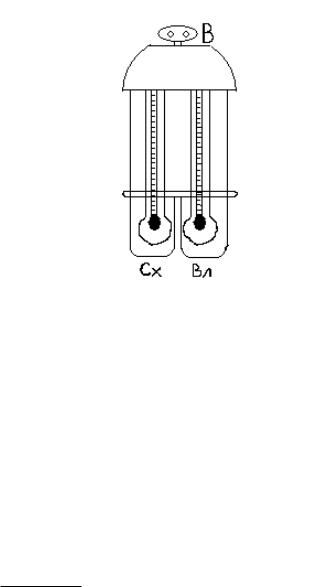
Рис.1.
Сухой термометр показывает температуру окружающего воздуха, а смоченный, теплоприемник которого обвязан влажным батистом - собственную температуру, зависящую от испарения, происходящего с поверхности его резервуара. Вследствие расхода тепла на испарение, показания смоченного термометра тем ниже, чем суше воздух, в котором измеряется влажность. При установившемся режиме испарения, когда температура мокрого термометра установится, приток тепла Q1 извне равен расходу тепла Q2 на испарение воды с поверхности термометра.
По закону Ньютона на единицу времени имеем
Q1=a t S1,
где t=tСх - tВл - наибольшая разность температур, S2 - поверхность мокрой части термометра, a - коэффициент пропорциональности.
По закону Дальтона испарение в единицу времени определяется выражением
M CS2 (Pн P) ,
Pатм
где M - масса испарившейся воды, S2 - площадь испаряющей поверхности, Pатм - давление воздуха, Pн – упругость насыщающего водяного пара при температуре испаряющейся жидкости, P – упругость водяного пара, находящегося в воздухе, C - коэффициент пропорциональности, зависящий от скорости потока воздуха.
Теперь легко получить количество тепла
Q2 M |
CS |
2 (Pн |
P) |
, |
|
|
Pатм |
|
|||
|
|
|
|
|
|
где τ - удельная теплота испарения воды. |
|||||
При условии Q1=Q2, S1=S2 получаем |
|
||||
a tS1 |
CS2 (Pн |
P) |
. |
|
|
|
Pатм |
|
|
||
|
|
|
|
|
|
И для влажности воздуха P получаем: |
|
||||
P Pн A(t t1 )Pатм , |
|
|
|
|
(6) |
где A=a/τC - постоянная прибора. Для стандартного аспирационного психрометра A=0.000662. По формуле (6) рассчитываются психометрические таблицы, что способствует оперативному определению влажности воздуха.
5
Порядок выполнения работы.
1.Изучить устройство аспирационного психрометра.
2.Смочить батист при помощи резиновой пипетки, наполненной дистиллированной водой, для чего легким нажимом пипетки поднять воду в пипетке примерно на один сантиметр, закрыть пипетку и очень осторожно ввести пипетку в трубку для смачивания батиста, затем открыть зажим пипетки для опускания воды в грушу.
3.Ключом завести вентилятор (В) (5-6 оборотов) и следить за показаниями термометров.
4.Снять показания термометров, когда они установятся (через 4-5 мин ). (Вентилятор включен!).
5.Используя таблицы 1 и 2, определить относительную, абсолютную влажность воздуха.
Контрольные вопросы.
1.Дать определение величин: упругость водяного пара, относительная и абсолютная влажность, точка росы.
2.Каковы устройство и принцип действия психрометра?
3.Продемонстрируйте умение пользоваться таблицами и определять по ним
4.абсолютную влажность воздуха, относительную влажность.
Литература.
1. Усольцев В.А. Измерение влажности воздуха. Л.: 1959.
6
Таблица 1.
Давление насыщающих водяных паров (мм рт.ст.) и их масса (г/м3 или 10-3 кг/м3).
Температура |
Давление |
Масса |
Температура |
Давление |
Масса |
|
|
|
|
|
|
-10 |
1.95 |
2.14 |
10 |
9.2 |
9.4 |
-9 |
2.13 |
2.33 |
11 |
9.8 |
10.0 |
-8 |
2.32 |
2.54 |
12 |
10.5 |
10.7 |
-7 |
2.53 |
2.76 |
13 |
11.2 |
11.4 |
-6 |
2.76 |
2.99 |
14 |
12.0 |
12.1 |
-5 |
3.03 |
3.24 |
15 |
12.8 |
12.8 |
-4 |
3.28 |
3.51 |
16 |
13.6 |
13.6 |
-3 |
3.57 |
3.81 |
17 |
14.5 |
14.5 |
-2 |
3.88 |
4.13 |
18 |
15.5 |
15.4 |
-1 |
4.22 |
4.47 |
19 |
16.5 |
16.3 |
0 |
4.58 |
4.84 |
20 |
17.5 |
17.3 |
1 |
4.9 |
5.2 |
21 |
18.7 |
18.3 |
2 |
5.3 |
5.6 |
22 |
19.8 |
19.4 |
3 |
5.7 |
6.0 |
23 |
21.1 |
20.6 |
4 |
6.1 |
6.4 |
24 |
22.4 |
21.8 |
5 |
6.6 |
6.8 |
25 |
23.8 |
23.0 |
6 |
7.0 |
7.3 |
26 |
25.2 |
24.4 |
7 |
7.5 |
7.8 |
27 |
26.7 |
25.8 |
8 |
8.0 |
8.8 |
28 |
28.4 |
27.2 |
9 |
8.6 |
8.8 |
29 |
30.0 |
28.7 |
|
|
|
30 |
31.8 |
|
Примечание 1 мм рт.ст. = 133 Па.
7

Таблица 2.
Упругость насыщающего пара воды.
Упругость пара, мм. рт. ст.
°С |
0.0° |
0.1° |
0.2° |
0.3° |
0.4° |
0.5° |
0.6° |
0.7° |
0.8° |
0.9° |
5 |
6.54 |
6.59 |
6.64 |
6.68 |
6.73 |
6.78 |
6.82 |
6.87 |
6.92 |
6.97 |
6 |
7.01 |
7.06 |
7.11 |
7.16 |
7.21 |
7.26 |
7.31 |
7.36 |
7.41 |
7.46 |
7 |
7.51 |
7.57 |
7.62 |
7.67 |
7.72 |
7.78 |
7.83 |
7.88 |
7.94 |
7.99 |
8 |
8.05 |
8.10 |
8.16 |
8.21 |
8.27 |
8.32 |
8.38 |
8.44 |
8.50 |
8.55 |
9 |
8.61 |
8.67 |
8.73 |
8.79 |
8.85 |
8.91 |
8.97 |
9.03 |
9.09 |
9.15 |
10 |
9.21 |
9.27 |
9.33 |
9.40 |
9.46 |
9.52 |
9.59 |
9.65 |
9.72 |
9.78 |
9 |
9.85 |
9.91 |
9.98 |
10.04 |
10.11 |
10.18 |
10.25 |
10.31 |
10.38 |
10.45 |
10 |
10.52 |
10.59 |
10.66 |
10.73 |
10.80 |
10.87 |
10.94 |
11.02 |
11.09 |
11.16 |
13 |
11.23 |
11.31 |
11.38 |
11.46 |
11.53 |
11.61 |
11.68 |
11.76 |
11.84 |
11.91 |
14 |
11.99 |
12.07 |
12.15 |
12.23 |
12.30 |
12.38 |
12.46 |
12.55 |
12.63 |
12.71 |
15 |
12.79 |
12.87 |
12.96 |
13.04 |
13.12 |
13.21 |
13.29 |
13.38 |
13.46 |
13.55 |
16 |
13.64 |
13.72 |
13.81 |
13.90 |
13.99 |
14.08 |
14.17 |
14.26 |
14.35 |
14.44 |
17 |
14.53 |
14.63 |
14.72 |
14.81 |
14.91 |
15.00 |
15.10 |
15.19 |
15.29 |
15.38 |
18 |
15.48 |
15.58 |
15.68 |
15.78 |
15.87 |
15.97 |
16.07 |
16.18 |
16.28 |
16.38 |
19 |
16.48 |
16.59 |
16.69 |
16.79 |
16.90 |
17.00 |
17.11 |
17.22 |
17.32 |
17.43 |
20 |
17.54 |
17.65 |
17.76 |
17.87 |
17.98 |
18.09 |
18.20 |
18.31 |
18.43 |
18.54 |
21 |
18.66 |
18.77 |
18.89 |
19.00 |
19.12 |
19.24 |
19.35 |
19.47 |
19.59 |
19.71 |
22 |
19.83 |
19.95 |
20.08 |
20.20 |
20.32 |
20.45 |
20.57 |
20.70 |
20.82 |
20.95 |
23 |
21.07 |
21.20 |
21.33 |
21.46 |
21.59 |
21.72 |
21.85 |
21.98 |
22.12 |
22.25 |
24 |
22.38 |
22.52 |
22.65 |
22.79 |
22.93 |
23.07 |
23.20 |
23.34 |
23.48 |
23.62 |
25 |
23.76 |
23.91 |
24.05 |
24.19 |
24.34 |
24.48 |
24.63 |
24.77 |
24.92 |
25.07 |
8
Таблица 3. Психрометрическая таблица.
Показания |
|
Разность показаний сухого и влажного термометра, °С |
|
|||||||||||
сухого |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
1 |
2 |
3 |
|
4 |
5 |
6 |
7 |
|
8 |
9 |
10 |
11 |
|
термомет- |
|
|
||||||||||||
|
|
|
|
Относительная влажность |
|
|
|
|
||||||
ра,°С |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
100 |
81 |
63 |
45 |
|
28 |
11 |
|
|
|
|
|
|
|
1 |
100 |
83 |
65 |
48 |
|
32 |
16 |
|
|
|
|
|
|
|
2 |
100 |
84 |
68 |
51 |
|
35 |
20 |
|
|
|
|
|
|
|
3 |
100 |
84 |
69 |
54 |
|
39 |
24 |
10 |
|
|
|
|
|
|
4 |
100 |
85 |
70 |
56 |
|
42 |
28 |
14 |
|
|
|
|
|
|
5 |
100 |
86 |
72 |
58 |
|
45 |
32 |
19 |
6 |
|
|
|
|
|
6 |
100 |
86 |
73 |
60 |
|
47 |
35 |
23 |
10 |
|
|
|
|
|
7 |
100 |
87 |
74 |
61 |
|
49 |
37 |
26 |
14 |
|
|
|
|
|
8 |
100 |
87 |
75 |
63 |
|
51 |
40 |
29 |
18 |
|
7 |
|
|
|
9 |
100 |
88 |
76 |
64 |
|
53 |
42 |
31 |
21 |
|
11 |
|
|
|
10 |
100 |
88 |
76 |
65 |
|
54 |
44 |
34 |
24 |
|
14 |
5 |
|
|
11 |
100 |
88 |
77 |
66 |
|
56 |
46 |
36 |
26 |
|
17 |
8 |
|
|
12 |
100 |
89 |
78 |
68 |
|
57 |
48 |
38 |
29 |
|
20 |
11 |
|
|
13 |
100 |
89 |
79 |
69 |
|
59 |
49 |
40 |
31 |
|
23 |
14 |
6 |
|
14 |
100 |
89 |
79 |
70 |
|
60 |
51 |
42 |
34 |
|
25 |
17 |
9 |
|
15 |
100 |
90 |
80 |
71 |
|
61 |
52 |
44 |
36 |
|
27 |
20 |
12 |
5 |
16 |
100 |
90 |
81 |
71 |
|
62 |
54 |
46 |
37 |
|
30 |
22 |
15 |
8 |
17 |
100 |
90 |
81 |
72 |
|
64 |
55 |
47 |
39 |
|
32 |
24 |
17 |
10 |
18 |
100 |
91 |
82 |
73 |
|
65 |
56 |
49 |
41 |
|
34 |
27 |
20 |
13 |
19 |
100 |
91 |
82 |
74 |
|
65 |
58 |
50 |
43 |
|
35 |
29 |
22 |
15 |
20 |
100 |
91 |
83 |
74 |
|
66 |
59 |
51 |
44 |
|
37 |
30 |
24 |
18 |
21 |
100 |
91 |
83 |
75 |
|
67 |
60 |
52 |
46 |
|
39 |
32 |
26 |
20 |
22 |
100 |
92 |
83 |
76 |
|
68 |
61 |
54 |
47 |
|
40 |
34 |
28 |
22 |
23 |
100 |
92 |
84 |
76 |
|
69 |
61 |
55 |
48 |
|
42 |
36 |
30 |
24 |
24 |
100 |
92 |
84 |
77 |
|
69 |
62 |
56 |
49 |
|
43 |
37 |
31 |
26 |
25 |
100 |
92 |
84 |
77 |
|
70 |
63 |
57 |
50 |
|
44 |
38 |
33 |
27 |
26 |
100 |
92 |
85 |
78 |
|
71 |
64 |
58 |
51 |
|
46 |
40 |
34 |
29 |
27 |
100 |
92 |
85 |
78 |
|
71 |
65 |
59 |
52 |
|
47 |
41 |
36 |
30 |
28 |
|
93 |
85 |
78 |
|
72 |
65 |
59 |
53 |
|
47 |
42 |
37 |
32 |
29 |
|
93 |
86 |
79 |
|
72 |
66 |
60 |
54 |
|
48 |
43 |
38 |
33 |
30 |
|
93 |
86 |
79 |
|
73 |
67 |
61 |
55 |
|
50 |
44 |
39 |
34 |
9

Работа №2.
Определение коэффициента поверхностного натяжения и исследование его температурной зависимости.
Цель работы: изучение явления поверхностного натяжения.
Приборы и принадлежности: аналитические весы, разновес, большой и малый химические стаканы, термометр, прибор Ребиндера, дистиллированная вода.
На молекулу жидкости действуют силы притяжения со стороны окружающих молекул. Если молекула находится внутри жидкости и удалена от ее поверхности на расстояние, превышающее радиус молекулярного действия, то эти в среднем уравновешиваются. Если же молекула находится в приграничном слое, толщина которого равна, радиусу сферы молекулярного действия, то появляется результирующая сила направленная внутрь жидкости. Для увеличения поверхности жидкости, т.е. для вывода молекул на поверхность, нужно совершить работу против этой силы. Работа, которую надо затратить, чтобы изотермически и квазистатически увеличить поверхность жидкости на единицу при сохранении ее объема неизменным, называется поверхностным натяжением жидкости.
Взаимное притяжение между молекулами поверхностного слоя вызывает появление в нѐм силы поверхностного натяжения, направленной по касательной к поверхности и перпендикулярной к контуру, ограничивающую эту поверхность. Сила F, обусловленная взаимодействием молекул жидкости, вызывающая сокращение площади еѐ свободной поверхности и направленная по касательной к этой поверхности, называется силой поверхностного натяжения. F– пропорциональна длине границы свободной поверхности жидкости l :
F l , отсюда Fl ,
где σкоэффициент поверхностного натяжения, численно равный силе поверхностного натяжения, действующей на единицу длины границы свободной поверхности жидкости. Таким образом, поверхностное натяжение можно также определить как свободную поверхностную энергию жидкости, приходящуюся на единицу ее поверхности.
В системе СИ коэффициент поверхностного натяжения измеряется Н/м. Опыт показал, что на величину σ влияет среда, находящаяся над поверхностью жидкости, и температура жидкости.
Задание 1. Определение коэффициента поверхностного натяжения методом отрыва капель жидкости.
Если поместить исследуемую жидкость в тонкую вертикально расположенную трубку и заставить ее медленно по каплям вытекать, то поверхностная пленка жидкости, образующаяся в отверстии трубки, будет оказывать сопротивление вытеканию жидкости. Под давлением вышележащих слоев пленка растягивается, и жидкость, собирается в каплю на конце трубки. В некоторый момент сила тяжести превысит силу поверхностного натяжения пленки, поддерживающей каплю, и капля оторвется. Перед отрывом у конца трубки образуется перетяжка, по которой капля отрывается. Длина контура, по которому разрывается поверхностная пленка, равна 2 R, где Rрадиус перетяжки (рис.1).
10
