
- •1.Гетероциклды қосылыстарға түсінік беріңіз. Гетероциклды қосылыстардың тәжірибелік мәнділігіне мысал келтіріңіз
- •2.Гетероциклды қосылыстардың негізгі принципті заманауи номенклатурасын атаңыз.
- •6. Азиридин синтезіне мысал келтіріңіздер. Өндірісте қолданылатын негізгі әдістерін көрсетіңіз.
- •9.Оксетан синтезіне мысал келтіріңіз, өндірісте қолданылатын негізгі әдістерін көрсетіңіз.
- •10. Азетидин синтезіне мысал.Өндірісте қолд.Әдісі
- •11.Тиетан синтезіне мысал келтіріңіз, өндірісте қолданылатын негізгі әдістерін көрсетіңіз.
- •12. 5 Мүшелі гетероциклдың жалпы синтез әдістерін мысалға келтіріңіз.
- •13. Фуран синтезі.
- •16. Конденсирленген 5 мүшелі гетероциклдың алыну жолдарын көрсетіңіз. Олардың өндірістік тиімділігін көрсетіңіз.
- •17.Фуранның алыну кезіндегі гетероциклдеу принциптерін көрсетіңіз.
- •20.Индол алыну кезіндегі гетероциклдеу принципі.
- •23. Оксиранды алудың әдістері. Оксиран синтезі:
- •25. Бензол және хинолиннің ұқсас реакциялық қабілеттілігін табыңыз. Өндірістік хинолинді алудағы реагенттер жинағына критикалық баға беріңіз.
- •26. Өндірістік фуран, тиофен, пирролды алудағы реагенттер
- •29. Окси- және аминопиридиндерді алу әдістерін іріктеңіз.
- •30. Хинолин мен изохинолин реак.Қабілеттілігі.Түсіндір
25. Бензол және хинолиннің ұқсас реакциялық қабілеттілігін табыңыз. Өндірістік хинолинді алудағы реагенттер жинағына критикалық баға беріңіз.
Хинолин құрамында гетероатомы бар (азот) гетероциклді органикалық қосылыс. Хинолин мен бензолдың көптеген реакциялары өте ұқсас болып келеді.
Электрофильді орынбасу реакциялары:
Нитрленуі.
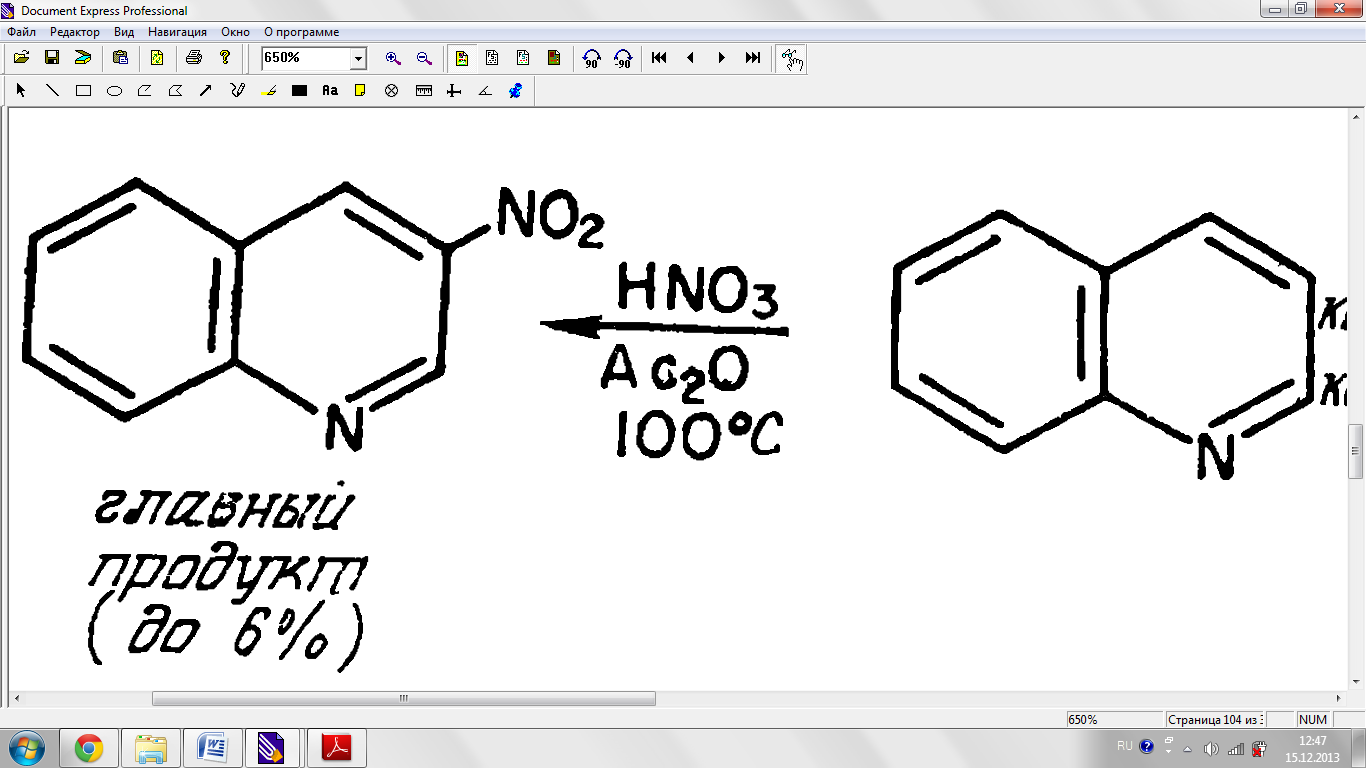
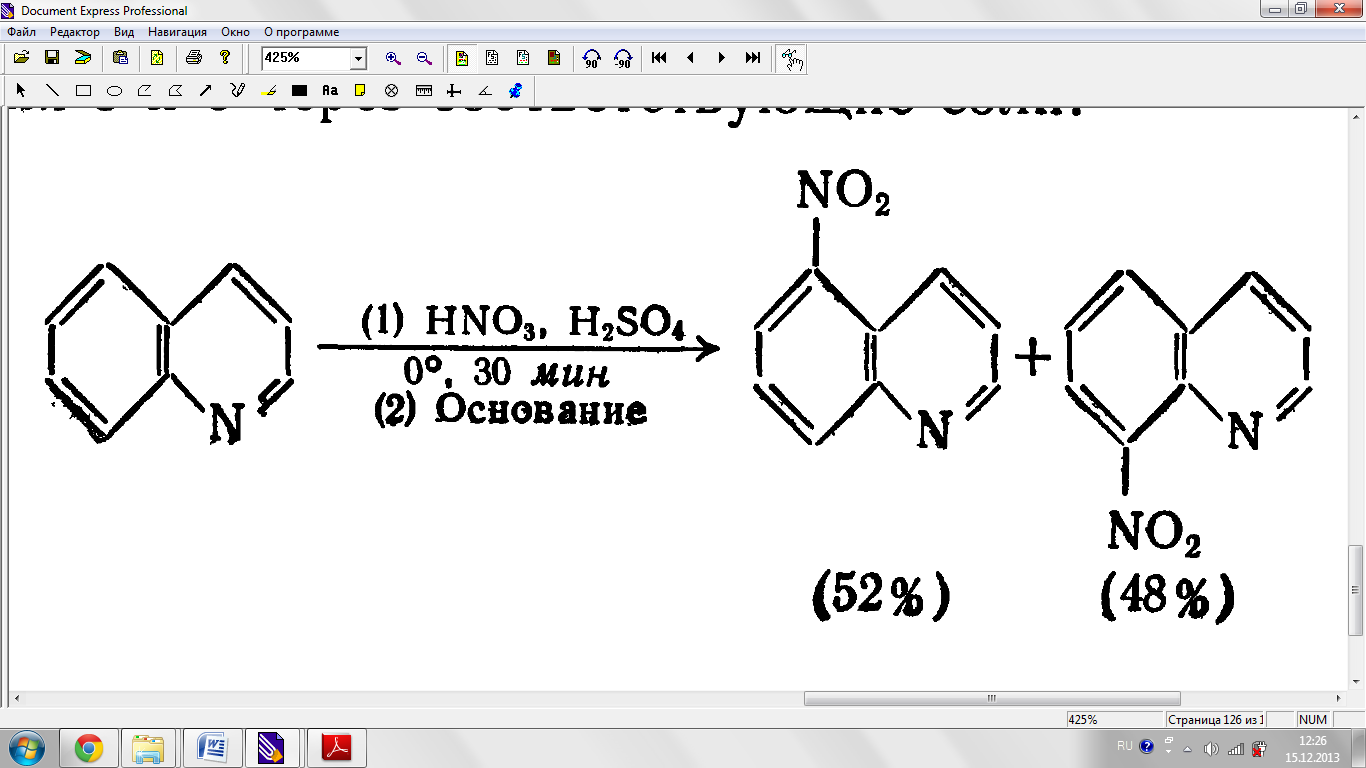
Сульфирленуі.


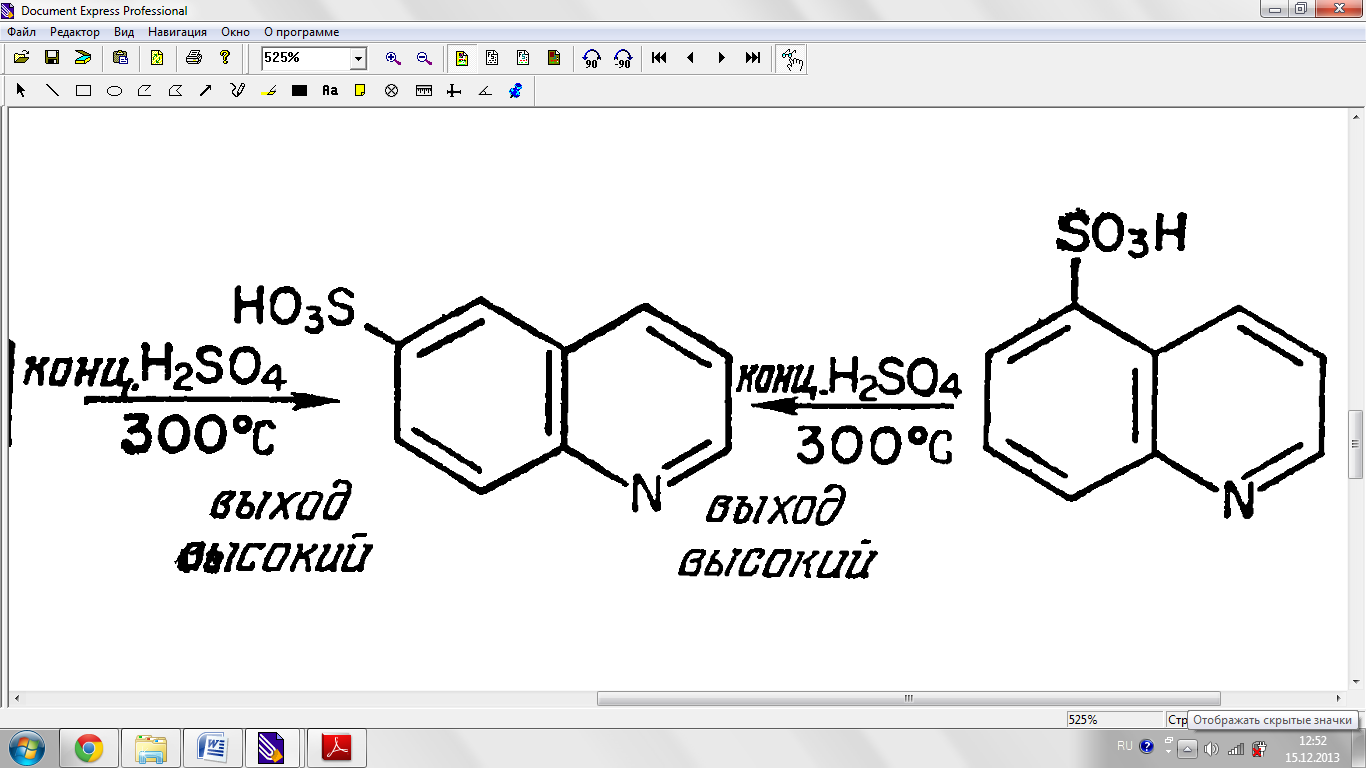
Галогенденуі.

Тотығу реакциялары.

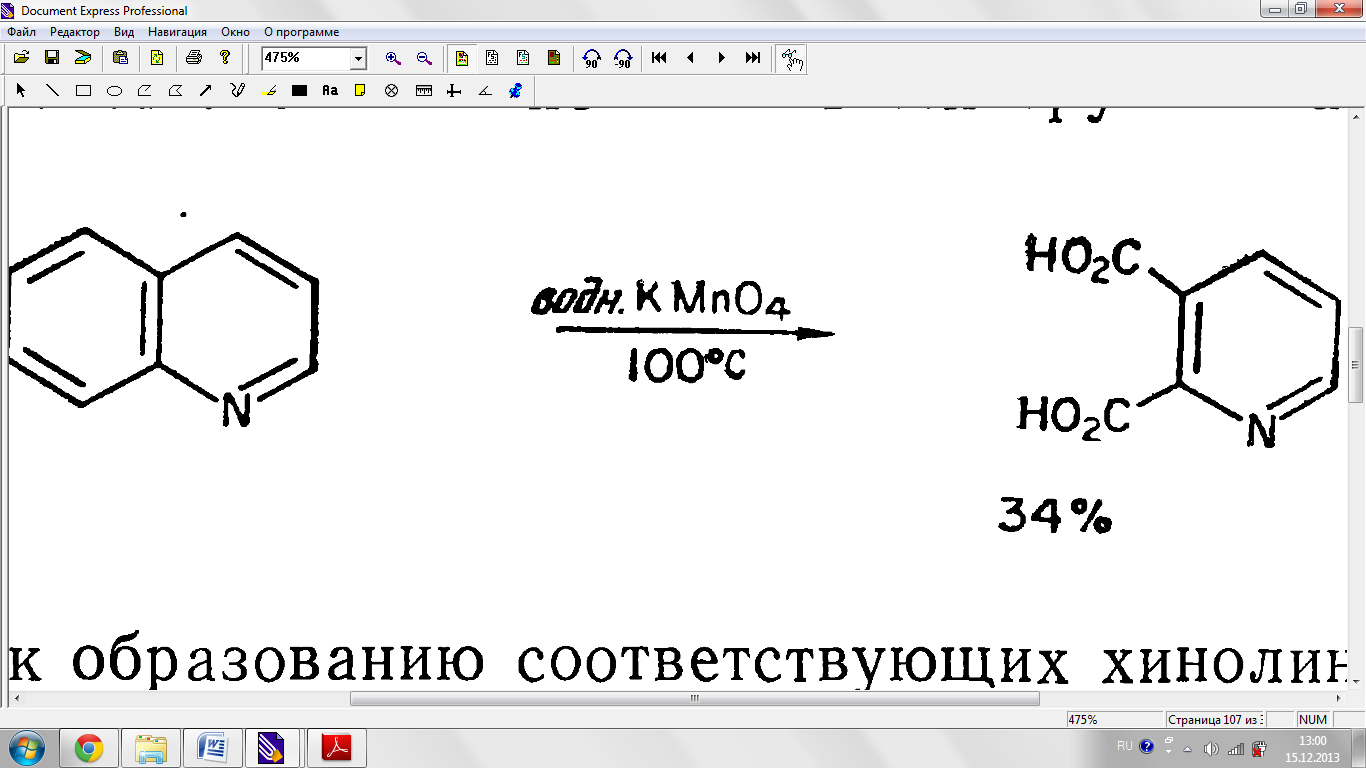
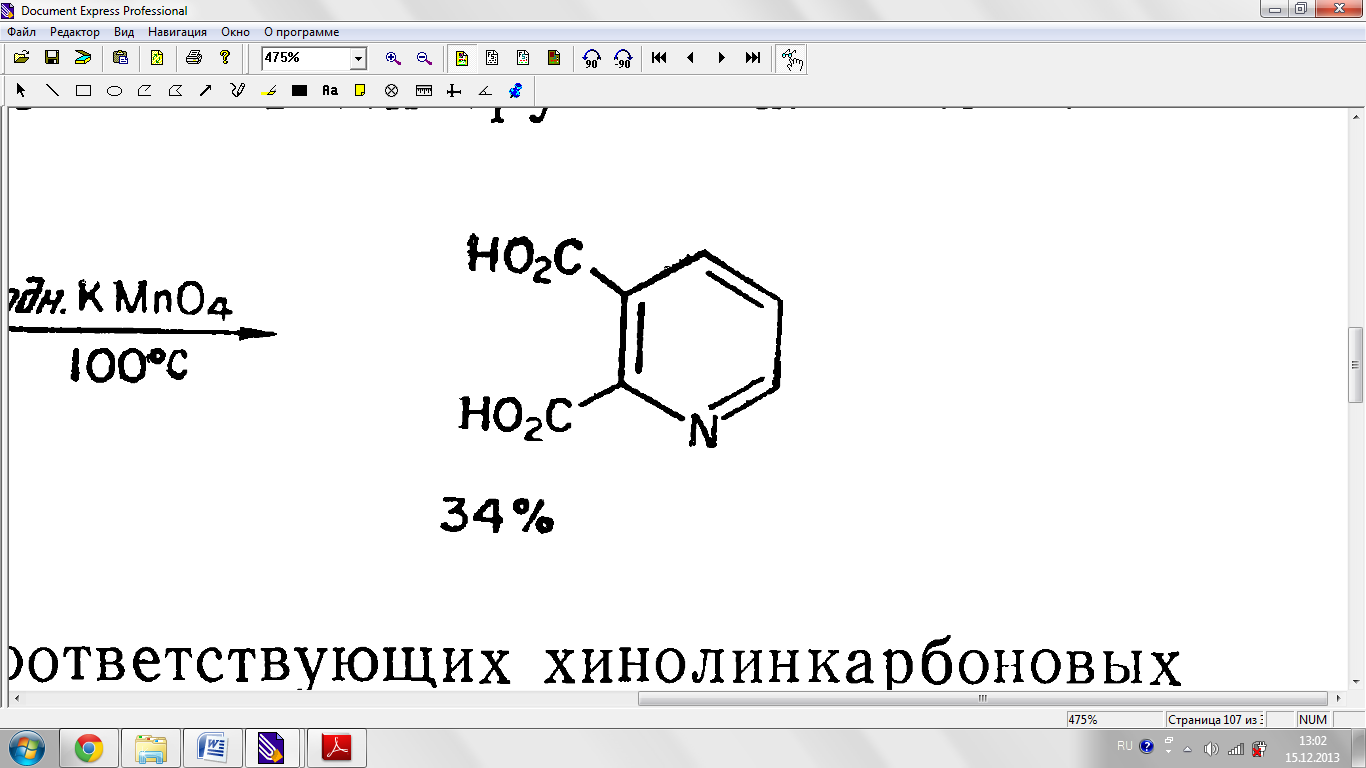
Радикалды орынбасу реакциялары.

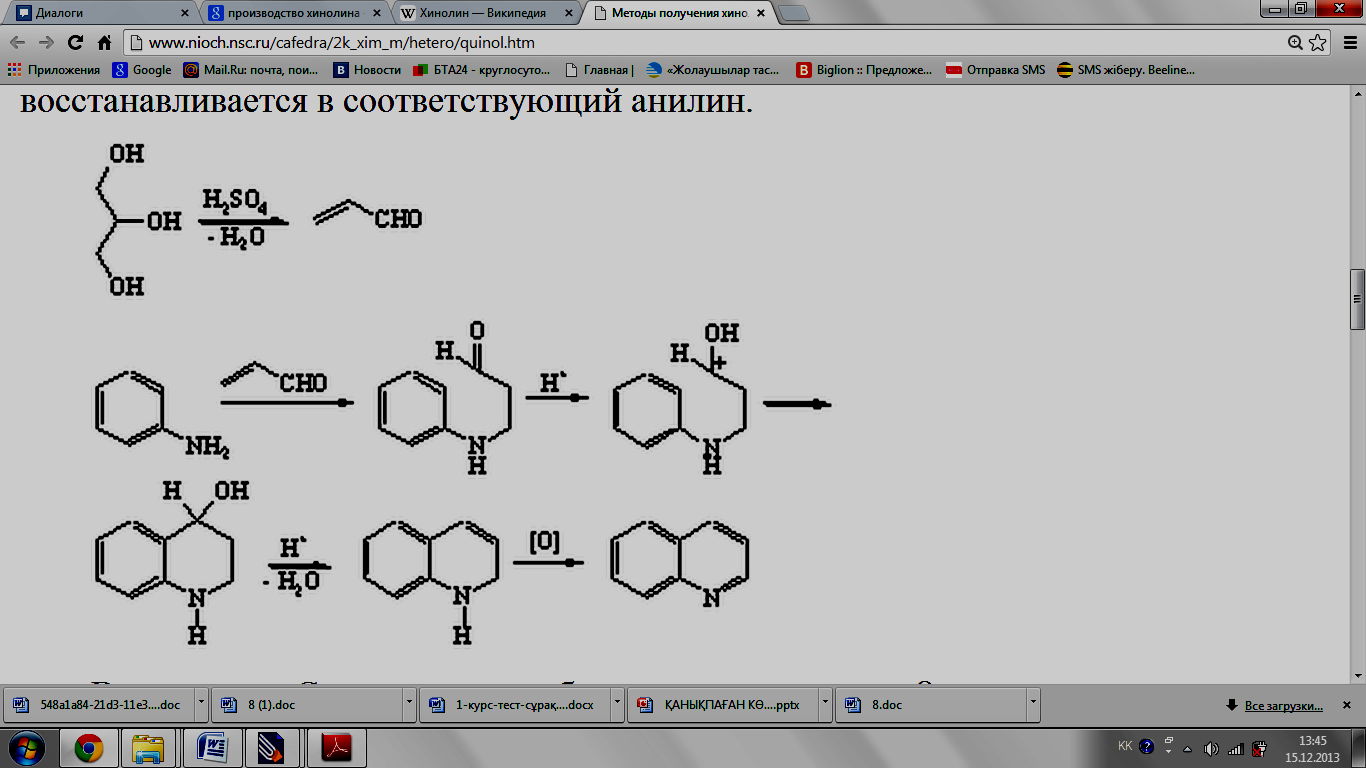
Өндірісте хинолин алудың ең тиімді әдісі Скрауп әдісі бойынша алу. Бұл әдіспен жүретін реакцияның өзі 3 сатыдан тұрады:
1. глицерин күкірт қышқылы әсерінен акролеинге дейін дегидраттанады.
2. анилиннің акролеинге қосылу реакциясы жүреді.
3. дегидратация реакциясы.
26. Өндірістік фуран, тиофен, пирролды алудағы реагенттер
жинағына критикалық баға беріңіз. Оларды электрофильді реагенттермен реакцияға түсу қабілетін салыстырыңыз.
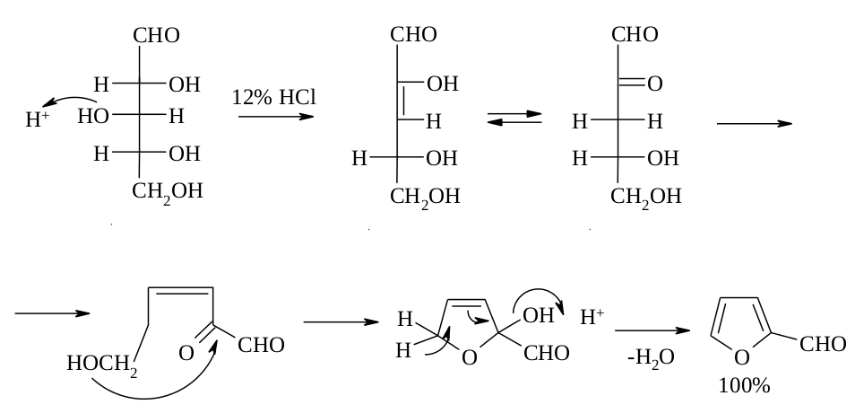
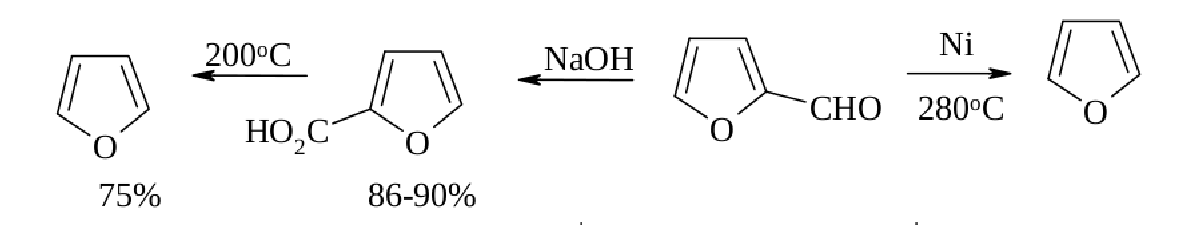
Өндірісте Фуранда алу үшін алдымен фурфуролды алады. Содан соң, фурфуролды Каннициаро реакциясы бойынша пирослизді қышқылдылығын арттырады, содан соң алынған қышқылды 200-250оС температурада қыздырып фуранға декарбоксилдейді. Ал, фурфуролдың өзі де 400оС температурада мырыш хроматы катализаторының қатысында фуранға айнала алады:
2.
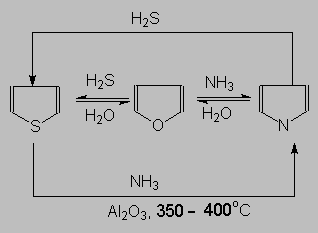
1. Фуран және оның туындыларын 1,4- дикарбонилді қосылыстардан алуға болады. Ол әдіс Пааль-Кнорр синтезі деп аталынады. Яғни, фуранның туындылары 1,4- дикетондарға Р2О5, ZnCl2, H2SO4- термен әсер еткенде түзіледі:
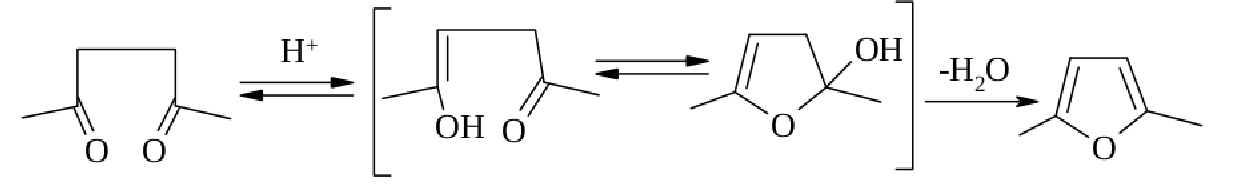
Электрофильді агенттермен реакциясы. Протонирлеу. Фуранның өзі және де алкилфурандар минералды қышқылдардың әсеріне тұрақты болып келеді. С-протонирлеу (1) және (2) катиондарының түзілуіне әкеледі

Алкилді
топтардың болуы, орынбасу, сонымен
қатар, 3-метилфуранды екінші жағдайға
дейтерлеу реакциясы кезінде әсер
етеді: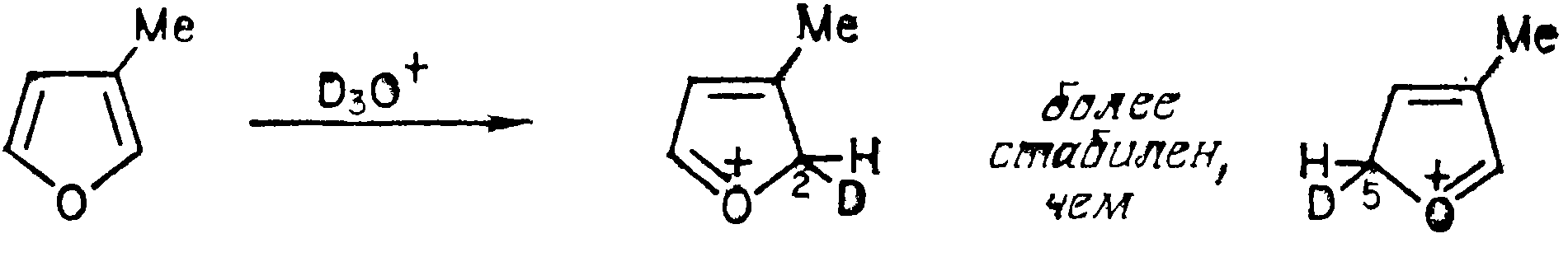 Нитрлеу:
Нитрлеу:
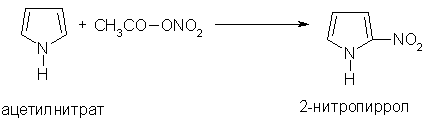
Сулфирлеу:
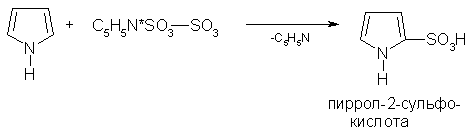
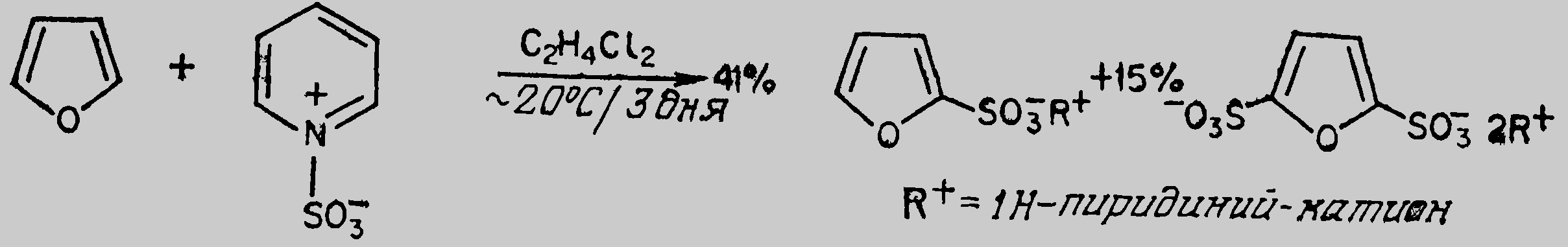
27.Азолдардың реакциялық қабілеттілігін салыстырыңыз. Нуклефильді және электрофильді реакциялардағы айырмашылықтары.
Азолдар – ароматик сипаттас,құрамында бір не одан да көп азот атомдары бар. Оларға: тиазол, имидазол, үшазол. Тетразол және т.б. жатады.
Егер фуран, тиофен не пиррол формулаларындағы СН топты азот атомымен айырбастасақ, біз азолдардың ең басты өнімдерінің формулаларын аламыз.
Фуранға екі қоосылыс сәйкес келеді: оксазол және изоксазол:
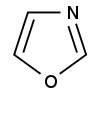
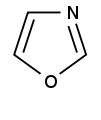
Тиофенге тиазол мен изотиазол сәйкес келеді:
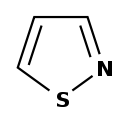
Пирролға диазолдар сәйкес келеді: пиразол мен имидазол:
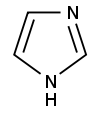
Химиялық қасиеттері
Электрофильді реакциялар:
Азол күшті қышқылдар үшін неігздік қасиет танытады. Азолдар қатарында электрофильді орын басу реак-на бейімділік оңнан солға қарай кемиді:
Имидазол›тиазол › оксазол
Галогендермен әрекеттесуі:
Имидазолдар катализатор қатысынсыз-ақ бромдалады:
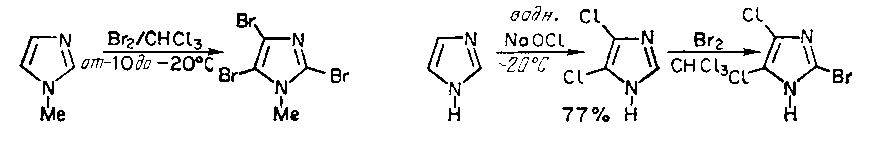
Тиазол бұл жайдайда броммен әрекеттеспейді.
Азолдардың ішінде имидазол сутекті оңай нитротопшаға алмастырады. Пиразол үшін де бұл реак-я жеңіл өтеді, ал тиазол олеум қатысында 160С тем-да әрекеттеспейді.
Егер тиазол сақинасына метил топшаны ендірсе, онда бұл зат оңай нитроқосылыс береді:
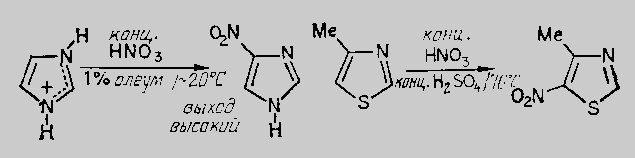

Имидазол – сульфотопшаны тиазолға қарағанда жеңіл қосып алады:
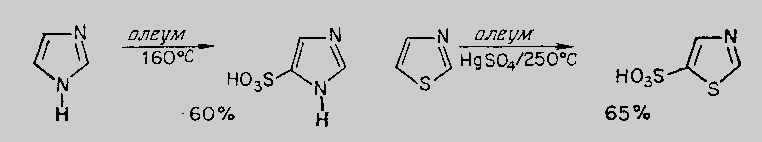
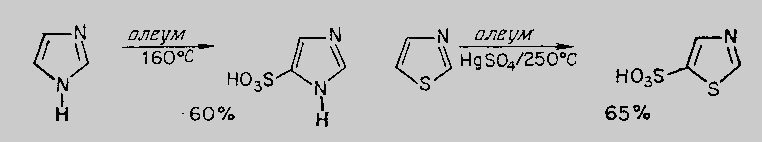
Нуклеофильді орын басу
Гидридты орын басу. Мұндай типті реакция тек біреу, ол – тиазолдың аминделуі.
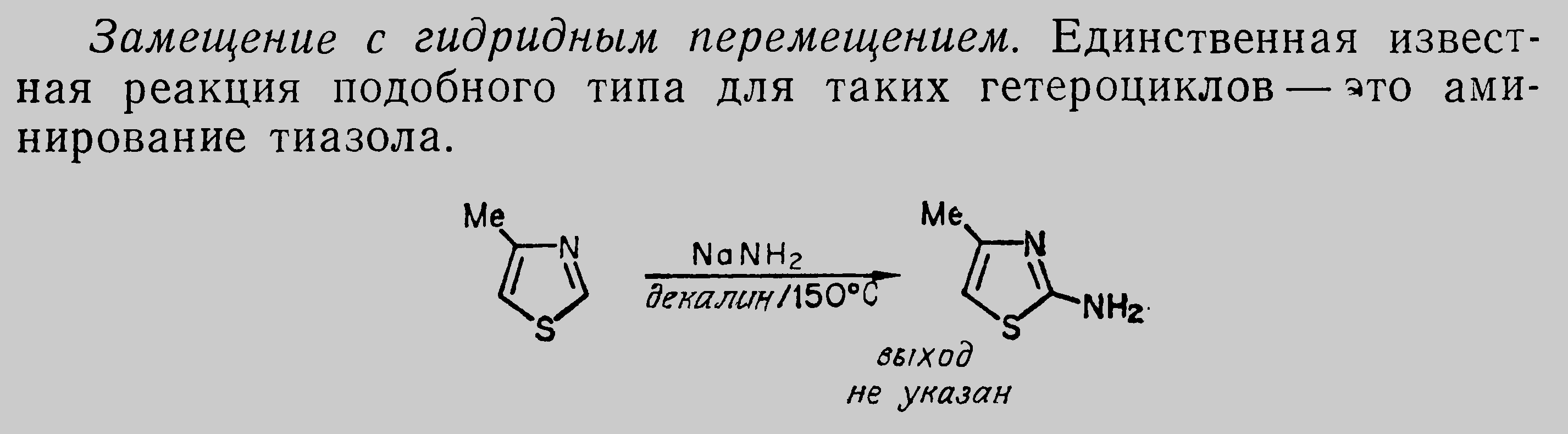
28. Пиридин және анилиннің реакциялық қабілеттілігін салыстырыңыз.
Анилин әлсіз негіздік қасиет көрсетеді. Пиридинмен салыстырғанда анилин алкилдеу және ацилдеу реакциясына түседі. Амин тобы бойынша реакциялар
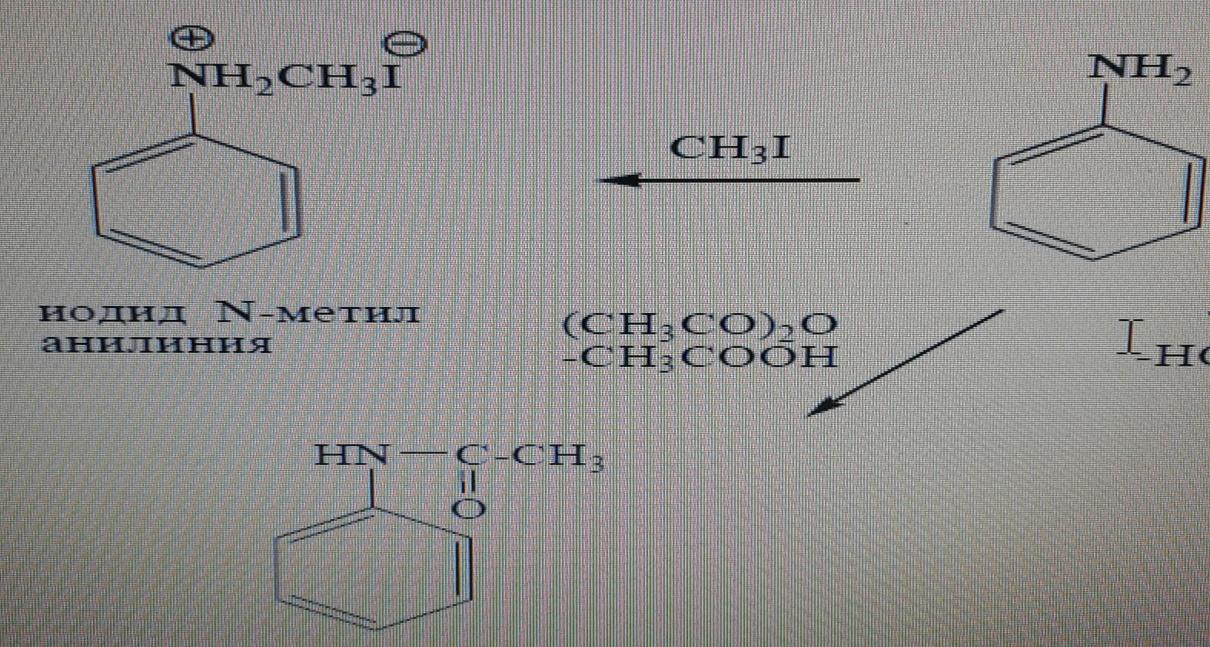
Бензол сақинасы бойынша реакциялар.
-NH2 тобы бензол сақинасын активтейтін электрондонорлы топқа жатады және қышқыл қатысында электрофилды орто және –пара орынға бағыттайды. Қышқыл әсерінен азот атомының протондалуы жүреді , олар электронакцептрлі топқа айналады.
Галогендеу.
Анилиннің моногалоген туындысын алу үшін алдымен -NH2 тобының активтілік қасиетін төмендету керек, ол үшін оны ацилдейді, сосын ацетил тобын сілтілік гидролиз арқылы алып тастайды:
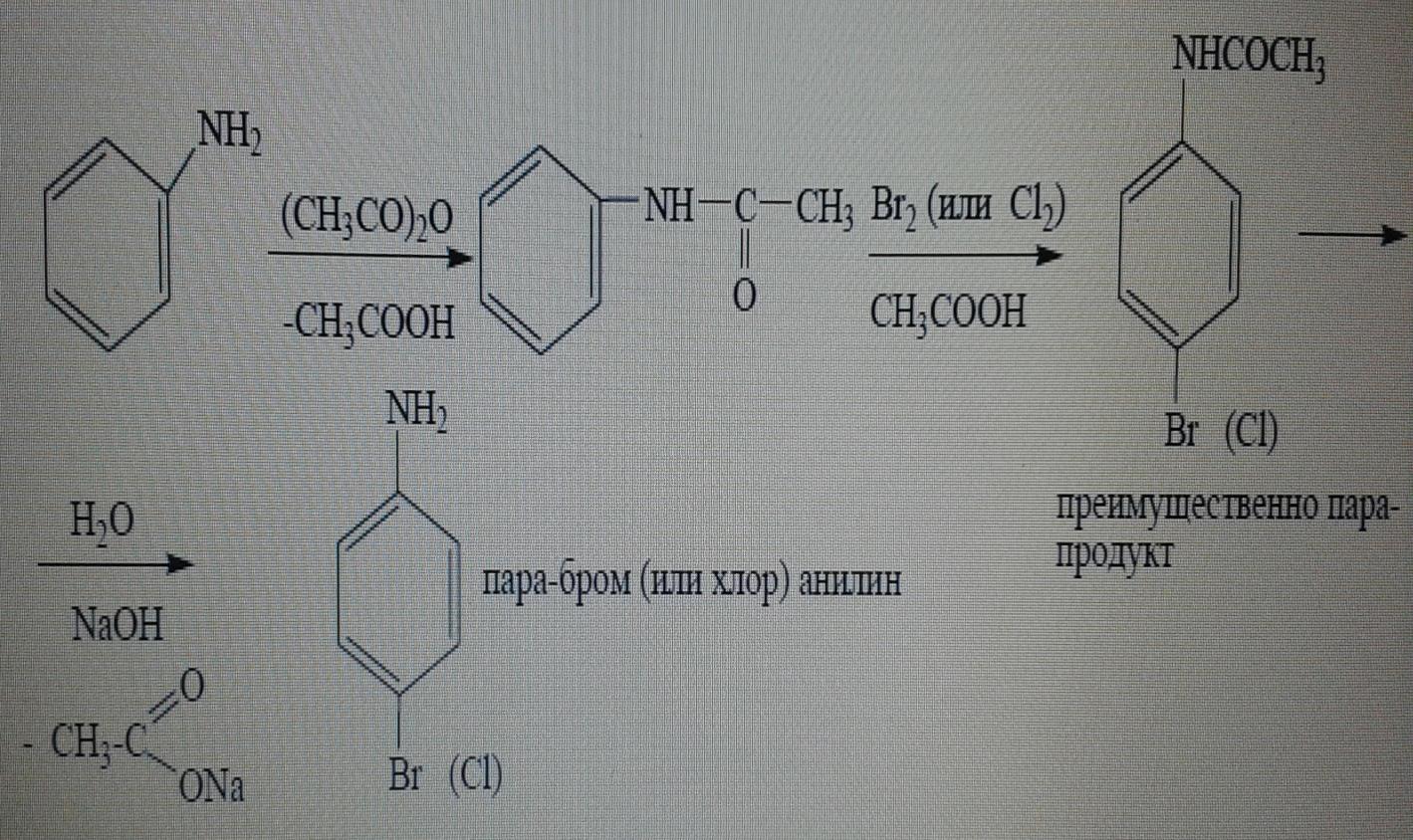
Нитрлеу.
Орто
және пара- нитроанилин алу үшін амин
тобын ацилдейді, сосын нитрлеу жүргізеді.
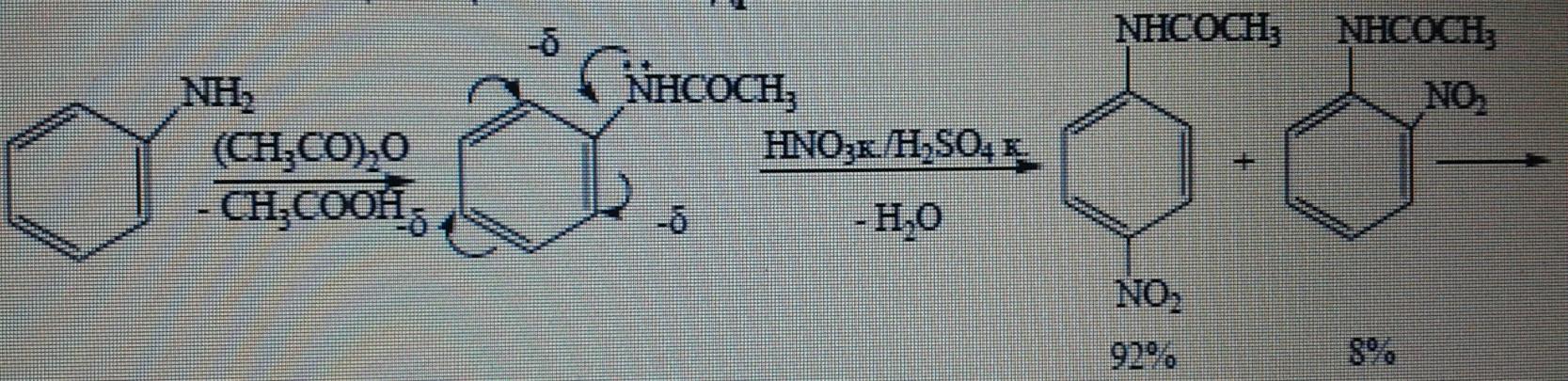
Пиридин электрофильді орын басу реакциясына қиын түседі. Нитрлеу, сульфлеу, галогендеу реакциялары қатаң жағдайда жүреді, ал Фридель- Крафтс реакциясына , яғни алкилдеу және ацилдеу реакцияларына түспейді. Пиридиндағы азот атомы жаңа орынбасарды мета –жағдайға бағыттайды.
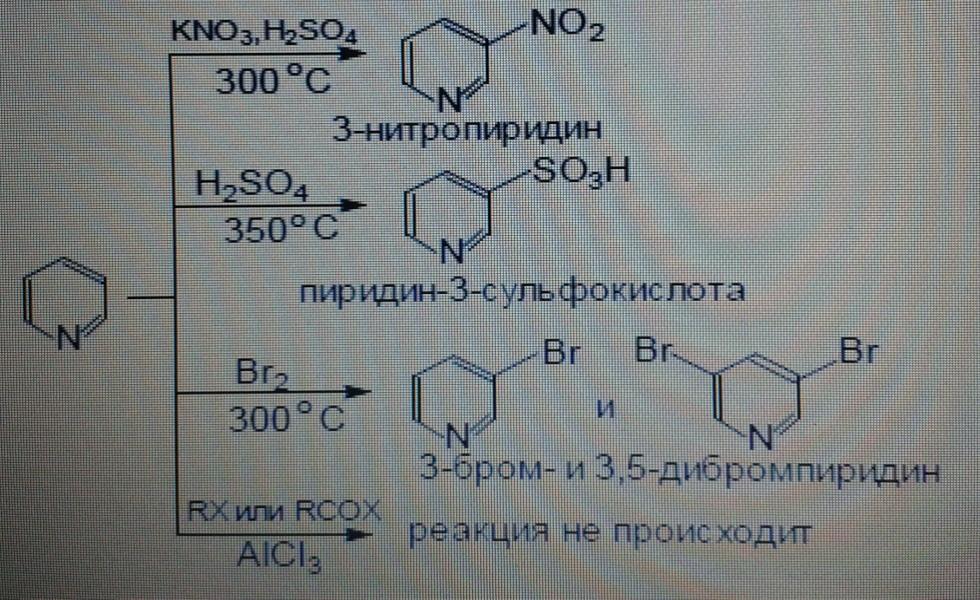
Нуклеофильді орынбасу оңай жүреді, 2 және 4 орын бойынша- бұл орындарда σ- комплекс оңай түзіледі.
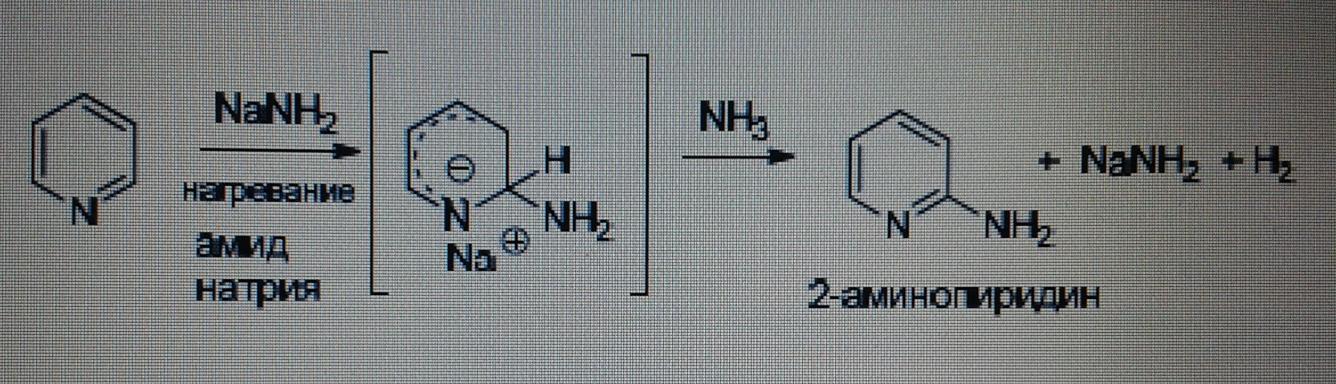

Пиридиннің электрофильді орынбасу реакциясында реакциялық қабілеттілігінң төмен болып, нуклеофильді орынбасу реакциясында жоғары активтілік қасиетін көрсетуіне негізгі себеп - азот атомының электртерістігі.
