
- •Содержание
- •Глава 1.Распространение воды на планете земля……………5
- •Глава 2.Строение состав воды………………………………………...6
- •Глава 3.Физические свойства воды……………………………….14
- •Глава 4.Определение временной или карбонатной жесткости воды…………………………………………………………....22
- •Глава 5.Химические свойства воды………………………………28
- •Глава 6.Загрязнение вод в тульской области………………….31
- •Введение
- •Глава 1. Распространение воды на планете земля
- •Глава 2.Строение и состав воды
- •2.1 Изотопный состав воды
- •2.2 Строение молекулы воды
- •2.3 Диаграмма состояния воды
- •Глава 3.Физические свойства воды
- •3.1 Определение физических показателей воды. Определение количества грубодисперсных примесей
- •3.1.1. Теоретическая часть
- •3.2. Определение содержания грубодисперсных примесей воды
- •3.2.1 Практическая часть
- •3.3 Определение запаха воды
- •3.4 Определение прозрачности воды
- •3.5 Определение цветности воды
- •3.6 Определение плотности жидкостей
- •3.6.1 Теоретическая часть
- •3.7 Определение плотности жидкости при помощи пикнометра
- •3.7.1 Практическая часть
- •3.8 Определение кислотности воды
- •3.8.1 Теоретическая часть
- •3.8.2 Практическая часть
- •Глава 4. Определение временной или карбонатной жесткости воды
- •4.1 Понятие и методы устранения жесткости воды
- •4.2 Проведение анализа
- •4.3 Определение сульфатов в воде
- •4.3.1 Теоретическая часть
- •4.3.2 Практическая часть
- •Глава 5. Химические свойства воды
- •Глава 6. Загрязнение вод в тульской области
- •Заключение
- •Литература
4.2 Проведение анализа
Точно отмеряют 50 мл исследуемой воды и добавляют несколько капель раствора метилового оранжевого.
При титровании в растворе произойдут следующие реакции:
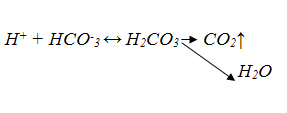 (1)
(1)
Сравним это и приведенное выше уравнение, которое показывало, что происходит с гидрокарбонатами кальция при кипячении. Как и при кипячении конечными продуктами этих реакций являются вода и углекислый газ. Только кальций здесь участия не принимает, так как ионы водорода, которые образуются в растворе при добавлении туда HCl вступают в реакцию не с ионами кальция, а именно с гидрокарбонатными ионами.
Кислоту удобно набрать в шприц до отмеченного заранее деления и из него дозировано добавлять в раствор. Сначала порции кислоты могут быть большими, но к концу титрования надо быть аккуратным и осторожным. Цвет может поменяться даже от одной капли. Способность раствора реагировать с ионами водорода по мере добавления кислоты будет постепенно уменьшаться и, наконец окажется почти совсем исчерпанной - кончатся гидрокарбонатные ионы и последняя капля кислоты резко сместит рН, так как связывать возникающие при ее диссоциации в воде ионы водорода уже будет «некому». При величине рН меньшей 4 гидрокарбонатных ионов в растворе уже нет. Индикатор при этом значении рН изменит цвет раствора с желтого на оранжевый. Тут титрование надо прекратить. Лучше проделать эту процедуру несколько раз, точно засекая какой объем кислоты был израсходован. Затем вычислить средний объем пошедший на титрование кислоты. Зная этот объем рассчитывают карбонатную жесткость по формуле:
Жесткость
карбонатная (мг-экв/л.) = (1000*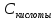 *
*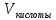 )
/
)
/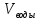
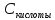 -
концентрация кислоты в молях,
-
концентрация кислоты в молях,
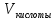 -
объем раствора кислоты, использованный
при титровании (мл)
-
объем раствора кислоты, использованный
при титровании (мл)
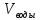 -
объем пробы воды, взятой для титрования
(мл.)
-
объем пробы воды, взятой для титрования
(мл.)
Если
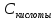 =
0,05 M, а
=
0,05 M, а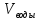 = 50 мл, то жесткость карбонатная (мг-экв/л.)
= (1000*0,05*
= 50 мл, то жесткость карбонатная (мг-экв/л.)
= (1000*0,05*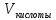 )/50
=
)/50
=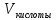
То есть титрование 50 мл воды 0,05 M соляной кислоты, то в этом случае карбонатная жесткость в мг-экв./л. Будет численно равна объему кислоты (в мл.), израсходованному для титрования. Например, если на титрование ушло 1,5 мл.раствора кислоты, то карбонатная жесткость воды 1,5 мг - экв./л. Для перевода в градусы KH значение в мг-экв/л. Надо умножить на 2,804.
1,5*2,804 = 4,2 ºKH
На самом деле этим методом мы определили щелочность воды, то есть ее способность связывать ионы водорода, которые образуются при диссоциации в воде соляной кислоты.
Гидрокарбонатный
ион может поступать в воду не только
при растворении карбонатов кальция и
магния, но и при растворении иных солей.
Всем известная питьевая сода являет
собой пример такого соединения NaHC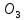 .
Если внести питьевую соду в аквариум,
то растворившись, она даст ионы натрия
и гидрокарбоната. Гидрокарбонатные
ионы присоединяют к себе ионы водорода,
поэтому вода в аквариуме от внесения
питьевой соды становится менее кислой
или приобретает щелочную реакцию, но
это зависит от дозы. Небольшие ее добавки
застрахуют от неожиданных скачков рН.
Решить достаточно соды внесено или нет
можно измерив щелочность. Зная щелочность,
вы можете оценить насколько вода в
аквариуме способна противостоять
закислению, то есть оценить буферность.
Если щелочность пресной воды низкая
(менее мг/экв/л), то ее буферность невелика.
Такая вода может резко скиснуть, например
при неожиданной остановке фильтра.
Интервал значений щелочности 1,2-2 мг-экв/л
пригоден для большинства рыб и растений.
Буферность воды при этом будет вполне
достаточной для поддержания стабильной
активной реакции воды рН. Обычно
щелочность аквариумной воды как раз и
оказывается в указанном интервале или
даже имеет еще большие значения 3 мг-экв/л
и выше (в этом случае возможны проблемы
с выращиванием многих растений и
нашествия водорослей). В регионах с
мягкой слабокислой водой она может быть
очень низкой. Если вносили в аквариум
соду, чтобы поднять и стабилизировать
рН, то не нужно удивляться если «карбонатная
жесткость» вдруг превысит общую. Если
вносили в воду аквариумаNaHC
.
Если внести питьевую соду в аквариум,
то растворившись, она даст ионы натрия
и гидрокарбоната. Гидрокарбонатные
ионы присоединяют к себе ионы водорода,
поэтому вода в аквариуме от внесения
питьевой соды становится менее кислой
или приобретает щелочную реакцию, но
это зависит от дозы. Небольшие ее добавки
застрахуют от неожиданных скачков рН.
Решить достаточно соды внесено или нет
можно измерив щелочность. Зная щелочность,
вы можете оценить насколько вода в
аквариуме способна противостоять
закислению, то есть оценить буферность.
Если щелочность пресной воды низкая
(менее мг/экв/л), то ее буферность невелика.
Такая вода может резко скиснуть, например
при неожиданной остановке фильтра.
Интервал значений щелочности 1,2-2 мг-экв/л
пригоден для большинства рыб и растений.
Буферность воды при этом будет вполне
достаточной для поддержания стабильной
активной реакции воды рН. Обычно
щелочность аквариумной воды как раз и
оказывается в указанном интервале или
даже имеет еще большие значения 3 мг-экв/л
и выше (в этом случае возможны проблемы
с выращиванием многих растений и
нашествия водорослей). В регионах с
мягкой слабокислой водой она может быть
очень низкой. Если вносили в аквариум
соду, чтобы поднять и стабилизировать
рН, то не нужно удивляться если «карбонатная
жесткость» вдруг превысит общую. Если
вносили в воду аквариумаNaHC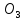 ,
то есть не связанные с кальцием и магнием
гидрокарбонатные ионы, то естественно
их будет больше, чем ионов
,
то есть не связанные с кальцием и магнием
гидрокарбонатные ионы, то естественно
их будет больше, чем ионов
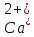 и
и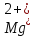 .
.
Вот в этом и состоит суть парадокса, когда формула:
Общая жесткость = Постоянная жесткость + Временная жесткость не выполняется из-за того, что временная больше общей. (2)
