
- •Колебательная спектроскопия
- •Спектральные области и методики
- •Определение и особенности ИКС
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Рис 1. Потенциальные кривые, уровни энергии и схематические спектры гармонического (1) и ангармонического
- •Происхождение инфракрасных спектров. Колебания атомов в молекуле
- •Рис 2. Схема энергетических уровней в молекуле, иллюстрирующая поглощение излучения
- •Правила отбора для ИК-спектроскопии
- •Рис 3. Валентные и деформационные колебания метиленовой группы
- •Колебания и спектры многоатомных молекул
- •Колебания и спектры многоатомных молекул
- •Каждая полоса в ИК-спектре характеризуется следующими параметрами:
- •Рис 5. Схема ИК-спектрометра (UR-10, UR-20, ИКС-29 и др.)
- •Современный ИК-спектрометр
- •Источники излучения ИК-спектров
- •Подготовка образцов для снятия ИК-спектров
- •Пробы для ИК-спектров
- •Держатель таблеток
- •Пресс и матрица для приготовления
- •Кювета жидкостная разборная
- •Монохроматоры (монохроматизаторы)
- •Детекторы для ИК-спектров
- •Рис 6. Пример ИК-спектра органического вещества
- •Рис 7. Частоты колебаний связей между атомами
- •Условия идентификации веществ и расшифровки структуры
- •Условия идентификации веществ и расшифровки структуры
- •Рис 8. ИК-спектр н-гексана СН3(СН2)4СН3
- •Рис 10. ИК-спектр гексанола-2 СН3(CH2)3СН(ОН)СН3
- •Рис 11. ИК-спектр гексанона-2 СН3(CH2)3С(О)СН3
- •Рис 12. ИК-спектр толуола С6H5СН3
- •Преимущества метода ИК-спектроскопии
- •Спектроскопия комбинационного рассеяния
- •Основы метода
- •Основы метода
- •Квантовая теория
- •Рис. 13. Пример спектра КР
- •Основные блоки установки для снятия спектров КР
- •Рис.14. Схема установки со спектрометром ИСП-15
- •Современный КР-спектрометр (RMP-300)
- •Преимущества КР спектроскопии
- •Преимущества КР спектроскопии
Колебательная спектроскопия
Инфракрасные спектры (ИКС) и спектры комбинационного рассеяния (СКР)
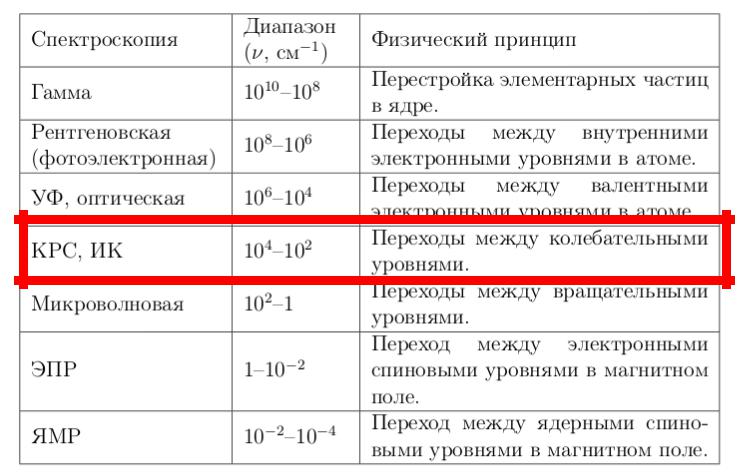
Спектральные области и методики
2
Определение и особенности ИКС
•Инфракрасная спектроскопия (ИКС) принадлежит к обширной группе методов молекулярной спектроскопии и основана на избирательном поглощении излучения в инфракрасной области (0.8 – 1000 мкм) спектра
•Поглощать инфракрасное (ИК) излучение могут только те молекулы веществ и соединений, у которых изменяется дипольный момент при колебаниях атомов
•ИК излучение расходуется только на изменение колебательной и вращательной энергии молекулы, не вызывая из-за недостатка поглощаемой энергии (hν) электронных переходов
•ИК спектры более сложные, чем электронные спектры в видимой области, поскольку большая часть поглощенной энергии затрачивается на колебательные процессы
•ИК спектры молекул характеризуются высокой информативностью
3

Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Длина волны ( ) и частота ( ) связаны между собой соотношением, где С – скорость распространения излучения в определенной среде
•Для характеристики электромагнитного излучения применяется также волновое число ( ,) – величина, обратная длине волны:
•Интенсивность поглощения ИК-излучения, как правило, выражают величиной пропускания (Т), где I – интенсивность излучения, прошедшего через образец;
•I0 – интенсивность падающего излучения.
С
' 1
T I 100%, I0
4

Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Для гармонического осциллятора возвращающая сила пропорциональна величине смещения ядер из положения равновесия и направлена в сторону, противоположную смещению, где К –
коэффициент пропорциональности, который называется силовой постоянной и
характеризует жесткость связи (упругость связи).
•Частота колебаний такой системы связана с силовой постоянной К и с массами атомов (m1 и
m2) следующим соотношением, где |
– |
приведенная масса
FK r
1 К 2 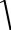
m1 m2 m1 m2
5
Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Силовые постоянные одинарных, двойных и тройных связей соотносятся приблизительно как 1: 2: 3
•Частота колебаний возрастает с увеличением прочности связи (кратности связи) и с уменьшением масс атомов:
•Меньше масса атома – выше частота :
С-H (3000 см-1), С-D (2200 см-1), C-O (1100 см-1), C-Cl (700 см-1)
•Связь прочнее – выше частота:
С≡O (2143 см-1), C=O (1715 см-1), C-O (1100 см-1).
6
Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Для гармонического осциллятора: величина полной энергии колебания подчиняется основному квантовому условию, где – колебательное квантовое число, принимающее значения целых чисел: 0, 1,
2, 3, 4 и т.д.; 0 – частота основного колебания (основной тон).
•Энергия поглощенного кванта равна разности энергий двух состояний:
•Разность энергий для двух энергетических уровней составляет:
•Таким образом, частота поглощенного излучения ( ) равна основной колебательной частоте ( 0)
Екол 1/ 2 h 0
h = Е + 1 – Е
Е + 1 – Е = h 0
7
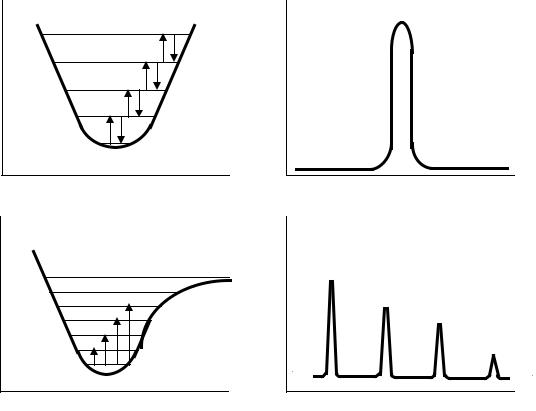
Рис 1. Потенциальные кривые, уровни энергии и схематические спектры гармонического (1) и ангармонического (2) осцилляторов
Е |
1 |
|
|
|
|
|
|
= 4 |
|
||
|
= 3 |
|
|
= 2 |
|
|
= 1 |
|
|
= 0 |
|
|
r |
|
Е |
2 |
|
|
|
|
|
|
|
|
= 3 |
|
|
V = 2 |
|
|
= 1 |
|
|
= 0 |
|
|
r |
|
= 1
|
/, см -1 |
|
|
= |
|
|
|
1 |
= |
= |
|
|
|
||
|
2 |
3 |
= |
|
|
||
|
|
|
4 |
|
/, см -1 |
|
|
8
Происхождение инфракрасных спектров. Колебания атомов в молекуле
•Обычно при комнатной температуре большинство молекул находится в нижнем колебательном состоянии, поскольку энергия теплового возбуждения значительно меньше, чем энергия перехода из основного состояния в возбужденное.
•Поэтому экспериментально легче всего наблюдать поглощение, соответствующее переходу из основного колебательного состояния ( = 0) в первое возбужденное ( = 1).
•Для гармонического осциллятора возможны и другие переходы с изменением квантового числа на единицу, т.е. переходы между
соседними уровнями: = 1
9
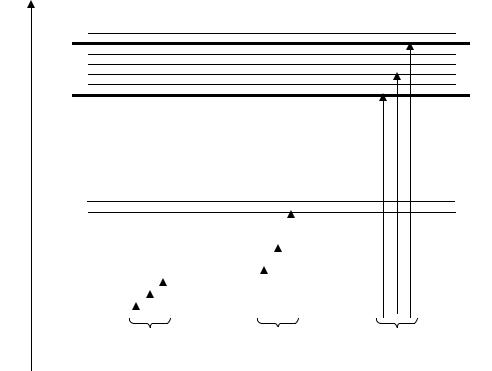
Рис 2. Схема энергетических уровней в молекуле, иллюстрирующая поглощение излучения
Е |
|
1 |
|
/ |
|
0 |
S1 |
/ |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Вращательные |
Колебательные |
|
|
|
|
||||||||||
|
|
|
|
Электронные |
||||||||||||
|
|
|
|
переходы |
переходы |
переходы |
||||||||||
10
