
Метода термодинамика(лекции)
.pdf
Здесь через const обозначены параметры, не зависящие от значения εi и
свойств подсистемы. Формула определяет вероятность того, что слабо взаимодействующая часть некоторого собрания произвольных физических
систем будет находиться в одном из Ω(εi ) состояний с энергией между εi и
εi + δεi , а термостат – в одном из состояний с энергией между E −εi и
E −(εi + δεi ). Но так как состояние термостата не представляет интереса,
для краткости говорят, что w(εi ) – вероятность нахождения подсистемы в одном из состояний с энергией εi . Из определения вероятности следует условие нормировки
∑w(εi ) = 1, |
(1.57а) |
i |
|
где суммирование ведется по всем возможным квантовым состояниям системы. Отсюда вытекает, что введенный формально коэффициент θ является существенно положительной величиной:
|
|
|
|
|
∂E |
> 0 . |
(1.57б) |
θ = |
|
||
|
|
|
|
|
∂σ ε =0 |
|
|
|
i |
|
|
Только в этом случае вероятность состояний сколь угодно больших энергий стремится к нулю. Постоянная в (1.56) находится из условия нормировки
const = 1 ∑e−εi 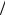 θΩ(εi ),
θΩ(εi ),
и распределение вероятностей принимает вид
wi |
= |
e−εi θΩ(ε ) |
(1.58) |
|
∑e−εi |
θΩ(εi ) . |
|||
|
|
|
i |
|
Оно впервые предложено Дж. Гиббсом (1901 г) для классических систем и получило название распределение Гиббса или канонического распределения.
Сумма, стоящая в знаменателе, играет большую роль в статистической физике, для нее введено специальное обозначение
Z = ∑e−εi θΩ(εi ), |
(1.59) |
52

и принято называть функцией (интегралом) состояния (статистической суммой). Распределение Гиббса позволяет вычислить среднее значение любой физической величины L(εi ), зависящей от состояния системы:
|
|
= ∑L(εi )w(εi ) = |
1 |
∑L(εi )e−εi θΩ(εi ). |
(1.60) |
|
L |
||||||
Z |
||||||
|
|
|
|
|
||
1.6.3. Квазиклассическое приближение . Переход от квантового описания системы к квазиклассическосму проведем следующим образом. Внутренняя энергия макроскопических систем меняется непрерывно, и квантовые эффекты не имеют существенного значения (см. раздел 1.3 и формулу (1.35) при a → ∞). Из распределения Гиббса следует, что для замены ступенчатой функции e−εi 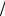 θ плавной – e−ε
θ плавной – e−ε θ необходимо, чтобы интервалы между энергиями ∆εi = εi+1 −εi были малы по сравнению с θ. Это означает, что переход к квазиклассической статистике должен происходить при прочих равных условиях в области высоких температур θ >> ∆εi .
θ необходимо, чтобы интервалы между энергиями ∆εi = εi+1 −εi были малы по сравнению с θ. Это означает, что переход к квазиклассической статистике должен происходить при прочих равных условиях в области высоких температур θ >> ∆εi .
Состояние системы, состоящей из N частиц и имеющей 3N степеней свободы, в квазиклассическом приближении определяется значениями координат (qi ) и импульсов ( pi ). Ее энергия является непрерывной функцией всех координат и импульсов ε(p,q). Это позволяет говорить о непрерывном распределении вероятностей того, что система находится в одном из состояний в интервале энергий между ε(p,q) и ε(p,q) + δε(p,q). Учитывая, что согласно
(1.40), число таких состояний равно Ω(ε)dε = (1 h3N ) (dΓ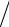 dε)dε,
dε)dε,
распределение Гиббса в квазиклассическом приближении принимает вид
dw = |
e−ε(p,q) θ |
|
∂Γdε, |
(1.61) |
|||||
Z h3N |
|||||||||
|
|
|
∂ε |
|
|||||
где |
|
|
|
|
|
|
|
|
|
Z = |
1 |
∫e− |
ε(p,q) |
∂Γdε |
(1.62) |
||||
θ |
|||||||||
3N |
|||||||||
|
h |
|
|
∂ε |
|
||||
53
Отличие этой формулы от (1.59) состоит в том, что сумма по состояниям заменена интегралом. Интегрирование ведется по всему фазовому пространству, доступному для системы, т.е. по всем дозволенным значениям координат и импульсов системы.
1.7. Свойства распределения Гиббса
Область применения распределения Гиббса ограничена следующими условиями:
1)система находится в равновесном состоянии;
2)наличие макроскопической системы (термостата), составляющей ее окружение (термостата);
3)слабое взаимодействие между системой и термостатом.
Востальном свойства системы произвольны, в частности, не зависят от характера взаимодействия и ее агрегатного состояния.
Поскольку статистическая температура θ положительная величина (1.57б), то энтропия, а, следовательно, и число состояний (σ = ln Ω) являются монотонно возрастающей функцией энергии. Чем больше частиц содержит
система, тем больше состояний Ω(εi ) , отвечает данному значению интервала энергии (εi, εi +δεi ). С ростом энергии (увеличением квантового числа n )
резко возрастает плотность энергетических уровней (1.35б). Поэтому рост
Ω(εi ) с энергией происходит тем быстрее, чем больше частиц в системе.
Чтобы выяснить характер зависимости распределения Гиббса w(ε) от энергии, необходимо вычислить производную ∂Γ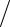 ∂ε (1.61). Расчеты
∂ε (1.61). Расчеты
проведем для ансамбля молекул идеального газа. Объем части фазового пространства, в котором энергия газа не превышает ε, по определению, равен интегралу
Γ = ∫dp1...dp3Ndq1...dq3N ,
54

где пределы интегрирования следуют из условия
3N
∑pi2 2m ≤ ε(p,q). (1.63)
i=1
Оно не включает координаты молекул, по которым можно интегрировать непосредственно
Γ =V N ∫dp1...dp3N , |
(1.64) |
поскольку для каждой молекулы можно написать
V= ∫dq1dq2dq3 .
Сгеометрической точки зрения формула (1.63) определяет в импульсном
пространстве 3N измерений шар, радиус которого равен R = 2mε , а
интеграл в (1.64) представляет его объем. В трехмерном пространстве объем пропорционален R3 , т.е. ~ ε3/2 . Исходя из соображений размерности в 3N –
мерном пространстве он пропорционален R3N . Поэтому из (1.64) следует
Γ = const R3N V N = const ε3N /2 V N .
После дифференцирования имеем
∂Γ |
= const ε |
(3N /2)−1 |
V |
N |
(1.65) |
∂ε |
|
|
Постоянная не имеет особого значения, поскольку оно будет сокращаться с такой же постоянной, возникающей при вычислении Z . Поэтому распределение Гиббса принимает вид
dw = const |
e− |
ε |
3N |
−1 V Ndε. |
θ |
ε 2 |
|||
h3N Z |
|
|
|
|
3N |
−1 |
3N |
Поскольку множитель ε 2 |
ε 2 |
весьма быстро растет с увеличением ε, а
множитель e−θε , напротив, резко убывает, функция распределения Гиббса для макроскопических систем (N ≈ 1023 моль-1) имеет очень резкий максимум, степень его размытости совершенно ничтожна. Это означает, что вероятность нахождения системы в состояниях с энергией, заметно отличающейся от
55
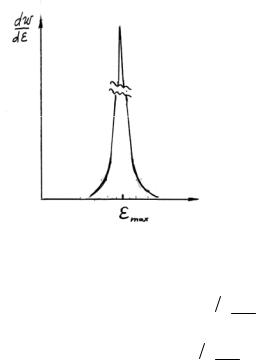
энергии εmax , отвечающей максимуму распределения Гиббса, практически равна нулю (рис. 1.5). Такой характер зависимости позволяет в первом приближении отождествить ее с δ(εmax −ε)–дельта функцией Дирака,
которая определяется для непрерывной функции ϕ(x) при ϕ(x → ±∞) → 0
|
операторным соотношением |
|
dw |
||
|
||
dε |
∞ |
|
|
||
|
∫ ϕ(x)δ(x −a)dx = ϕ(a). |
|
|
||
|
−∞ |
|
|
|
В макросистемах εmax практически совпадает |
|
|
|
со средним значением энергии ε . Поэтому |
|
|
|
средняя величина какого-либо физического |
|
|
|
|
|
εmax |
ε |
параметра L(ε) макроскопической системы |
Рис. 1.5. |
|
есть функция средней энергии |
|
|
|
|
∫ L(ε)e |
−ε θ ∂Γ |
|
|
|
|
||
|
|
= |
|
∂ε dε |
= |
∫ L(ε)δ(εmax −ε)dε |
= L(ε) . |
(1.67) |
||
L(ε ) |
|
|||||||||
|
|
|
|
|
||||||
|
i |
|
∂Γdε |
∫ δ(εmax −ε)dε |
|
|||||
|
|
|
∫e−ε θ |
|
||||||
|
|
|
|
|
∂ε |
|
|
|
|
|
По сути это означает, что состояние с энергией |
ε = ε осуществляется с |
|||||||||
полной достоверностью, |
а при |
остальных |
энергиях невозможно |
|||||||
w(ε ≠ ε) = 0 . |
|
|
|
|
|
|
|
|||
1.8. Большое каноническое распределение Гиббса
Взаимодействие подсистемы с окружением в общем случае осуществляется взаимным обменом не только энергией, но и частицами. В процессе взаимодействия частицы уходят из подсистемы или приходят в нее, унося или принося при этом соответствующее количество энергии. Обмен энергией и частицами происходит одновременно. В такой ситуации переменной является не только энергия, но и число частиц в ней. При этом
56
выделенная подсистема может побывать во всех квантовых состояниях, отличающихся числом частиц.
Примером систем с переменным числом частиц могут быть капля или кристалл (лед), находящийся в равновесии с паром или расплавом (водой), соответственно. Последние играют роль окружения (термостата). Молекулы с поверхности жидкости переходят в пар, а молекулы из пара конденсируются на поверхности жидкости. Тоже происходит с молекулами на поверхности кристалла. Если систематического перехода частиц из пара в жидкость или обратно не происходит, то в системе установится состояние равновесия, при котором число частиц, переходящих в обоих направлениях, уравнивается. Подобная ситуация имеет место и в равновесной химической реакции. В выделенной подсистеме (например, молекулах соединения AB ) число частиц изменяется: уменьшается за счет реакции распада AB → A +B и увеличивается за счет синтеза A +B → AB .
Для характеристики состояния таких систем необходимо указать не только ее полную энергию, но и число частиц, которое в ней содержится.
Задача заключается в нахождении распределения вероятностей win того, что подсистема находится в i -ом состоянии и содержит при этом n частиц. Ее решение проведем по алгоритму, изложенному в разделе 1.6.2. Отличие состоит в том, что число состояний системы с данной энергией Ω(εi ) следует заменить на Ω(εi,n) , где учитывается число частиц, а число состояний термостата – на Ω0(E0,N0 ) . Поскольку сумма числа частиц в подсистеме и термостате остается постоянной N = n +N0 = const , вместо формул (1.51)
и (1.53) получаем
win ~ Ω0(E −εi,N −n) Ω(εi |
,n), |
||||
|
|
|
|
|
(1.68) |
Ω0(E − |
εi,N −n) e |
σ(E−εi |
,N −n) |
. |
|
|
|
|
|||
Так как размеры термостата, его энергия и число содержащихся в нем частиц велики, то для всей замкнутой системы (подсистема + термостат) справедливы
57

неравенства εi << E и |
n << N . Поэтому, |
как и в разделе 1.6.2, можно |
|||||||||||
разложить функцию σ в ряд по степеням εi |
и n и ограничиться линейными |
||||||||||||
членами разложения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
∂σ |
|
|
|
∂σ |
n +.... |
|||
σ(E −ε,N −n) |
σ(E,N) − |
|
|
|
|
|
ε |
− |
|
|
|||
|
|
|
|
|
|||||||||
i |
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
∂E ε =0 |
|
|
∂N n=0 |
|
|||||
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
И для вероятности имеем |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
w |
|
= const e |
− |
εi −µn |
Ω(ε,n). |
|
|
(1.69) |
||||
|
in |
θ |
|
|
|||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
Статистическая температура по-прежнему вычисляется по формуле (1.55)
θ = (∂E ∂σ) |
. Коэффициент µ называется |
химическим (парциальным) |
|||
ε =0 |
|
|
|
|
|
|
i |
|
|
|
|
потенциалом и определяется выражением |
|
|
|||
|
|
|
|
|
|
|
|
∂σ |
, |
(1.70) |
|
|
µ = −θ |
|
|
||
|
|
||||
|
|
|
|
|
|
|
|
∂N n=0 |
|
|
|
где производная берется при постоянном значении энергии и внешних
параметров. Из условия нормировки |
∑∑win |
= 1 находится постоянная |
||||
|
|
|
i n |
|
|
|
величина |
|
|
|
|
|
|
|
|
|
µn−εi |
|
|
−1 |
|
|
|
|
Ω(εi |
|
|
|
|
θ |
|
|||
const = ∑∑e |
|
|
,n) . |
|||
|
i n |
|
|
|
|
|
|
|
|
|
|
|
|
Искомое распределение вероятностей состояний системы с переменным числом частиц принимает вид
win |
= |
e−(εi −µn) θΩ(ε,n) |
1 |
|
−(ε −µn) θ |
Ω(εi |
,n). |
(1.71) |
||
∑∑e−(εi |
−µn) θΩ(εi,n) |
= Z e |
i |
|||||||
|
|
|
i |
|
|
|
|
|
|
|
i n
Здесь через Z обозначена функция состояний, которая при постоянном числе частиц в системе n = n совпадает с (1.60). Полученная формула называется
большим каноническим распределением Гиббса. Оно позволяет находить
58

средние значения любой величины L(εi,n), зависящей от состояния системы и числа частиц:
L = 1 ∑∑L(εi,n)e−(εi −µn)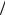
Z i n
θΩ(εi,n) . (1.72)
В частности, среднее число частиц при произвольном значении энергии системы равно
|
|
= |
1 |
∑∑ne−(εi −µn) θΩ(εi,n) = θ |
∂ |
ln ∑∑e−(εi −µn) θΩ(εi,n) = θ |
∂ |
ln Z . |
|
n |
|||||||||
|
|
∂µ |
∂µ |
||||||
|
|
|
Z i n |
i n |
|
||||
(1.73)
Это по существу первый и далеко не единственный пример определения физических параметров через функцию состояний.
Рассмотрим равновесную систему, состоящую из двух подсистем, также находящихся в состоянии статистического равновесия и слабо взаимодействующие между собой (обмениваются частицами и энергией). Для каждой из них можно записать
w |
1 |
= Ae(µ1n1 −εi1 ) θ1 |
Ω , |
w |
2 |
= Ae(µ2n2 −εk 2 ) θ2 |
Ω . |
|
1 |
1 |
|
2 |
2 |
Поскольку подсистемы слабо взаимодействуют, то, согласно теореме умножения вероятностей, для вероятности одновременного нахождения первой системы в i -ом, а второй – в k -ом состояниях находим
w′ |
= w w |
2 |
= Ae(µ1n1 −εi1 ) θ1 |
Ae(µ2n2 −εk 2 ) θ2 |
Ω Ω . |
|
12 |
1 |
1 |
2 |
1 |
2 |
|
Две подсистемы образуют одну равновесную систему с суммарной энергией
(εi1 + εk 2 ) и числом частиц (n1 +n2 ), для которой также справедливо большое каноническое распределение
′′ |
= Ae |
µ(n +n )−(ε |
+ε ) |
θ |
Ω. |
|
|
|
|||
w12 |
1 2 i1 |
k 2 |
|
||
|
|
|
|
Если подсистемы находятся в состоянии равновесия, то при установлении взаимодействия между ними их состояние не должно изменяться. Поэтому необходимо, чтобы вероятности w12′ и w12′′, определенные последними двумя
59

равенствами, были тождественно равны друг другу w′ |
≡ w′′ |
. Отсюда |
12 |
12 |
|
следуют равенства |
|
|
θ = θ1 = θ2 , µ = µ1 = µ2 . |
|
(1.74) |
С физической точки зрения, это означает равенство температур и парциальных потенциалов во всех квазинезависимых подсистемах, входящих в состав равновесной системы. Согласно молекулярным представлениям, равенство температур выражает требование, чтобы количества энергии, отдаваемое и получаемое подсистемой, были равны друг другу. В равновесном состоянии при обмене частицами не только совпадает числа приходящих и уходящих из подсистемы частиц, но равны и средние энергии, переносимые этими частицами – об этом свидетельствует равенство парциальных потенциалов. Если бы это было не так, например, уходили только быстрые, а приходили только медленные частицы, то состояние равновесия было бы нарушено.
Статистические температура θ и парциальный потенциал µ определяют состояние термостата. Только в том случае, когда выделенная подсистема является макроскопической, условия равновесия позволяют относить θ и µ к
самой подсистеме. Не имеет смысла говорить о температуре и парциальном потенциале микроскопической подсистемы, например, молекулы.
Вквазиклассическом приближении число состояний системы Ω(εi,n) , как
ив разделе 1.6.3, можно выразить через объем фазового пространства ∆Γn
Ω(ε,n) = ∆Γ |
n |
h3n . |
(1.74) |
i |
|
|
Здесь величина объема фазового пространства в отличие от систем с постоянным числом частиц изменяется с изменением числа частиц (степеней свободы 3n )
∆Γn = ∆q1∆q2...∆q3n ∆p1∆p2...∆p3n .
И большое каноническое распределение принимает вид
dwin |
= |
1 |
|
e−(ε−µn) θdΓn , |
(1.75) |
|
3n |
||||
|
|
Z h |
|
|
|
60
где функция состояния выражается следующим образом
Z = ∑∫e−(ε−µn)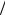 θdΓn .
θdΓn .
n
Приведенные положения статистической физики и распределения в равновесных системах относятся к широкому классу веществ. Конкретизации найденных закономерностей посвящены следующие разделы книги, где будут рассмотрены различные физические системы с учетом характера движения молекул, квазичастиц, типов взаимодействия. Общность законов статистической физики позволила не ограничивать круг ее рассмотрения чисто тепловыми процессами, но включить в нее самые разнообразные макроскопические свойства тел – оптические, электрические, магнитные, химические и т.п.
61
