
- •Раздел 1
- •1.1 Химический состав сплавов
- •Эталон для сравнения – фса 25 - Fe - 10, Si - 65, Al - 25 .
- •1.2 Технология получения и физические свойства
- •Дисперсный состав порошка сплава фса 25
- •Физические свойства порошков кристаллических сплавов
- •1.3 Методика проведения опытов
- •1.4 Результаты кинетических исследований
- •Термодинамические и кинетические данные реакций взаимодействия
- •1.5 Математическое описание процесса выделения водорода из воды
- •Зависимость полноты реакции от температуры, давления, концентрации едкого натра и содержания алюминия в сплавах фса
- •Раздел 2
- •Опытные и расчетные данные по теплоотдаче одиночной неподвижной сферической частицы сплава фс 90 Ба4
- •Раздел 3
- •3.1 Результаты испытаний кинетического реактора
- •3.2 Исследование процесса получения водорода в газогенераторе авг-45
- •Результаты испытаний газогенератора авг-45 на сплавах ферросилиция с добавками бария фс 75 Ба1 и фс 75 Ба4 и сплавах фса 15, фса 30 и фса 30 Мн1
- •Термодинамические и кинетические данные реакций взаимодействия сплавов с водным раствором едкого натра (авг-45)
- •Характеристики баллонных водородных реакторов
- •Опытные и расчетные данные по теплоотдаче от частиц сплавов к раствору едкого натра в газогенераторе авг-45
- •Термодинамические данные реакций взаимодействия сплавов с водой и водным раствором едкого натра с учетом влияния давления, рассчитанные на полупериод реакции τ0,5 (авг-45)
- •3.3 Методика расчета реакторов баллонного типа
Раздел 2
ТЕПЛОМАССООБМЕН ПРИ ВЗАИМОДЕЙСТВИИ ФЕРРОСИЛИЦИЯ И АЛЮМИНИЕВОГО СПЛАВА С ВОДОЙ
2.1 Методика ведения экспериментов
Для описания явления во всей полноте приходится прибегать как к методам термодинамики, так и к смежным дисциплинам, трактующим процесс с точки кинетики. В данном разделе ставится задача выявить роль тепломассообмена в ходе химических и физических превращений сплавов в оксиды.
Опыты по изучению тепломассообмена проведены в стеклянном сосуде и металлическом реакторе (см. раздел 3.4). На данном этапе исследовалась интенсивность теплоотдачи от кубика сплава ферросилиция ФС 90 Ба4 и частиц сплава А-98КаМг к циркулирующему потоку.
В центре кубика со стороной (8 - 12)∙10–3 м устанавливают термопару, отверстие для термопары (dотв = 3∙10–3 м) заливают эпоксидной смолой, предварительно изолировав спай термопары слоем хлопка (рис. 2.1).
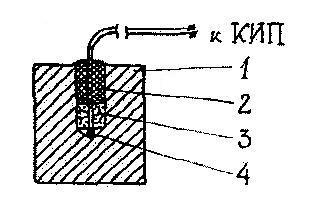
Рис. 2.1. Схема заделки спая термопары в образец:
1 - кубик сплава, 2 - эпоксидная
смола, 3 - слой хлопка, 4 - спай
термопары.
Контакт между термопарой и телом кубика
контролируют тестером. В качестве вторичного
прибора используют потенциометр КСП-4.
Одновременно с записью температуры среды
фиксируют температуру центра образца. Измерение
температуры поверхности образца выполняют термопа-
рой со щупом при проведении реакции в открытом сосуде.
Оценку инерционности системы проводят следующим образом: в открытый сосуд с кипящей водой погружают спай термопары и начинают отсчет времени. Прибор отображает повышение температуры до 93 °С за 5 с, через 60 - 90 с устанавливается температура 99 °С.
При погружении спая термопары в сосуд с маслом, нагретом до 180 °С, прибор через 5 с фиксирует 115 °С, через 55 с – 165 °С и через 180 с устанавливается температура 180 °С. Расчет стехиометрических (теоретических) температур дан в приложении А.
2.2 Результаты исследования тепломассообмена
Опытные данные по взаимодействию образцов сплава ФС 90 Ба4 и сплава на основе алюминия А-98КаМг с водным раствором едкого натра представлены в таблице 2.1 и на рисунках 2.2 - 2.7.
Таблица2.1
Зависимость скорости выделения водорода от температуры при взаимодействии сплава ФС 90 Ба4 с 13,3 %-ным раствором NaOH (кинетический реактор Vp = 1,13∙10–3 м3)
|
№№ опыта |
Начальная температура среды, tн,°С |
Максимальная температура сплава, tmax, °С
|
Время достижения максимальной температуры, τ∙10-3, с |
Максимальное давление, Рmax, МПа |
Время достижения максимального давления, τ∙10-3, с |
Общее время реакции τ∙10-3, с |
Вес сплава, m∙103, кг |
Максимальная скорость выделения водорода, Wmax∙103, м3/(кг∙с) |
|
1 2 3 4 5 6 7 |
901) 1201) 90 130 120 902) 903) |
100 128 103 137 130 105 109 |
0,54 0,16 0,51 0,2 0,18 0,05 0,047 |
0,44 0,68 0,48 0,84 0,8 0,92 0,93 |
2,94 0,72 3 2,1 2,4 0,05 0,047 |
2,94 0,9 3 2,2 2,6 0,06 0,05 |
5 5 5 5 5 5 5 |
0,18 0,68 0,22 1,08 1,04 8,9 9,1 |
Примечание:
1)–NaOH10 %-ной конц.;
2)–А-98КаМг с10 %NaOH;
3)–А-98КаМг с13,3 %NaOH.
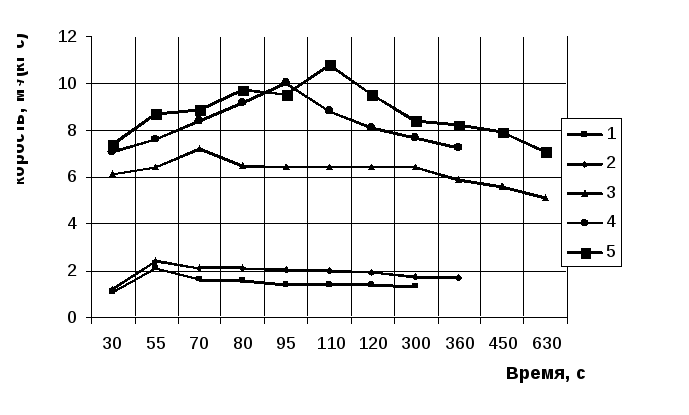
Рисунок 2.2. Зависимость скорости выделения водорода от времени
при различной температуре для реакции сплава ФС 90 Ба4 с водным
раствором едкого натра (кинетический реактор): 1-100 °С (10 % NaOH);
2-103 °С (13,3 %NaOH); 3-128 °С (10 %NaOH); 4-130 °С (13,3 %NaOH);
5-137 °С (13,3 %NaOH).
Давление в реакторе не превышает 0,93 МПа. Максимальная скорость выделения водорода при этом составила Wmax = 1,08∙10–3 м3/(кг∙с) или Wmax = 0,35 м3/(м2∙с) – см. табл. 2.1.
Характер изменения
температуры поверхности и центра
реагирующего образца сплава ФС 90 Ба4
при исследовании реакции в открытом
сосуде представлен на рисунке 2.3.
Установлено, что температура внешней поверхности гидроксидного слоя в местах газообразования (tm) выше температуры среды (td) на 2,3 - 3,1 °С.
Температура центра образца сплава (tц) превышает температуру среды на 3,1 - 5,3 °С (рис. 2.4).
Приближение фронта реакции к спаю термопары,
находящегося в центре образца, вызывает скачкообразное
повышение температуры на 7 - 9 °С при кипении и газо-
образовании (стеклянный сосуд). Больший скачок наблюдается
при более высокой температуре. Время прохождения
всплеска температуры 40 - 50 с.
После прохождения скачка прибор показывает темпера-
туру среды, измеряемую дополнительно ртутным термометром,
что свидетельствует о завершении реакции в связи с полным
разрушением образца.
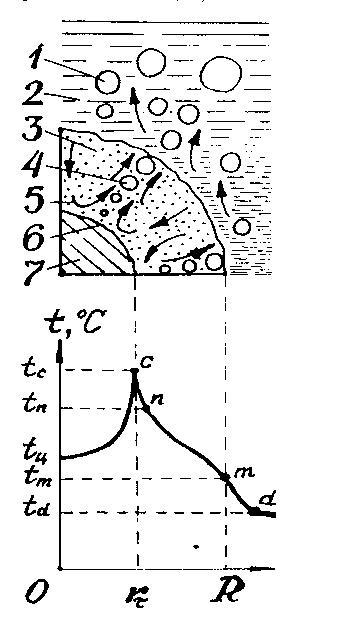
Рис. 2.4. Схема частицы сплава и изменения ее структуры при взаимо-действии с водой: 1 – газовые пузыри в жидкости, 2 – жидкость, 3 – слой образующегося гидроксида, 4 – газовые пузыри в слое гидроксида, 5 – направление циркулирующих потоков жидкости в слое гидроксида, 6 – реакционная поверхность частицы, 7 – непрореагировавшее ядро частицы.
Найденному значению температурного напора
(tп – td) соответствует вполне определенная интенсив-
ность теплоотдачи. Для расчета теплообмена от реаги-
рующей частицы к омывающей ее жидкости необходимо
найти скорость естественной циркуляции потока.
Эксперименты показали, что кубик сплава
ФС 90 Ба4 в воде, нагретой до 90 °С, практически не реагирует. В растворе щелочи 13,3 %-ной концентрации и температуре 95 °С реакция интенсифицируется. В течении 19-20 минут сплав полностью прореагировал.
При падении кассеты со сплавом ФС 90 Ба4 (d = 1·10–3 м) в раствор щелочи, температура среды в реакторе снижается на 8 - 10 °С. Индукционный период при этом составляет 3 - 5 с. Скачкообразное повышение температуры на 15 - 17 °С вызывает стремительный рост скорости реакции. Время прохождения всплеска температуры cоставило 10 - 12 с – см. рис. 2.5. На начальном этапе температура резко возрастает, затем темп роста замедляется, тем самым сказывается влияние образующегося гидроксидного слоя.
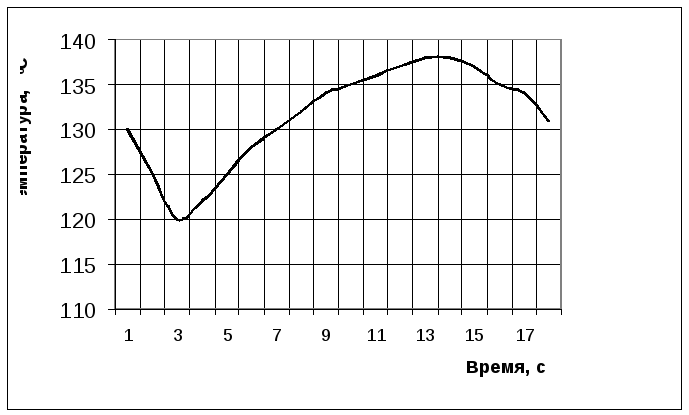
Рис. 2.5. Зависимость температуры от времени реакции сплава ФС 90 Ба4 с 13,3 %-ным раствором едкого натра (кинетический реактор),tнач= 130 °С.
После завершения скачка прибор показывает постепенное снижение температуры, что свидетельствует о завершении реакции в связи с полным разрушением частиц сплава.
С учетом принятой инерционности системы, экспериментальные значения температуры реакционной поверхности (tп) оказались равными температуре кипящей жидкости при критическом давлении.
В опыте №4 на конечной стадии реакции за 6 с температура поднялась со 130 °С до 137 °С – см. табл. 2.1. Ввиду кратковременности существования тонкого реагирующего слоя и инерционности системы реальная величина температуры составила 266 °С. Фактический скачок равен 134 °С. В пересчете на полупериод реакции (7,5 с) подъем температуры происходит от 100 °С до 194 °С, т.е. всплеск составляет 94 °С. Величина 194 °С является температурой насыщения при критическом давлении, зафиксированная в момент времени, соответствующий αr = 0,5.
При повышении начальной температуры реакции для сплава ФС 90 Ба4от 90 до 130 °С скорость выделения водорода увеличивается в 5 раз – см. табл. 2.1 и рис. 2.5, 2.6.
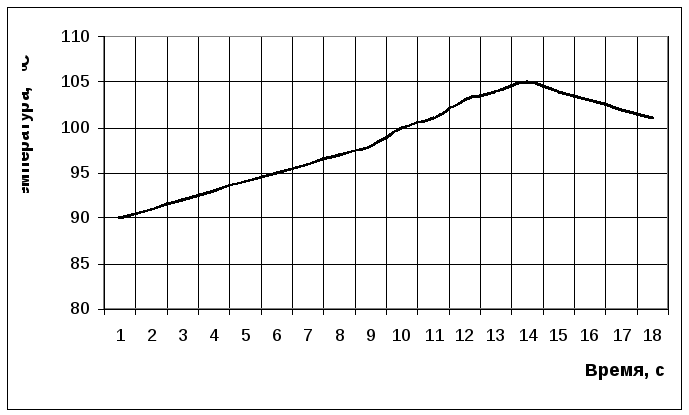
Рис. 2.6. Зависимость температуры от времени реакции сплава ФС 90 Ба4 с
13,3 %-ным раствором едкого натра (кинетический реактор),tнач= 90 °С.
Для сравнения были проведены исследования со сплавом на основе алюминия А-98КаМг. Методика ведения опыта не отличается от описанной выше.
При взаимодействии сплава А-98КаМг с водным раствором едкого натра за 7 с температура поднялась с 88 до 95 °С - рис. 4.7. Скорость реакции равна W = 8,9∙10–3 м3/(кг∙с). Индукционный период составил 3 с. Повышение концентрации щелочи от 10 % до 13,3 % приводит к возрастанию скорости реакции – см. табл. 2.1, опыт № 7.
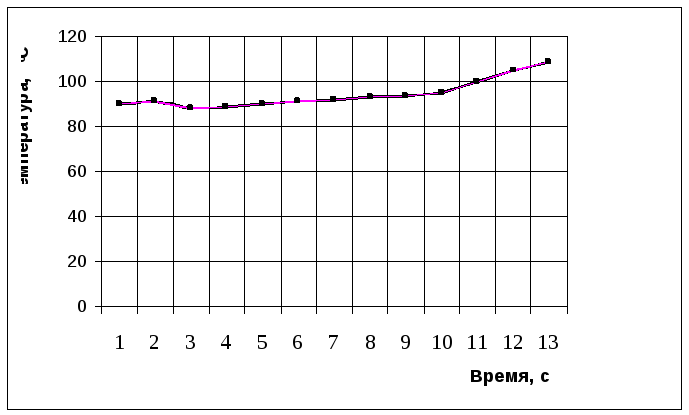
Рис. 2.7. Зависимость температуры от времени реакции сплава А-98 КаМг
с 10 %-ным раствором едкого натра (кинетический реактор),tнач= 90 °С.
2.2.1 Оценка зависимостей по теплоотдаче
При омывании неподвижной реагирующей частицы обнаружено более существенное влияние критерия Рейнольдса для сплава ФС 90 Ба4
Nu = 0,9∙10–7 Re1,8 Pr0,33. (2.1)
Значение приведенной скорости жидкости, найденное по разработанной методике, находится в пределах 1,77 - 2,26 м/с. Числа Рейнольдса изменяются от 110000 до 160000 (табл. 2.2). Поскольку коэффициент лобового сопротивления kлс в указанном интервале возрастает – следует ожидать увеличения безразмерного коэффициента теплоотдачи с ростом чисел Рейнольдса.
Установление величин температурного напора и скорости омывания частиц жидкостью позволили рассчитать осредненное значение коэффициента теплоотдачи и удельную тепловую нагрузку.
Обработка экспериментальных данных проведена по известным зависимостям. Расчеты выполнены на момент равный полупериоду реакции (αr = 0,5). Результаты представлены в таблице 2.2 и на рисунках 2.8 - 2.10.
Оказалось, что наименьшее отклонение дает формула Кунии, а наибольшее – формула Кацнельсона - Тимофеевой. В упомянутых работах степень влияния чисел Рейнольдса находится в пределах 0,5 - 0,58. Для активированного алюминия АГ5О5И5 (масс.%: Al - 85, Ga - 5, Sn - 5, In - 5) степень влияния числа Рейнольдса составила 1,6.
Отклонение расчетных значений критерия Нуссельта от экспериментальных не превышает ± 15%.
С ростом скорости омывания возрастает паро- и газообразование, что сопровождается турбулизацией пограничного слоя.
Близкие условия тепломассообмена наблюдаются при испарении воды в собственные перегретые пары.
|
Температура среды в реакторе, td,°С |
Температура на реакционной поверхности, tнас,°С |
Среднелогарифмическая разность температур, ∆tср,°С |
Давление в реакторе, Ре, МПа |
Давление на реакционной поверхности, Рнас, МПа |
Время полуреакции, τ, с (αr = 0,5) |
Скорость выделения водорода, Wτ∙106, м3/с |
Радиус сферы эквивалентного объема, Rτ∙103, м |
Скорость выделения водорода, Wτ∙103, м3/(м2∙с) |
Диаметр подъемного потока, dп.п∙103, м |
Скорость жидкости в потоке, νпр, м/с |
Число Рейнольдса |
Число Прандтля |
Число Нуссельта |
Значения чисел Нуссельта, рассчитанные по зависимостям в литературе: |
Величины коэффициентов теплоотдачи, α, Вт/(м2∙К), определенных согласно: | ||||||
|
Re |
Pr |
Nu |
Nu1 |
Nu2 |
Nu3 |
Опытным данным, α |
α1 |
α2 |
α3 | ||||||||||||
|
98 100 101 128 130 137 |
181 192 207 238 251 265 |
21,7 23,5 26,2 26,9 29 30,3 |
0,42 0,44 0,48 0,68 0,76 0,84 |
0,77 0,81 0,93 1,28 1,47 1,61 |
1440 1470 1500 390 450 630 |
1,9 2,1 7,2 2,4 9,2 9,7 |
5,64 5,61 5,45 5,49 5,37 5,26 |
0,18 0,2 0,3 13,4 13,8 17,1 |
16,95 16,74 18,21 16,14 16,43 16,66 |
2,2 2,1 1,77 2,26 2,18 2,12 |
123804 119166 110269 158869 158484 163363 |
1,78 1,74 1,76 1,55 1,31 1,23 |
159,8 148,1 129,3 239,2 225,4 233,1 |
257,3 250,6 242,1 278,4 263,1 261,6 |
276,4 269,1 259,4 300,5 284 282,6 |
403,1 391,3 375,6 444,5 422,1 420,3 |
6433,4 6042,5 4851,8 10166,7 9411,1 9588,4 |
10358,6 10224,6 9083 11832,8 10896 10760,7 |
11127,7 10976,1 9732,1 12772,2 11857,8 11624,6 |
16225,4 15965,2 14091,7 18893,9 17627,6 17289,6 | |
Таблица 2.2
