
- •Глава 1. Вступ до генетики поведінки тварин.
- •Глава 7. Феногенетика поведінки птахів.
- •Глава 8. Генетика поведінки ссавців.
- •Глава 1. Вступ до генетики поведінки тварин.
- •Варіант батареї тестів для фенотипування тварин
- •Глава 2. Шляхи реалізації генетичної інформації на рівні поведінки.
- •2.1. Генетика морфологічних особливостей нервової системи та їх зв'язок з мінливістю ознак поведінки.
- •2.2. Зв'язок поведінки з деякими біохімічними показниками.
- •2.3. Гормональна регуляція мінливості ознак поведінки та ендокринологічна генетика.
- •Глава 3. Генетика поведінки бактерій.
- •3.1. Генетичні засади соціальної поведінки бактерій.
- •3.2. Генетика хемотаксису бактерій.
- •3.3. Самоідентифікація та взаємне упізнавання бактерій.
- •Глава 4. Генетика поведінки одноклітинних тварин.
- •4.1. Особливості поведінки одноклітинних тварин.
- •4.2. Генетика поведінки інфузорій.
- •4.3. Генетика поведінки Dictyostelium discoideum.
- •Глава 5. Генетика поведінки безхребетних тварин.
- •5.1. Генетика поведінки круглих черв’яків.
- •5.2. Генетика поведінки молюсків.
- •5.3. Генетика поведінки комах.
- •5.3.1. Комахи як об’єкт генетики поведінки.
- •5.3.2. Вплив окремих генів на поведінку комах.
- •5.3.3. Деякі аспекти генетики поведінки суспільних комах.
- •5.3.4. Генетичні засади нейрогуморальної регуляції поведінки комах.
- •5.3.5. Еволюційні аспекти поведінки комах.
- •Глава 6. Генетика поведінки дрозофіли.
- •6.1. Історія вивчення поведінкових мутацій дрозофіли.
- •6.2. Зорові мутації дрозофіли.
- •6.3. Мутації рухової системи в дрозофіли.
- •6.4. Температурочутливі мутації в дрозофіли
- •6.5. Мутації, що порушують циркадні ритми в дрозофіли
- •6.6. Мутації, що змінюють статеву поведінку дрозофіли.
- •6.7. Використання мозаїків для виявлення структур, що порушені при поведінкових мутаціях.
- •6.8. Метод локалізації фокуса дії мутації на карті презумптивних органів дрозофіли.
- •6.9. Селекційно-генетичний метод в аналізі поведінки дрозофіли.
- •Глава 7. Феногенетика поведінки птахів.
- •7.1. Птахи як об'єкт генетичного аналізу поведінки.
- •7.2. Середовищна модифікація деяких форм уродженої поведінки птахів.
- •7.3. Імпринтинг і його роль у постнатальному онтогенезі виводкових птахів.
- •7.4. Гібридологічний аналіз поведінки птахів.
- •7.5. Окремі гени й ознаки поведінки птахів.
- •7.6. Еволюційна модифікація поведінки птахів.
- •Глава 8. Генетика поведінки ссавців.
- •8.1. Генетика поведінки собак.
- •8.2. Генетика поведінки гризунів.
- •8.3. Генетика поведінки кішок.
- •Таблиця ___ Типи спадкування деяких ознак і аномалій у кішок
- •8.4. Генетика поведінки коней і великої рогатої худоби.
- •8.5. Генетика поведінки лис.
4.3. Генетика поведінки Dictyostelium discoideum.
Dictyostelium discoideum (діктіостеліум) – це клітиннийслизьовик, відноситься до типу Mycetozoa. Описаний у 1935 році діктіостеліум незабаром став одним з найцікавіших об’єктів у клітинній біології, генетикці й біології розвитку.

Рис. 4.4. Dictyostelium discoideum – модельний об’єкт клітинної біології, генетики та біології розвитку.
Більшу частину життя діктіостеліум проводить у вигляді одиночних ґрунтових амеб, однак за певних умов ці амеби утворять рухливі агрегати, а потім багатоклітинні плодові тіла складної будови. Процеси міжклітинної сигналізації, клітинного диференціювання й морфогенезу, що відбуваються при цьому, дозволяють використовувати цей організм як модельний об'єкт.
У природі Dictyostelium discoideum живе в ґрунті й підстилці (вологому листовому опаді). Одиночні амеби харчуються в основному бактеріями – їх залучає виділювана бактеріями фолієва кислота.
Життєвий цикл діктіостеліуму починається з того, що його спори вивільняються зі зрілих плодових тіл і розносяться вітром. При досить високій вологості й температурі зі спор виходять міксамеби – одноклітинна стадія розвитку діктіостеліуму. При достатній вологості й наявності їжі вони харчуються й діляться за допомогою мітозу.
При вичерпанні їжі починається агрегація міксамеб. На цій стадії в клітинах міксамеб синтезуються специфічні глікопротеїди і аденілатциклаза. Глікопротеїди забезпечують міжклітинну адгезію, а адінилатциклаза синтезує цАМФ.

Рис. 4.5. Утворення цАМФ
цАМФ, що секретується у середовище, слугує, як і в бактерій, сигналом «клітинного голоду». У дітіостеліуму цАМФ також є хемоатрактантом для голодних міксамеб. Кілька випадково міксамеб, які опинилися поряд і «склеїлися» першими слугують центром, до якого приваблюються й повзуть із усіх боків голодні міксамебы. З'єднуючись за допомогою молекул клітинної адгезії, вони утворюють агрегат з кількох десятків тисяч клітин.
Спочатку плаский агрегат робить складні рухи, піднімається над субстратом, а потім лягає на бік і перетворюється в мігруючого «слизняка» – рухливий псевдоплазмодій довжиною 2-4 мм.
Псевдоплазмодій мігрує увесь час одним кінцем уперед, і в його складі починається диференціювання клітин. Частина клітин на передньому кінці утворять полісахаридну оболонку. Псевдоплазмодій мігрує крізь неї, і якась її частина залишається на субстраті у вигляді слизового сліду.
Псевдоплазмодій рухається в напрямку до світла, більш високої температури й більшої сухості повітря.
цАМФ і речовина, відома як фактор індукції диференціювання (DIF), стимулюють подальше диференціювання й формування кількох типів клітин.
На передньому кінці псевдоплазмодію опиняються клітини – попередники стеблинки плодового тіла, а на задньому – клітини-попередники спор. «Подібні до передніх» (аnterior-like) клітини, відкриті порівняно нещодавно, розподілені по задній половині тіла псевдоплазмодію. Ці клітини формують підставку (найнижчу частину плодового тіла). Після закінчення міграції у придатні умови клітини псевдоплазмодію здійснюють складні переміщення й формують відповідні частини плодового тіла.
Після зупинки псевдоплазмодію за рахунок переміщення клітин формуються «стадія сомбреро», а потім починається кульмінаційна фаза формування плодового тіла.
У ході цієї фази передні й задні клітини псевдоплазмодію міняються місцями. Передні клітини «сомбреро» формують целюлозні клітинні стінки й збираються в порожню трубчасту стеблинку, по зовнішній поверхні якої клітини-попередниці спор мігрують нагору, а інші клітини — попередниці підставки – долілиць.
Цілком сформоване плодове тіло висотою 1-2 мм утвориться через 8-10 годин після початку цієї фази. Після дозрівання спор на його вершині, вони розсіюються, і цикл починається знову.

Рис. 4.6. Плодове тіло Dictyostelium discoideum
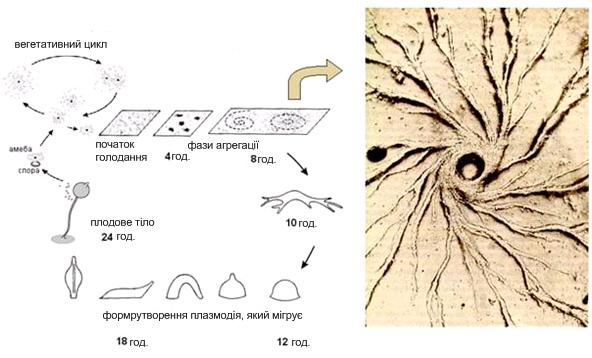
Рис. 4.7. Життєвий цикл Dictyostelium discoideum

Рис. 4.8. Мікрофотографії життєвого циклу Dictyostelium discoideum
Крім описаної вище безстатевої частини циклу, у життєвому циклі діктіостеліуму може відбуватися й статеве розмноження. Перехід до статевого розмноження може запускатися підсиханням підстилки, де живуть міксамебы. Зливаючись, дві миксамеби різних типів парування утворюють зиготу – «гігантську клітину». Зигота починає заковтувати навколишніх міксамеб. Проковтнувши кілька сотень міксамеб, зигота виділяє товсту целюлозну оболонку, формуючи так звану макроцисту.
Макроциста ділиться спочатку за допомогою мейозу, а потім за допомогою мітозу, формуючи безліч гаплоїдних міксамеб. Виходячи з-під оболонки макроцисти, вони починають харчуватися й розмножуватися безстатевим шляхом. Таким чином, у життєвому циклі Dictyostelium discoideum єдина диплоїдная стадія – це зигота.
Переваги діктиістеліуму як модельного об'єкта – відносно проста будова, невелике число типів клітин, а також короткий життєвий цикл і простота вирощування в лабораторних умовах.
Хемотаксис у Dictyostelium discoideum вивчається на прикладі руху міксамеб у напрямку до джерела секреції цАМФ. У секреції цАМФ і швидкості пересування міксамеб спостерігається циклічність із певним періодом. Цікаво, що використання цАМФ у якості хемоатрактанту не описане в жодного іншого організму. У прокаріотичних і тваринних клітинах цАМФ слугує внутрішньоклітинним сигналом, а Dictyostelium discoideum –єдиний організм, у якого цАМФ діє ще і як позаклітинна сигнальна молекула.
При формуванні плазмодія окремі клітини слизовика агрегують у результаті хемотаксису. Одна з реакцій на голодування в міксамеб полягає в тому, що вони починають виробляти й виділяти цАМФ, що слугує хемотаксичним сигналом, який приваблює інших міксамеб. Агрегація ініціюється випадковим чином: будь-які клітини, що починають першими секретувати цАМФ, приваблюють інші клітини й у такий спосіб стають центрами агрегації. цАМФ, вироблюваний такими «клітинами-ініціаторами», секретується окремими «імпульсами» і зв'язується специфічними рецепторами на поверхні сусідніх голодуючих амеб, спрямовуючи тим самим їхній рух убік джерела цАМФ.
Таку хемотаксичну відповідь можна продемонструвати, наносячи з мікропіпетки незначну кількість цАМФ на будь-яку ділянку поверхні клітини голодуючої міксамеби. Відповіддю буде негайне утворення псевдоподії, що росте убік піпетки. Псевдоподія прикріплюється до поверхні, на якій перебуває клітина, і тягне клітину в тім же напрямку. Як тільки утвориться центр агрегації, зона його впливу швидко розширюється, тому що агрегуючі клітини не тільки відповідають на сигнал цАМФ, але й передають його від клітини до клітини.
Кожен імпульс цАМФ спонукає сусідні клітини не тільки до руху до джерела імпульсу, але й до випущення власного імпульсу у вигляді цАМФ. Цей новий, що вивільняється з невеликою затримкою імпульс у свою чергу орієнтує клітини, що перебувають поруч, викликаючи в них теж викид цАМФ, і т.д.
У такий спосіб виникають регулярні хвилі цАМФ, що чергуються та поширюються з кожного центра агрегації, змушуючи більше віддалених міксамеб рухатися усередину концентричними або спіральними хвилями. Перевага такої системи передачі полягає в тому, що в міру розповсюдження із центру сигнал постійно відновлюється, не послабляючись на великій відстані.
Крім активації сигнальної системи цАМФ голодування міксамеб Dictyostelium викликає експресію сотень нових генів, і деякі з них кодують молекули міжклітинної адгезії, що беруть участь в агрегації клітин.
Амеби Dictyostelium в останні роки стали улюбленим об'єктом біологів, що вивчають еволюцію кооперації й соціальної поведінки. Учених цікавлять скупчення одноклітинних індивідуумів, які створюють ідеальні умови для розвитку соціального паразитизму й нахлібництва. Для того щоб вижити начебто соціальним організмам діктіостеліуму необхідно якимось чином захищатися від нахлібників.
Дослідження на діктіостеліумі, показали, що ймовірність розвитку стійкості в результаті випадкових мутацій у цього організму досить висока. Учені працювали із двома штамами діктіостеліуму – «чесними» амебами дикого типу (умовна позначка штаму – AX4) і одним з кількох відомих штамів амеб-«ошуканців» (chtC). Якщо змішати амеб із цих штамів у рівній пропорції й почати морити їх голодом, вони утворять химерні (змішані) плодові тіла. При цьому «ошуканці» посідають кращі місця в плодовому тілі й перетворюються на спори, у той час як «чесні» амеби будують ніжку плодового тіла. У результаті серед спор, що утворилися, різко переважають спори ошуканців.
Учені штучно підвищили темп мутування в «чесних» амеб AX4 за допомогою генетичних конструкцій (плазмід), що вмонтовуються в різні ділянки геному діктіостеліуму. До складу плазміди входив ген стійкості до антибіотика бластицидину S. Вмонтовуючись у різні місця геному, ця плазміда впливала на роботу прилеглих генів. Потім з безлічі отриманих амеб-мутантів взяли тисячу особин з різними мутаціями й кожній з них дали можливість розмножитися.
Після цього сталі вести добір на стійкість до нахлібників. Амеб з тисячі мутантних штамів змішували в рівній пропорції й поєднували з амебами-ошуканцями, причому останніх було в чотири рази більше, ніж чесних амеб-мутантів. Змішану популяцію морили голодом, змушуючи утворювати плодові тіла. Потім збирали спори, що утворилися, і виводили з них амеб. Природно, серед них переважали ошуканці chtC, але експериментатори вбивали їх всіх бластицидином S (адже всі амеби-мутанти мали ген, що захищає їх від цього антибіотика). У результаті утворювалася суміш амеб-мутантів, але з тисячі вихідних штамів у ній тепер переважали ті, хто зміг краще інших протистояти ошуканцям. Цих амеб знову змішували з ошуканцями в пропорції 1:4 і знову змушували утворювати плодові тіла.
Після шести таких циклів у популяції амеб-мутантів залишилися представники тільки одного з тисячі вихідних штамів. Автори досліджували геном цих амеб і з'ясували, що плазміда в них вмонтувалася в ген DDB_G0271758, що кодує білок з невідомою функцією.
Мутантний штам, що вижив, назвали rccA (resister of cheater chtC A).
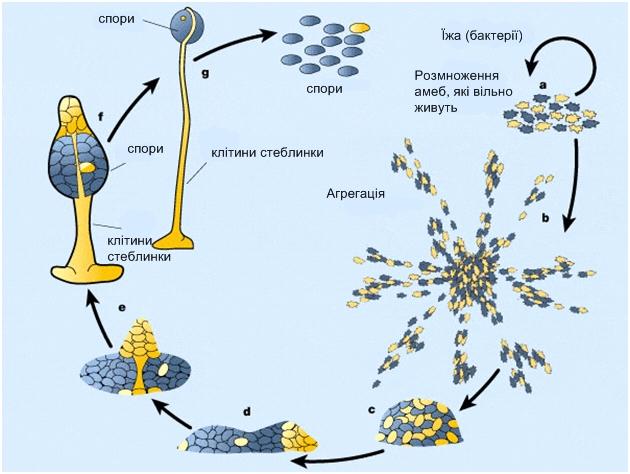
Рис. 4.9. Соціальний паразитизм у Dictyostelium
а – при надлишку їжі амеби живуть поодинці, ростуть і розмножуються безстатевим шляхом (поділом); b–c – при нестачі їжі амеби збираються в великі скупчення. d – у результаті утворюються багатоклітинні агрегати довжиною в кілька міліметрів. e–g –багатоклітинний агрегат перетворюється на «плодове тіло» на ніжці; при цьому близько 20% клітин жертвують собою, створюючи ніжку (жовті клітини - «чесні»), а 80% перетворюються на спори й отримують шанс продовжити свій рід (сині клітини- «ошуканці»).
Автори переконалися, що амеби rccA дійсно захищені від нахлібництва з боку ошуканців-chtC. Якщо змішати тих і інших у рівній пропорції, то спори в химерних плодових тілах утворяться теж у рівній пропорції — отже, шахрайські прийоми амеб chtC, у чому б вони не полягали, безсилі проти амеб rccA. Однак інший штам амеб-ошуканців, LAS1, успішно паразитував на амебах rccA. Отже, мутація в гені DDB_G0271758 захистила амеб не від будь-яких ошуканців, а тільки від цілком визначених.
Дослідники також перевірили, чи не став стійкий штам rccA сам «ошуканцем» стосовно вихідного штаму AX4. Теоретично, один зі способів здолати ошуканця в еволюційній «гонці озброєнь» — це самому стати ще більш митецьким ошуканцем. Подібне змагання між ошуканцями в підсумку може призвести всю систему, засновану на кооперації, до повного краху. Однак у цьому випадку цього не відбулося: штам rccA залишився цілком «чесним» стосовно AX4.
Експерименти зі змішаними культурами, що складаються з рівної кількості амеб AX4 («диких»), chtC («ошуканців») і rccA («захищених»), показали, що амеби rccA захищають від обману не тільки себе, але й диких амеб AX4 (хоча й у трохи меншому ступені). Присутність амеб rccA якимсь чином заважає ошуканцям chtC витісняти амеб AX4 з вигідних позицій у плодових тілах. Ясно, що взаємодопомога чесних штамів відкриває додаткові можливості для боротьби з ошуканцями.
Дослідження показало, що ймовірність появи мутацій, що забезпечують захист від нахлібників, у діктіостеліуму досить висока. Присутність нахлібників сприяє поширенню захисних мутацій. Це повинне приводити до еволюційної «гонці озброєнь» між ошуканцями й чесними амебами: перші вдосконалюють засоби обману, другі – засоби захисту. Для того щоб захиститися від ошуканців, амеби не зобов'язані самі ставати ошуканцями. Це сприяє збереженню кооперації.
Генетичні механізми обману й захисту від нього поки залишаються невідомими, але швидше за все вони пов'язані із системами міжклітинної комунікації й взаємного упізнавання.
Питання для повторення й обговорення.
1. Які поведінкові реакції одноклітинних тварин вивчає генетика поведінки?
2. Які таксиси є у одноклітинні тварини?
3. Наведіть приклади складних спеціалізованих рецепторів в одноклітинних тварин.
4. Доведіть, що одноклітинні тварини мають досить складними поведінковими реакціями.
5. Чи можуть одноклітинні тварини використовувати попередній «досвід»?
6. Чим компенсується в одноклітинних тварин відсутність оперативної індивідуальної пам'яті?
7. Що ви знаєте про поведінкові мутаціях Paramecium aurelia?
8. Чи можуть поведінкові мутації Paramecium aurelia успадковуватися згідно законам Менделя?
9. У чому полягають незвичайні особливості геному Paramecium aurelia?
10. У чому переваги діктіостеліума як модельного об'єкта генетики поведінки?
