
Гнойно-воспалительные осложнения при черепно-мозговой травме
2 7
7
ГНОЙНО-ВОСПАЛИТЕЛЬНЫЕ
ОСЛОЖНЕНИЯ ПРИ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЕ
АЛ.Парфенов, В.Г.Амчеславский, И.А.Александрова, И.А.Арефьева, А.Г.Гаврилов
Гнойно-воспалительные осложнения (ГВО) у больных в остром периоде тяжелой черепно-мозговой травмы (ТЧМТ) представляют одну из важнейших проблем нейрореаниматологии, решение которой способно в значительной степени снизить летальность, уменьшить продолжительность пребывания больного на реанимационной койке и существенно улучшить исходы заболевания (61).
Возникая в процессе лечения в стационаре, ГВО у больных с тяжелой черепно-мозговой травмой, по определению ВОЗ, являются нозокомиальной (госпитальной) инфекцией.
Распределение инфекций в отделении интенсивной терапии (ОИТ) отличается от других отделений. В отделениях общего профиля превалируют инфекции мочевыводящих путей и раневая инфекция, в то время как в ОИТ наиболее частой является инфекция нижних дыхательных путей (45 %), и, прежде всего пневмония (около 30 %). Сходные данные о преобладании в ОИТ инфекций нижних дыхательных путей получены в 1992 году в ходе многоцентрового исследования, проведенного в 1417 отделениях интенсивной терапии в 17 странах Европы — (European Prevalence of Infection in Intensive Care-«EPIC-study») (20).
Частота развития инфекционных осложнений у больных в ОИТ в 5—10 раз выше, чем у больных в отделениях общего профиля и составляет от 7 до 32 %, увеличиваясь до 48—79 % у больных, находящихся на искусственной вентиляции легких (ИВЛ). Структура инфекционных осложнений в ОИТ распределяется следующим образом: 1-е место занимает пневмония — 79 % всех осложнений, затем следует уроинфекния — 15—20%, раневая — 13% и ангиогенная инфекция — 9 %. Наиболее частыми и
опасными среди них являются инфекции нижних дыхательных путей, летальность при которых в среднем составляет 33 % (5, 20).
Известно, что ГВО (как внутричерепные, так и внечерепные) относятся к факторам, обусловливающим развитие «вторичных» повреждений мозга.
Установлено, что внутричерепная инфекция осложняет течение тяжелой черепно-мозговой травмы в 5—8 % случаев и проявляется в виде абсцессов мозга и/или менингита. Инфицирование происходит через поврежденную твердую мозговую оболочку, чаще при проникающих повреждениях, вдавленных переломах или при переломах основания черепа (8, 9, 51).
Сложность борьбы с церебральными инфекционными осложнениями, прежде всего связана с наличием гематоликворного и гематоэнцефаличес-кого барьеров, затрудняющих проникновение многих антибиотиков в патологический очаг при парентеральном их применении. Введение же антибиотиков эндолюмбально или непосредственно в мозговую рану чревато опасностью нейротоксичес-кого и эпилел тоге иного действия.
Экстракраниальные инфекционные осложнения у больных с тяжелой черепно-мозговой травмой доминируют над интракраниальными. По мнению ряда авторов (44, 49, 78, 46), наиболее часто поражаются дыхательная система, мочевыводящие пути и сосудистая система.
Основным ГВО у больных с ТЧМТ по частоте и тяжести течения заболевания является пневмония, которая нередко выступает в качестве основной причины смерти (44).
В тяжелых случаях, течение пневмонии, уроин-фекции и раневой инфекции осложняется бакте-
435
Клиническое руководство по черепно-мозговой травме
 риемией
и сепсисом, что приводит к летальным
исходам
в подавляющем числе наблюдений (22, 25,
26,
40, 24, 85).
риемией
и сепсисом, что приводит к летальным
исходам
в подавляющем числе наблюдений (22, 25,
26,
40, 24, 85).
Тяжелые ГВО сочетаются с развитием синдрома эндогенной интоксикации (СЭИ), который сопутствует любому соматическому, инфекционному, хирургическому и другим заболеваниям (1, 11, 12, 14). СЭИ является интегративным фактором, в котором участвуют множество патогенетических феноменов: гипоксия, расстройства микроциркуляции, энергетический дефицит, мембранопатоло-гические процессы, рецепторные нарушения, изменения деятельности генома, накопление множества промежуточных субстанций патологического обмена веществ, развитие синдрома вторичного иммунодефицита и др.
Большое значение в формировании СЭИ имеет воздействие бактериальных и экзогенных токсинов, являющихся триггерами в каскадных реакциях образования эндогенных медиаторов липидной и белковой природы (тромбоксан, простациклин, лей-котриены, фактор активации тромбоцитов, интер-лейкины, фактор некроза опухоли и др.), которые в очень высоких концентрациях вызывают системные патологические реакции (I, 14, 16).
При критических состояниях на фоне нарастающего эндотоксикоза прогрессируют микроцирку-ляторные нарушения, тканевая гипоксия и метаболические расстройства, формируется вторичный иммунодефицит и полиорганная недостаточность (ПОИ), значительно усугубляющие течение основного заболевания.
27.1. Интрацеребральные
ГНОЙНО-ВОСПАЛИТЕЛЬНЫЕ ОСЛОЖНЕНИЯ
Посттравматические менингоэнцефалиты (ПМ) представляют большую опасность для жизни и серьезно влияют на течение заболевания и исход у больных перенесших ТЧ МТ.
Считается, что частота развития менингитов после черепно-мозговой травмы составляет от 0,2 до 17,8% (28).
Наиболее часто это осложнение развивается в течение первых 2 недель после травмы, хотя и известны случаи развития ПМ и в более поздние сроки (16). Вторичный менингит при ЧМТ различен по патогенезу и имеет смешанную бактериальную флору. Такие факторы как локализация и характер травмирующего агента, время до начала клинических проявлений менингита, наличие инородных
тел, абсцедирование мозга, ликворный свищ, обусловливают бактериологический диагноз, терапию и прогноз заболевания.
Среди факторов значительно повышающих вероятность развития менингита на первом месте стоит ликворея (29, 34). При этом, вероятность возникновения менигита тесно связана с продолжительностью ликвореи. Назальная ликворея встеча-ется примерно в три раза чаще чем ушная. При тяжелой черепно-мозговой травме около 25 % пострадавших имеют переломы основания черепа, из которых у 10 % выявляется ликворея (35).
Патогенез посттравматических менингитов тесно связан с анатомией твердой мозговой оболочки. При переломах основания черепа, то есть в местах где твердая мозговая оболочка особенно тесно прилегает к костям, почти всегда происходит ее разрыв часто с образованием ликворной фистулы (79, 80). Бактериальная флора, находящаяся в носо-, ротоглотке или во внутреннем ухе, проникая в лик-вор может явиться причиной менингита.
Перелом основания черепа, проходящий через параназальные пазухи является косвенным признаком возможной ликвореи (21,36).
Приведем пример: Больной В. 24 лет. Верифицированный диагноз: острая тяжелая открытая проникающая краниофациальная травма; многоочаговый ушиб головного мозга, перелом костей лицевого скелета справа.
Травма в результате ДТП. Обстоятельства неизвестны. Поступил через 1,5 часа после травмы. При поступлении: глубокая кома, спонтанное неадекватное дыхание, анизокория D > S, ушибленно-рваная рана правой теменной области, выделение мозгового детрита из раны, кровотечение из левого наружного слухового прохода, обширная подкожная гематома правой височ-но-теменной области, гематома век правого глаза.
После стабилизации витальных функций выполнена трепанация в правой височно-теменной области, удаление вдавленных фрагментов височной кости, отмывание мозгового детрита.
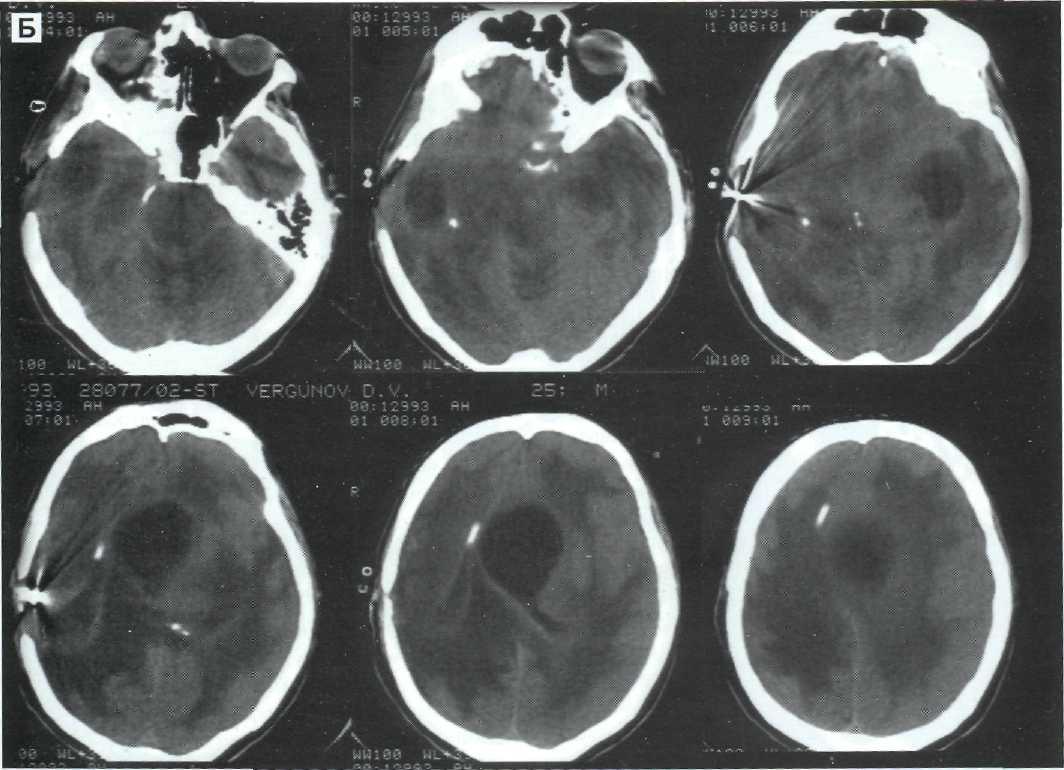
На серии КТ-снимков (рис. 27-1. А, Б) выявляются очаги гетерогенной плотности в полюсно-базаль-ных отделах правой лобной и височной доли, а так же теменно-височной области с мелкими костными фрагментами и металлическими клипсами. Признаки полушарного отека вещества мозга, со смещением срединных структур справа налево. Затемнение пазух решетчатой кости, основной пазухи, уровень жидкости в гайморовых пазухах с 2-х сторон. Назальная и ушная ликворея слева.
Несмотря на профилактику и активное антибактериальное лечение гнойно-воспалительных про-
436
Гнойно-воспалительные осложнения при черепно-мозговой травме

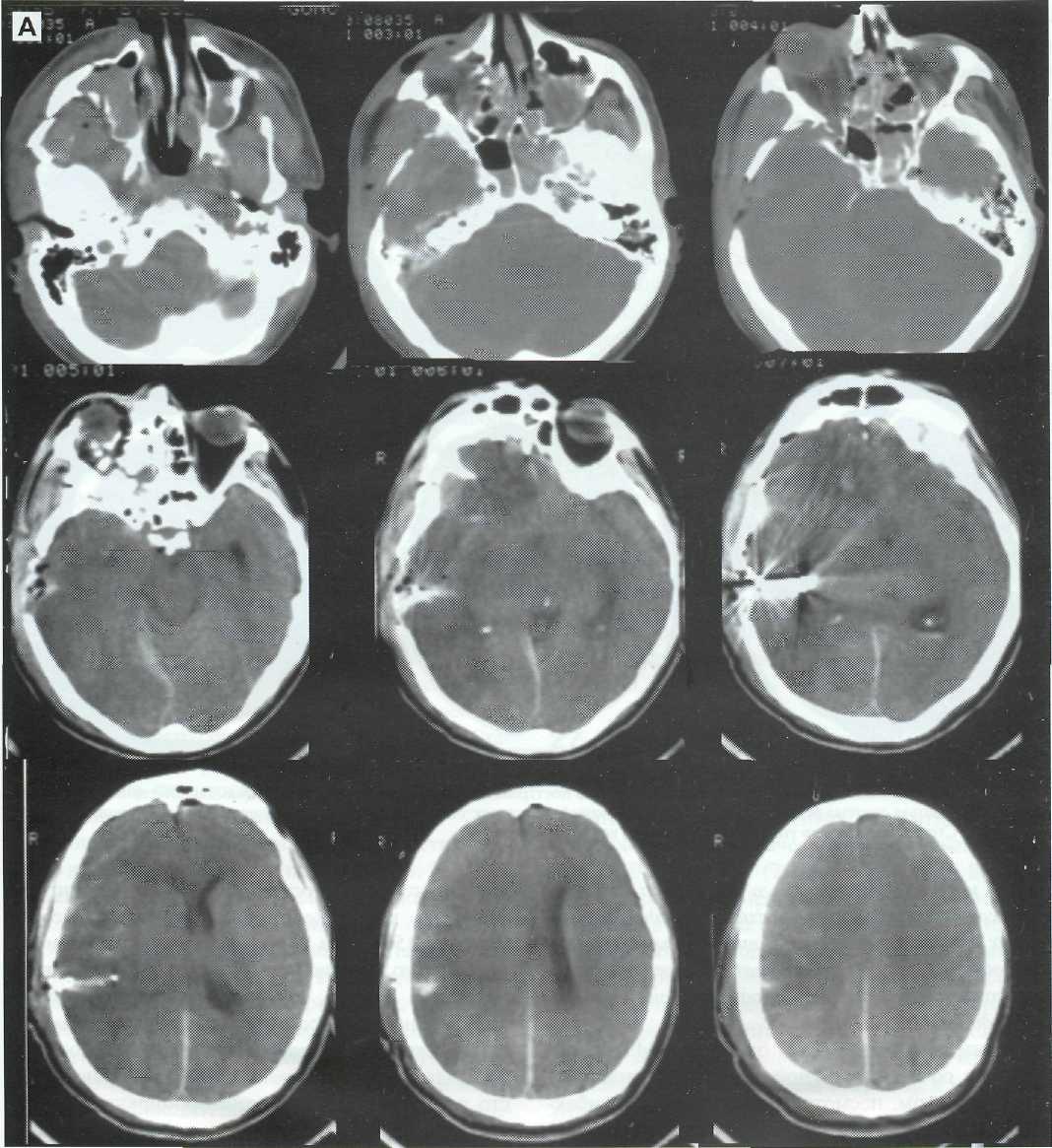
явлений, течение заболевания осложнилось развитием гнойного посттравматического гайморита слева с последующим развитием менингоэнцефали -та.
За время пребывания в стационаре перенес пневмонию, осложненную пневмотораксом, гнойный гайморит, менингоэнцефалит. Были произведены эндоскопическая эндоназальная санация правой клиновидной
Клиническое руководство по черепно-мозговой травме
пазухи и клеток решетчатого лабиринта, эндоскопическая пластика ликворной фистулы задних решетчатых клеток справа. При выписке больной в сознании, общителен. Речевой контакт умеренно ограничен, сохраняются редкие эпизоды подъема температуры до субфебрильных цифр.
Таким образом, тяжелая открытая ЧМТ, с лик-вореей в сочетании с гнойным посттравматическим синуситом, несмотря на массивную антибактериальную терапию, привела к развитию менин-гоэнцефалита.
Перелом пирамиды височной кости, тесно связанной со слуховым проходом, может явиться причиной ушной ликвореи.
Обычно ликворея продолжается несколько дней, но может длиться годами после черепно-мозговой травмы. В 90 % случаев ликворная фистула спонтанно закрывается в течение 7—10 дней; в 10 % — в течение периода времени, превышающим 1 месяц (39, 53, 71).
Симптоматика посттравматических менингитов такая же, как и менингитов не травматической природы (58). При постановке диагноза менигита необходимо идентифицировать патогенный микроорганизм. Ликвор, полученный при поясничной пункции не всегда соответствует ликвору в базаль-ных цистернах и желудочках мозга, поскольку у больных с тяжелой черепно-мозговой травмой часто имеются нарушения ликвороциркуляции. Более того, наличие нормальных показателей в лик-воре, взятом из желудочков мозга, полностью не гарантирует отсутствие менингита. Увеличение числа лейкоцитов и/или нейтрофилов в ликворе, предполагающее наличие менингита, может быть находкой неспецифических проявлений. Специальные методики такие как метод латексной агглютинации и метод иммуноэлектрофореза широко используются для выявления бактериальной флоры (Нето-philus influenzae, Neisseria meningitis u Streptococcus pneumonia).
438
Гнойно-воспалительные осложнения при черепно-мозговой травме
 Наличие
ликвореи может быть установлено
несколькими
способами. Простейший — при визуль-ном
обследовании. В ряде случаев
диагностирование
ликвореи бывает затруднено и, это
осложнение
может быть установлено только при
тщательном
оторинологическом обследовании.
Существенную
помощь в установлении ликвореи может
дать КТ
исследование, при котором отмечают
наличие воздуха.
В остром периоде черепно-мозговой
травмы
КТ-цистернография для диагностики
ликвор-ной
фистулы обычно не применяется из-за
высокого
риска осложнений вызванных люмбальной
пункцией
в условиях внутричерепной гипертензии,
а
также из-за большого количества
ложно-положительных
результатов при дифференциации дорожки
контраста и свежей крови. Методом выбора
для
диагностики ликворных фистул в этом
случае является
КТ высокого разрешения или
МРТ-цис-тернография.
Наличие
ликвореи может быть установлено
несколькими
способами. Простейший — при визуль-ном
обследовании. В ряде случаев
диагностирование
ликвореи бывает затруднено и, это
осложнение
может быть установлено только при
тщательном
оторинологическом обследовании.
Существенную
помощь в установлении ликвореи может
дать КТ
исследование, при котором отмечают
наличие воздуха.
В остром периоде черепно-мозговой
травмы
КТ-цистернография для диагностики
ликвор-ной
фистулы обычно не применяется из-за
высокого
риска осложнений вызванных люмбальной
пункцией
в условиях внутричерепной гипертензии,
а
также из-за большого количества
ложно-положительных
результатов при дифференциации дорожки
контраста и свежей крови. Методом выбора
для
диагностики ликворных фистул в этом
случае является
КТ высокого разрешения или
МРТ-цис-тернография.
Источником патогенной флоры у больных с менингитами преимущественно является носоглотка. При этом более чем у 80 % больных с тяжелой закрытой черепно-мозговой травмой, осложненной менингитами высевается S. Pneumoniae (51). Н. 1п-fluezae, S. pyogenes и N. meningitid.es также выявляются достаточно часто, особенно у больных с назальной ликвореей (62, 30). Менингит, обусловленный S. Pneumoniae часто сочетается с бактериемией. Стафилококки, грамотрицательные патогены и негемолитические стрептококки — основная причина посттравматических менингитов. (54).
Иногда развитие менингита нельзя четко связать с наличием ликворного свища (51, 56, 79). 75 % ПМ связано с наличием переломов основания черепа, а 58 % — с назальной ликвореей (47).
Особенности ЧМТ и временной интервал между ЧМТ и началом менингита важны для эмпирической терапии. Если у пострадавших, имеющих переломы костей черепа, осложненный ликвореей менингит развивается в течение 3 суток, то можно с большой долей вероятности предполагать наличие пневмококковой инфекции (55). У детей в возрасте от 6 месяцев до 6 лет, наличие менингита может быть связано с N. influenzae. При наличии открытой ЧМТ с сильно загрязненной раневой поверхностью, причиной возникновения менингита могут быть грамотрицательные микроорганизмы или/и Staphylococcus aureus.
Важнейшая причина ПМ — инфицирование микроорганизмами, населяющими полость носа. Среди наиболее распространенных возбудителей — грамположительные кокки (S. haemolyticus, S.war-neri, S. cochnii, S.epidermidis и Streptococcus pneumonia.
Среди грам-отрицательных возбудителей — Esche-rishia coli, Ktebsiella pneumonia, Acinetobacter anitratus (23). В этой связи, важнейшим аспектом лечения ПМ является адекватная антибиотикотераиия. Эффективность адекватной антибиотикотерапии ПМ в первую очередь связана с наличием гемато-энцефалического и гематоликворного барьера (ГЭБ и ГЛБ).
Структура сосудов головного мозга устроена таким образом, что замедляет прохождение некоторых антибиотиков из крови в ликвор и внеклеточную жидкость мозговой паренхимы (41). Пассаж многих веществ в ликвор блокирован базальными мембранами и плотными участками клеток капиллярного эндотелия, а также отсутствием трансэн-дотелиальных каналов.
Характеристики антибиотика, которые влияют на его пассаж в ликвор, включают способность антибиотика растворяться в жирах, степень его ионизации, способность связывания антибиотика с белком, и серологические реакции.
Воспалительные процессы подобные менингиту и энцефалиту, способствуют увеличению пассажа антибиотика в цереброспинальную жидкость (41), что, однако не позволяет в полной мере преодолеть ГЭБ и ГЛБ.
27.1.1. Послеоперационные менингиты
Частота послеоперационных менингитов, после «чистых» нейрохирургических вмешательств составляет от 0,5 до 0,7 % (73, 46, 63, 84, 38). В других случаях, развитие менингита после краниотомии возникает в пределах от 0,4 до 2 %. В основе патогенеза послеоперационных менингитов обычно лежит непосредственное попадание возбудителей из пазух или с загрязненного скальпа. Гематогенный путь развития менигита весьма редок. Половина из случаев послеоперационных менигитов возникает в пределах двух суток после операции и характеризуется острым началом.
Диагностика менингита основана на особенностях клинической картины и данных исследования ликтора. Наиболее распространенные изменения в ликворе — это значительное повышение концентрации белка и уменьшение концентрации глюкозы менее чем на 50 % от ее концентрации в крови; значительное (более ЮОО/мм3) количество лейкоцитов при сдвиге формулы в сторону нейтрофилов.
В случаях послеоперационных менингитов наиболее часто высеваются Klebsiella pneumoniae, Enterobacter species и Pseudomonas aeruginosa (45, 86).
439
Клиническое руководство по черепно-мозговой травме
 27.1.2.
Инфекция
при
наружном
дренировании
27.1.2.
Инфекция
при
наружном
дренировании
Возникновение инфекции у больных с наружным дренированием или при установлении датчиков встречается в пределах от 4,5 до 14 % случаев. При этом, частота развития инфекции при люмбопе-ритонеальном шунтировании меньше чем при вен-трикулоперитонеальном или вентрикуловенозном шунтировании (82, 83).
Факторами риска развития инфекции являются повышение внутричерепного давления, внутриже-лудочковое кровоизлияние и интракраниальное нахождение датчиков более 5 суток (74, 32). При установке резервуаров, собирающих цереброспинальную жидкость, развитие инфекции возникает в пределах от 3 до 15 % случаев. Наиболее вероятное развитие инфекции отмечено в сроки до 30 дней после установки дренажа (81).
Важнейшими факторами развития шунт-ассо-циированных менингитов являются ретроградное попадание возбудителей по дренажу; раневая инфекция, связанная с установкой дренажа или нагноением послеоперационной раны и, самая редкая причина — гематогенная колонизация шунта патогенными микроорганизмами (57, 70).
Щунт-ассоциированпые менингиты всегда сопровождаются характерной клинической картиной. Появляются выраженные клинические и лабораторные признаки воспалительных проявлений (высокая лихорадка, головная боль, тошнота и рвота, снижение уровня бодрствования и изменения ментального статуса, высокий лейкоцитоз со сдвигом лейкоцитарной формулы, признаки эндогенной интоксикации и др.). Менингиальные симптомы при инфицировании интравентрику-лярно установленных шунтов возникают значительно реже, чем при инфицировании люмбопе-ритонеальных шунтов. Инфицирование шунтов, установленных в сосудистую систему, всегда связано с бактериемией.
27.2. БАКТЕРИЕМИИ
Бактериемия может возникать вторично при наличии любого очага гнойно-воспалительной инфекции. Наиболее четкая связь прослеживается между бактериемией и септическим эндокардитом. Однако в большинстве случаев возникновение бактериемии вызвано другими причинами. Главнейшие из них: катетер-ассоциированная бактериемия и бактериемия, обусловленная транслокацией патогенной флоры из ЖКТ (52).
Сосудистые катетеры ответственны за возникновение 10—15 % случаев всех госпитальных инфекций (54). Частота инфекций, вызванных ими, по данным различных авторов варьирует в широких пределах, составляя в среднем 7—8 % при катетеризации центральных вен и применении артериальных катетеров (54, 50, 66). Катетерный источник бактериемии может быть доказанным лишь в том случае, если один и тот же возбудитель выделен из гемакультур и с дистального конца катетера, и, если на катетере имеется компактный рост возбудителя (68).
Механизмы возникновения бактериемии вследствие катетеризации могут быть следующими: 1. инфицирование раневого канала с развитием бактериемии при установке катетера в не стерильных условиях; 2. попадание бактерий через соединения в ин-фузионной системе; 3. миграция бактерий вдоль канала, созданного катетером; 4. оседание и колонизация катетера бактериями, уже находящимися в крови (68). Последний механизм бактериемии наиболее доказан и обоснован. Источником бактериемии у реанимационных больных, по данным литературы, в подавляющем большинстве случаев служит ЖКТ. Развитию септицемии, обусловленной кишечной флорой, способствуют два фактора: — снижение кислотности в ЖКТ, при котором происходит бурный рост патогенной флоры и, повреждение защитного барьера слизистой оболочки кишечника, разделяющего кишечную микрофлору и кровоток.
Доказательством этого источника бактериемии служит идентичность возбудителей в кишечнике и в смыве с кончика внутри со суди сто го катетера(68). В структуре патогенной флоры около 50 % составляют стафилококки, а также грибы рода Candida и различные грамотрицательные микроорганизмы, обитающие в кишечнике (50).
В качестве иллюстрации катетер-ассоциирован-ной пневмонии может служить следующее наблюдение: Б-ная М., 35 лет. Верифицированный диагноз: тяжелая сочетанная черепно-мозговая травма, ушиб головного мозга тяжелой степени, перелом затылочной кости. Перелом большой берцовой кости левой голени.
Травма в результате ДТП (сбита автомашиной). Поступила в коматозном состоянии через 40 мин с момента травмы. Течение заболевания осложнилось развитием ГВО — посттравматическим синуситом, двусторонней пневмонией. Больная получала массивную инфузионную терапию через катетер, установленный в подключичную вену. На фоне проводимого лечения состояние больной улучшилось, с больной стал возможен речевой контакт. Тнойно-воспалительные
440
Гнойно-воспалительные осложнения при черепно-мозговой травме

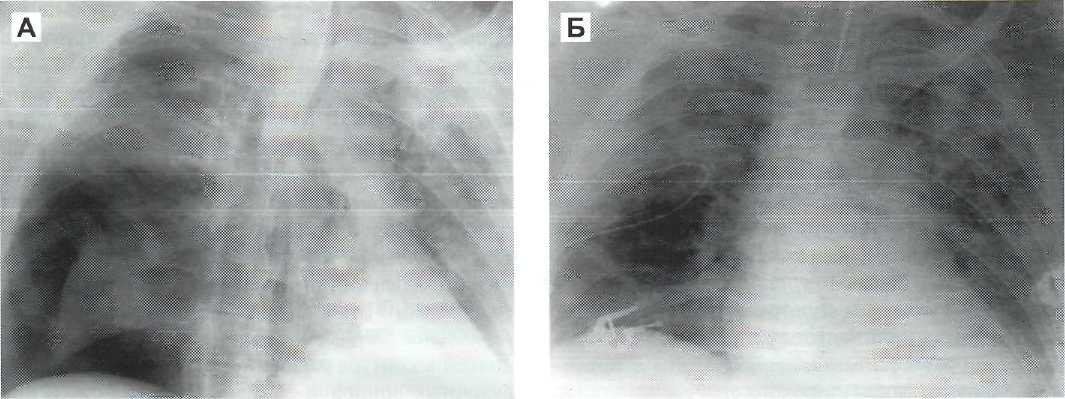
явления регрессировали, и больная переведена в нейрохирургическое отделение. Через 56 суток с момента травмы состояние больной ухудшилось, появилась эктеричноетъ кожных покровов. Диагностирован гепатит «С», что потребовало назначения ин-фузионной терапии. Через 7 суток после установки катетера в подключичную вену состояние больной ухудшилось. Больная высоко лихорадит, в легких выслушиваются хрипы с двух сторон, нарастают явления интоксикации и респираторной недостаточности. На рентгенограмме — начинающаяся двусторонняя пневмония. В подключичной области, в месте катетеризации ткани умеренно отечны, легкая гиперемия кожных покровов. Катетер удален. Отделяемое из раневого канала, и кончик катетера отправлены на микробиологическое исследование. Через сутки получен ответ: в посевах отделяемого и в смывах с катетера обнаружен метицилин-резистент-ный стафилококк. В связи с нарастанием дыхательной недостаточности наложена трахеостома. Вольная подключена к аппарату ИВЛ. Начата антибио-тикотерапия (ванкомицин), детоксикация с помощью внутривенного капельного введения гипохлори-та натрия в дозе О,1 О ЦК в концентрации 600 мг/л, введение антистафилококковой донорской плазмы, антистафилококкового у-глобулина, иммуноглобулина. В последующие сутки состояние больной резко ухудшилось, наросла гипоксия. На рентгенограмме легких (рис. 27-2) — пневмоторакс справа. Наложен плевральный дренаж с активной аспирацией содержимого. По плевральному дренажу отходит воздух с гнойно-серозным отделяемым. В посеве крови и отделяемого из плеврального дренажа — метици-лин-резистентный стафилококк.
Таким образом, клиническая картина развития данного осложнения в сочетании с данными бактериологического исследования доказывают наличие катетер-ассоциированной септицемии.
