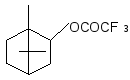
Глава 1 Трифторацетаты терпеновых спиртов (литературный обзор)
Сложные эфиры на основе терпеновых спиртов и фторкарбоновых кислот могут быть получены двумя способами:
присоединение кислот по двойным связям
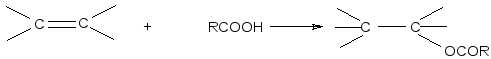
Взаимодействие трифторуксусного ангидрида с терпеновыми спиртами
![]()
Взаимодействием трифторуксусного ангидрида и сукцинимида можно получить N-(трифторацетил)сукцинимид, который является эффективным трифторацетилирующим агентом[1]
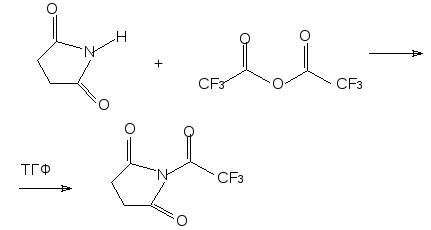
N-(трифторацетил)сукцинимид реагирует со спиртами в кипящем ТГФ или толуоле давая трифторацетаты с хорошим выходом.
Например ментол реагирует с N-(трифторацетил)сукцинимидом, образуя трифторацетат с выходом 86%.
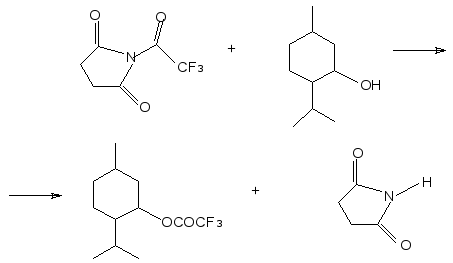
Таблица 1. Синтезы трифторацетатов с помощью N-(трифторацетил)сукцинимида.
|
R (радикал спирта) |
растворитель |
Время, ч |
Выход, % |
|
n-C18H37 |
ТГФ |
5 |
95 |
|
ментил |
ТГФ |
10 |
86 |
|
(1S)-эндо-(-)борнил |
ТГФ |
10 |
95 |
|
3-пентадецилфенил |
ТГФ |
12 |
92 |
|
1-нафтил |
Толуол |
5 |
99 |
|
4-нитрофенил |
толуол |
10 |
96 |
Присоединение фторуксусной кислоты по двойным связям
После просмотра соответствующей литературы, а именно реферативных журналов "Химия" за период 1993-2005гг и Chemical Abstracts за 1924-2005гг, можно сделать вывод, что исследованием взаимодействия терпеновых спиртов и фторкарбоновых кислот занимались крайне мало. Было найдено небольшое количество статей, посвященных изучению этой темы.
Особый интерес представляет взаимодействие α-пинена и камфена с трифторуксусной кислотой, в результате чего возможно образование изоборнилтрифторацетата, который можно рассматривать как потенциальное физиологически активное вещество. В результате литературного поиска не было найдено достоверной информации о получении изоборнилтрифторацетата из α-пинена и камфена.
Так в работах белорусских химиков [2,3] было установлено, что после смешения α-пинена(1) с трифторуксусной кислотой при последующем нагревании образуется сложная смесь веществ, в которой с помощью ГЖХ обнаружены β-пинен(2), камфен(3), дипентен(4), терпинолен(5), трициклен, α- и γ-терпинены(6,7), α- и β-фелландрены(8,9), фенхены, эфиры борнеола(10), фенхола(12), изоборнеола(11) и изофенхола(13). Однако, если приготовление реакционной смеси осуществлялось таким образом, чтобы при смешивании компонентов температура не поднималась выше 0°С, то после нагревания в продуктах реакции оказывалось только шесть соединений. Сначала появлялись камфен, дипентен, терпинолен, β-пинен, борниловый эфир трифторуксусной кислоты, а спустя некоторое время - изоборниловый эфир, содержание которого в конечном продукте реакции было незначительным. Основные направления превращений α-пинена показаны на схеме 1.

Схема 1. Основные маршруты превращений α-пинена в ходе реакции с трифторуксусной кислотой.
1. α-пинен; 2. β-пинен; 3. Камфен; 4. Дипентен; 5. терпинолен; 6. α-терпинен; 7. γ-терпинен; 8. α-фелландрен; 9. β-феландрен; 10,11. эфиры борнеола и изоборнеола; 12,13. эфиры эфиры фенхола и изофенхола.
Многообразие конечных продуктов объясняется образованием неустойчивого пинанильного катиона (схема 2).
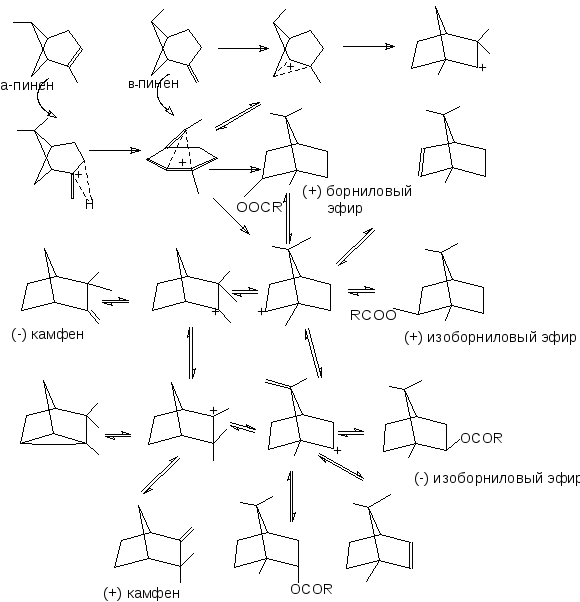
Схема 2.Взаимные переходы между мостиковыми карбкатионами (R=CF3)
Маркевич Р.Н., Ламоткин А.И. и Резников В.Н. в своей работе [4] предположили, что при гомогенном кислотном катализе промежуточным продуктом в изомеризационных превращениях α-пинена является борниловый эфир. По утверждению этих авторов ими были синтезированы борнилтрифторацетат и изоборнилтрифторацетат. Однако конкретные методики получения этих эфиров в статьях [2,3] не приведены.
Таким образом, на основании литературных данных можно сделать вывод, что реакции терпенов с карбоновыми кислотами характеризуются многообразием направлений и в результате приводят к получению сложной смеси важных в практическом отношении веществ.
На кафедре органической химии дипломницей Язвенко М. было исследовано присоединение трифторуксусной кислоты по двойным связям камфена и α- пинена.
Установлено, что процесс с использованием камфена является в высокой степени хемо – и стереоселективным. Практически единственным продуктом при соотношении реагентов 1:1 является изоборнилтрифторацетат, который выделен с выходом 90%.

При увеличении соотношения камфен : трифторуксусная кислота до 10 : 1 селективность реакции уменьшается.
Изоборнилтрифторацетат был идентифицирован методами ГЖХ, а также ЯМР 1Н и 19F спектроскопии путем сравнения соответствующих характеристик с характеристиками заведомого препарата, синтезированного взаимодействием изоборнеола с ангидридом трифторуксусной кислоты. Изоборнеол, в свою очередь был получен из камфена через образование в качестве промежуточного продукта – изоборнилацетата.
Таблица 2. Физико-химические характеристики изоборнилтрифторацетата
|
формула |
Способы получения |
Характеристика продукта |
Способы получения |
Характеристика продукта |
|
изоборнилтрифторацетат |
Камфен с трифторуксусной кислотой |
F19 ЯМР - 74,97 м.д. По отношению к CCI3F |
Изоборнеол с трифторуксусным ангидридом [10] |
F19ЯМР 0,535 м.д. По отношению к метилтрифторацетат[5,9] |
|
Н1ЯМР δ м.д. 4,84 т (H,CHO); 0.96 c (3H, CH3CO); 0.84 c, 0.86 c (6H,(CH3)2C).
| ||||
|
Выход 87% | ||||
|
Ткип=97-980/28 мм | ||||
|
Угол вращения=-32*50 | ||||
|
Выход 86,8% | ||||
|
Ткип=76,5-78,50С |
Элементный анализ С,57*6 Н,6*9 | |||
|
Показатель преломленияnd25 1,4165 | ||||
|
Элементный анализ С,57,44 Н,6,71 |
Схема 3. Изоборнилтрифторацетат, синтезированный взаимодействием изоборнеола с ангидридом трифторуксусной кислоты, через образование в качестве промежуточного продукта – изоборнилацетата.
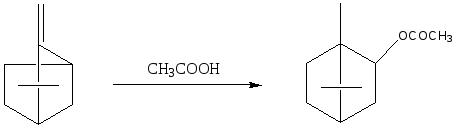
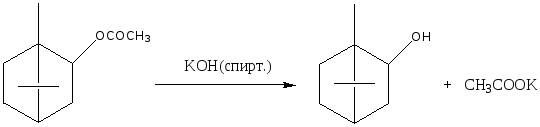
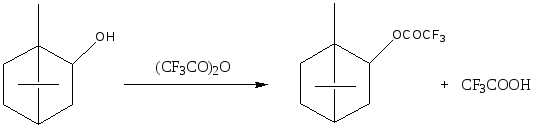
Для оптимизации условий выделения изоборнилтрифторацетата изучена его термическая устойчивость при 100, 150 и 180ºC. Установлено, что существенный распад эфира протекает лишь при 180ºC. Это позволяет рекомендовать выделение изоборнилтрифторацетата вакуумной разгонкой при остаточном давлении не более 15 мм рт. ст.
Бразильские ученые взаимодействием лимонена с трифторуксусной кислотой в циклогексане получили терпинилтрифторацетат, который охарактеризован с помощью ЯМР спектроскопии [7].
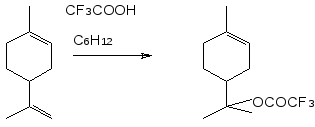
Взаимодействие лимонена с трифторуксусной кислотой исследовано также в работе японских ученых, в которой осуществлен синтез α – терпинеола из d – лимонена через терпинилтрифторацетат [8]. На первой стадии использовали в качестве растворителя толуол, мольные соотношения лимонена и трифторуксусной кислоты 1:1,2.
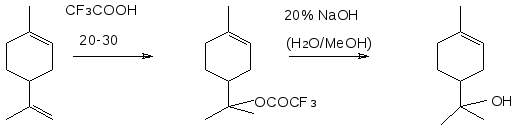
Однако терпинилтрифторацетат не выделялся из реакционной смеси, а его физико-химические свойства не исследовались.
Таким образом, на примере камфена и лимонена показано, что присоединение трифторуксусной кислоты к экзоциклическим двойным связям протекает хемоселективно. Тогда как присоединение трифторуксусной кислоты к эндоциклической двойной связи, например, α- и β-пинена сопровождается образованием широкой гаммы продуктов реакции вследствие образования на промежуточной стадии склонного к изомеризации пинанильного катиона.