
- •Программа блоков «основы строения и реакционной способности органических соединений». «углеводороды»
- •Конспект лекций
- •1. Предмет органической химии
- •2. Электронная теория химической связи
- •3. Изомерия органических соединений
- •Проекционные формулы Фишера l-молочной кислоты.
- •Способы преобразования проекционных формул.
- •Трео- и эритро- изомеры
- •Необходимые условия проявления оптической активности
Трео- и эритро- изомеры
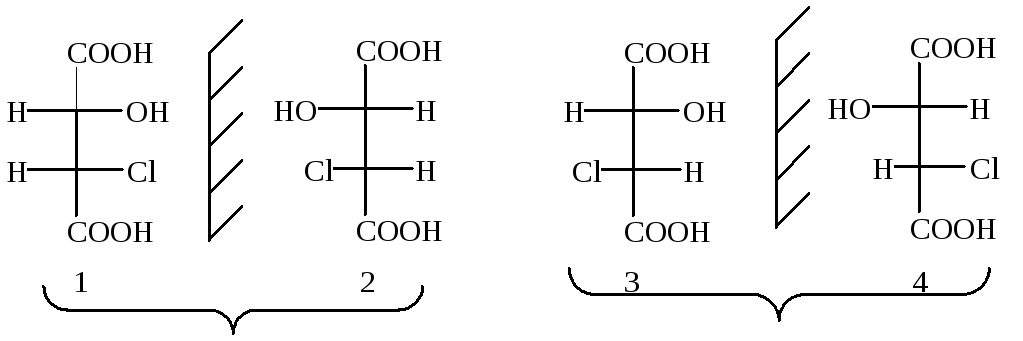
Эритро-изомеры Трео-изомеры
Эритро-изомер – диастереомер с двумя асимметрическими атомами углерода, у которых одинаковые заместители находятся по одну сторону в проекционной формуле Фишера.
Трео-изомер – диастереомер с двумя асимметрическими атомами углерода, у которых одинаковые заместители находятся по разные стороны.
Свойства стереоизомеров. Оптическая активность – способность вещества вращать плоскость поляризации.
Плоскость поляризации – плоскость, в которой происходят колебания поляризованного луча.
Оптически активные вещества – вещества, способные вращать плоскость поляризации.
Правовращающее вещество вращает плоскость поляризации вправо. Обозначается (+) или d (лат. dextrum – правый).
Левовращающее вещество вращает плоскость поляризации влево. Обозначается (–) или l (лат. laevus – левый).
Энантиомеры различаются физическими и химическими свойствами только в хиральных системах.
Их удельное вращение равно по величине и противоположно по направлению. Образуют рацемическую форму (рацемат).
Рацемат – эквимолярная смесь энантиомеров, не обладающая оптической активностью вследствие компенсации вращения. Обозначается () или d, l или D, L. Рацемат можно разделить на энантиомеры.
Диастереомеры различаются по свойствам значительно. Удельное вращение их может иметь одинаковый или противоположный знак и разную величину. Рацематов не образуют.
Мезо-формы не обладают оптической активностью вследствие внутренней компенсации вращения обеими зеркально противоположными половинами.
Таблица 4 – Сравнение свойств винных кислот.
|
Винная кислота |
[]20D |
Т. пл., оС |
|
L D мезо D,L(виноградная) |
- 11.98 + 11.98 0,00 0,00 |
168 – 170 168 – 170 140 206 |
Необходимые условия проявления оптической активности
Хиральность молекулы.
Конфигурационная устойчивость.
Третичные амины конфигурационно неустойчивые, т. к. четвертым партнером хирального атома азота является свободная орбиталь, вследствие чего возможен равновероятный обратимый переход одного энантиомера в другой с образованием рацемической смеси.
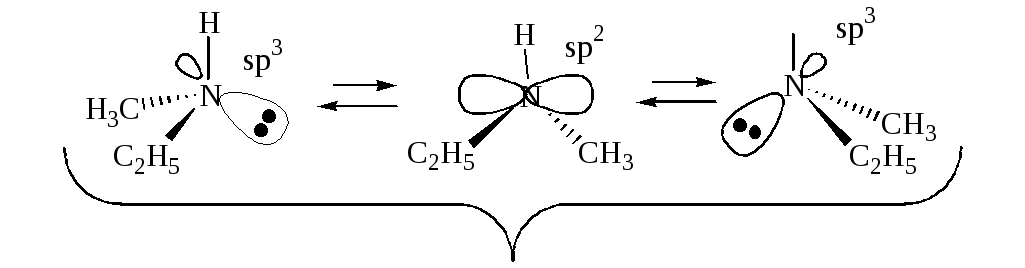
Рацемат
Рацематы, образованные из конфигурационно неустойчивых энантиомеров, разделить на энантиомеры невозможно. Соли четвертичных аммониевых оснований с 4-мя различными радикалами конфигурационно устойчивые, обладают оптической активностью. Их рацематы разделимы на энантиомеры.
Стереоизомерия замещенных циклоалканов
Оптическая изомерия, обусловленная наличием хиральных центров.
Геометрическая цис-транс-изомерия, обусловленная различным расположением заместителей относительно плоскости кольца.

цис-изомер транс-изомер транс-изомер
1, 2 и 1, 3 – пары диастереомеров;
2, 3 – пара энантиомеров.
Цис-изомер – мезо–форма, не обладает оптической активностью.
Широко распространены молекулы с одинаковыми заместителями у хиральных центров. В этом случае диастереомеры имеющие в проекциях одинаковые заместители по одну сторону – эритромеры, а по разную – треомеры.
Например, молекула винной кислоты может иметь четыре изомерные структуры:
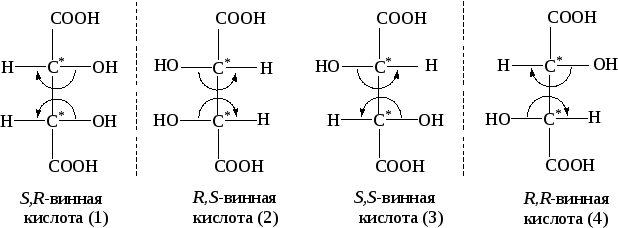
Из которых 1 и 2 – эритромеры, 3 и 4 – треомеры. Эти же пары являются по отношению друг к другу энантиомерами. А пары 1 и 3, 1 и 4, 2 и 3, 2 и 4 – диастереомеры. Эритромеры винной кислоты, несмотря на наличие хиральных центров в целом ахиральны, не обладают оптической активностью и называются мезо-формами.
Число изомеров растет по мере перехода к высшим членам гомологического ряда (табл. 5).
Таблица 5 – Структурные изомеры алканов
|
Соединение |
Структурная формула |
Количество структурных изомеров |
Примечание |
|
бутан |
С4Н10 |
2 |
|
|
пентан |
С5Н12 |
3 |
|
|
гептан |
С7Н16 |
9 |
|
|
октан |
С8Н18 |
18 |
|
|
декан |
С10Н22 |
75 |
известны 71 |
|
додекан |
С12Н26 |
355 |
|
|
эйкозан |
С20Н42 |
366319 |
|
|
триконтан |
С30Н62 |
4,11·109 |
известен 1 |
|
гектан |
С100Н202 |
5,921·1040 |
|
