
Патологическая анатомия Серов
.pdf
Изменения гранулярной эндоплазматической сети и рибосом могут быть представлены гиперплазией и атрофией, упрощением структуры, дезагрегацией (диссоциацией) рибосом и полисом, образованием аномальных рибосомально-пластинчатых комплексов.
Гиперплазия гранулярной эндоплазматической сети и рибосом, т.е. увеличение их количества, светооптически проявляется повышенной базофилией цитоплазмы, которая отражает объемную плотность рибосом и является показателем интенсивности белкового синтеза в клетке. Электронно-микроскопически в таких случаях можно судить о сопряжении синтеза и экскреции белка или отсутствии такого сопряжения. В интенсивно секретирующих и экскретирующих белок клетках (например, в активных фибробластах) цистерны гранулярной эндоплазматической сети расширены и содержат мало электронно-плотного материала: отмечается гиперплазия как связанных с мембранами, так и свободных рибосом, образующих полисомы; пластинчатый комплекс (комплекс Гольджи), участвующий в экскреции синтезируемого белка, хорошо развит (рис. 11). В интенсивно секретирующих белок клетках с нарушенной его экскрецией в гиперплазированных расширенных цистернах эндоплазматической сети с обилием рибосом и полисом накапливается хлопьевидный электронноплотный материал (рис. 12), иногда происходит его кристаллизация; комплекс Гольджи в таких случаях развит плохо.
Рис.
11. Гиперплазия гранулярной эндоплазматической сети, расширение ее цистерн, гиперплазия пластинчатого комплекса (плазматическая клетка). х13 500
31
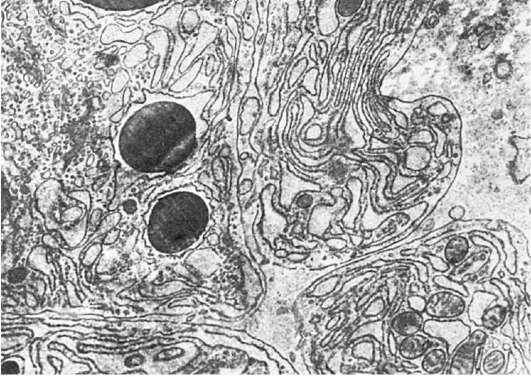
Рис.
12. Конденсированный белковый секрет в эндоплазматической сети (плазматическая клетка).
х13 500
Атрофия гранулярной эндоплазматической сети, т.е. уменьшение ее размеров, светооптически представлена снижением или исчезновением базофилии цитоплазмы, а электронно-микроскопически - уменьшением размеров канальцев и объема сети, количества и размеров рибосом (рис. 13). Она отражает снижение белково-синтетической функции клетки (белковый дефицит при голодании, болезнях печени; старение).
32
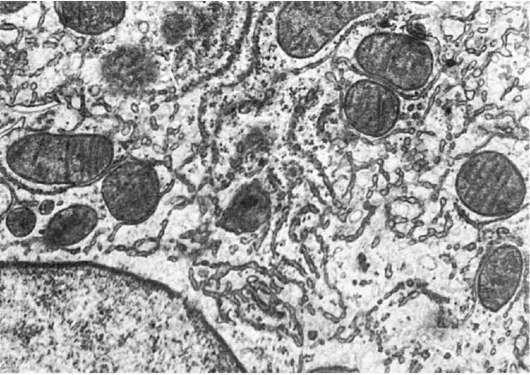
Рис.
13. Атрофия гранулярной и гиперплазия агранулярной эндоплазматической сети гепатоцитов.
х16 500
Упрощение структуры гранулярной эндоплазматической сети клеток свидетельствует о недостаточной их дифференцировке, нередко встречается в клетках злокачественных опухолей.
Дезагрегация (диссоциация) рибосом и полисом, выражающаяся в нарушениях рибосомально-мембранных взаимоотношений, «неорганизованной» ассоциации рибосом в полисомы, может быть выражением структурного упрощения эндоплазматической сети недифференцированной и опухолевой клетки. Но те же изменения наблюдаются и в дифференцированных клетках при кислородном голодании и дефиците белка в организме.
Образование аномальных рибосомально-пластинчатых комплексов является выражением субклеточной атипии и встречается при опухолях системы крови - гемобластозах (см. Опухоли системы крови).
Изменения агранулярной эндоплазматической сети
Агранулярная цитоплазматическая сеть может претерпевать ряд морфологических изменений, отражающих нарушения разнообразных функций этого органоида. Среди них главные - гиперплазия и атрофия.
Гиперплазия мембран эндоплазматической сети с расширением ее канальцев и систем (см. рис. 13) может отражать различные по интенсивности и разные по своей сути процессы. Вопервых, это усиление метаболической активности ряда веществ (белков, липидов, лекарственных средств). Во-вторых, это нарушенный внутриклеточный транспорт
33
метаболизируемых продуктов, которые накапливаются в расширенных канальцах и цистернах сети, при этом пластинчатый комплекс редуцирован. В-третьих, это дефицит ферментов (ферментопатия), ведущий к недостаточности специфических функций этого органоида. При нарушении внутриклеточного транспорта метаболизируемых продуктов и ферментопатии в расширенных цистернах эндоплазматической сети накапливаются белки и вода (гидропическая дистрофия) или липиды и липопротеиды (жировая дистрофия).
Атрофия, а в дальнейшем и редукция гладкой эндоплазматической сети возникают при остром или хроническом воздействии на клетку различных ядов и токсических веществ (рис. 14), а также при белковом голодании.
Эндоплазматическая сеть и система оксигеназ со смешанной функцией
Ряд чужеродных веществ, подвергающихся метаболизму в эндоплазматической сети, способен взаимодействовать с макромолекулами клетки, что ведет к ее повреждению. Катализаторами таких метаболических процессов в эндоплазматической сети является группа родственных NADH- и 02-зависимых ферментов. Это - монооксигеназы (гидроксилазы) или оксигеназы со смешанной функцией (ОСФ); терминальной оксигеназой этой системы является цитохром-Р-450. Система ОСФ, связанная с цитохромом Р-450, найдена в эндоплазматической сети клеток многих органов (печень, легкие, кишечник, кора надпочечников, семенники, кожа). Эта система может, помимо гидроксилирования стероидов, утилизировать многие липофильные эндогенные (жирные кислоты) и экзогенные
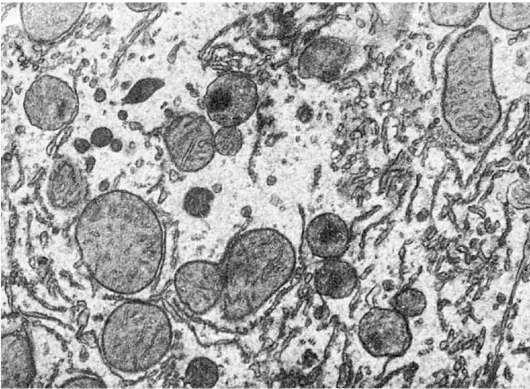 Рис.
Рис.
14. Атрофия гладкой эндоплазматической сети гепатоцита. х18 000
34

(лекарственные препараты, органические растворители, карциногены) вещества. Метаболизм чужеродных липофильных веществ требует сложного взаимодействия ряда ферментативных процессов, в которых система ОСФ - цитохром Р-450 занимает центральное место. Такой метаболизм не всегда ведет к инактивации метаболических веществ. Возможно образование реакционноспособных оксигенированных продуктов, которые могут взаимодействовать с нуклеиновыми кислотами и белками клетки, что ведет к ее повреждению. Основной механизм такого повреждения - это генерация супероксидных радикалов кислорода и перекиси водорода, индуцирующих переокисление липидов.
Пластинчатый комплекс (комплекс Гольджи), секреторные гранулы и вакуоли Синтетическая деятельность пластинчатого комплекса, тесно связанная с
эндоплазматической сетью, завершается образованием секреторных гранул и вакуолей. Поэтому морфология нарушенной деятельности пластинчатого комплекса отражает и нарушения секреции, т.е. нарушения продукции клеточных включений - гранул и вакуолей. Можно говорить о двух основных морфологических проявлениях нарушенной деятельности пластинчатого комплекса и секретообразования: гипертрофии и атрофии.
Гипертрофия пластинчатого комплекса, т.е. его увеличение за счет гиперплазии его мембран, увеличения количества секреторных гранул, везикул и вакуолей, является проявлением повышенного синтеза и секреции белков, гликолипидов или полисахаридов (рис. 15). При этом увеличивается количество секреторных гранул и везикул в цитоплазме и за пределами пластинчатого комплекса. Гипертрофия пластинчатого
Рис.
15. Гиперплазия мембран пластинчатого комплекса в подоците. х20 500
35
комплекса в таких случаях сочетается с гиперплазией эндоплазматической сети. В тех случаях, когда синтез тех или иных веществ опережает их секрецию и выведение, эти вещества избирательно накапливаются в гипертрофированном пластинчатом комплексе и могут повреждать его. Таково, например, скопление желчи в пластинчатом комплексе гепатоцитов при холестазе.
Атрофия пластинчатого комплекса, т.е. уменьшение его размеров с редукцией компонентов, потерей секреторных гранул и вакуолей, свидетельствует о снижении его функциональной активности. Одной из причин такого снижения может быть недостаточность белковых запасов организма (белковое голодание); при этом эндоплазматическая сеть также атрофична, в цитоплазме мало секреторных гранул. Другая причина снижения функциональной активности пластинчатого комплекса - это нарушение взаимодействия пластинчатого комплекса с эндоплазматической сетью, т.е. «повреждение» клеточного конвейера. В этих случаях эндоплазматическая сеть гиперплазирована, функционально активна, а цитоплазма заполнена множеством секреторных гранул и вакуолей.
Митохондрии
Митохондрии являются наиболее лабильными внутриклеточными структурами. Они первыми подвергаются изменениям при гиперфункции клетки и различных ее повреждениях. Изменения митохондрий, возникающие при многих патологических процессах и болезнях, достаточно стереотипны, хотя ряд патологических состояний и болезней имеет специфические признаки повреждения митохондрий.
Изменения структуры, размеров, формы и числа митохондрий
Среди изменений структуры митохондрий наибольшее значение придается их конденсации и набуханию, а также появлению митохондриальных включений. Конденсация и набухание митохондрий (см. рис. 10) могут отражать функциональное напряжение клетки, но чаще нарастающее кислородное голодание. Эти изменения нередко обратимы, однако, прогрессируя, ведут к тяжелой деструкции митохондрий и гибели клетки. Тогда к набуханию митохондрий присоединяются уплотнение их внутреннего пространства, деформация крист и потеря митохондриальных гранул, гомогенизация матрикса и появление в нем хлопьевидного материала, очагов обызвествления; в финале возникают разрывы наружной мембраны митохондрий.
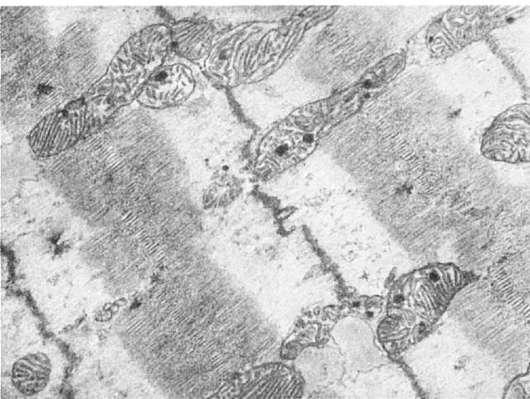
Митохондриальные включения представлены хлопьевидным электронноплотным материалом (липидные вещества), очагами обызвествления (гидрооксиапатитоподобные кристаллы - рис. 16), миелиновыми фигурами, филаментоподобными и пластинчатыми структурами, белковыми кристаллами. Включения в митохондрии, как правило, встречаются при патологических состояниях, отражая неспецифическую реакцию митохондрий на повреждение клетки.
36
Размеры митохондрий колеблются в широких пределах - от гигантских до резко редуцированных форм. Гигантские митохондрии, которые образуются за счет гипертрофии или слияния митохондрий, встречаются только в патологических условиях (рис. 17). Такие митохондрии, нередко с кристаллическими включениями, как правило, обнаруживают, напри-
Рис.
16. Включения солей кальция в матриксе митохондрий мышечного волокна при ишемии. х18
500
37
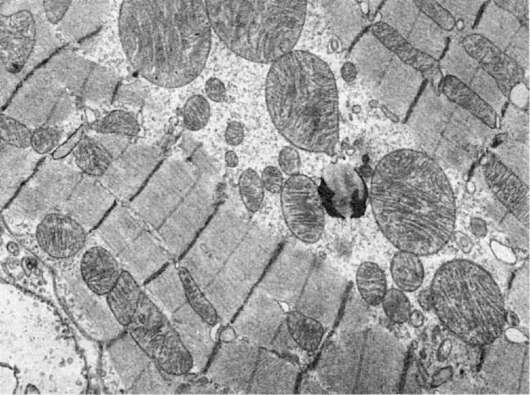
Рис.
17. Гигантские митохондрии кардиомиоцитов. Миокард собаки при синдроме длительного раздавливания. х16 000
мер, в гепатоцитах при алкоголизме. Митохондрии, в том числе и гигантские, могут быть различной формы: сигарообразные, каплеобразные, извитые и т.д.
Число митохондрий крайне вариабельно. Увеличение числа митохондрий (т.е.
гиперплазия), отражающее усиление протекающего в них окислительного фосфорилирования, характерно для клеток с активацией специализированной функции, что имеет место при гипертрофии, пролиферации и трансформации клеток, особенно после повреждения ткани. Большое число митохондрий крайне характерно для онкоцитов, в том числе и онкоцитарньгх опухолей. Уменьшение числа митохондрий типично для так называемых регрессивных процессов - старения клеток, их атрофии.
Изменения крист митохондрий
Изменения крист митохондрий, как и самих митохондрий, могут касаться также их структуры, размеров, формы и числа.
Структурные изменения разнообразны: пластинчатые кристы появляются при усилении активности митохондрий. Деформация и агрегация крист встречаются при понижении этой активности. Форма кристтакже отражает повышенную или пониженную активность митохондрий. Размеры крист, как правило, соответствуют размерам митохондрий: гигантские кристы в гигантских митохондриях, редукция крист при редукции митохондрий. В такой же мере и число крист отражает активность митохондрий: увеличение числа крист митохондрий
38
- свидетельство возрастающих функциональных потребностей клетки; уменьшение числа крист (редукция) митохондрий - свидетельство снижения этих потребностей.
Митохондриальный транспорт кальция и повреждение клетки
Одной из важных функций митохондрий является транспорт кальция. Кальций может накапливаться митохондриями в весьма значительных количествах, особенно параллельно с неорганическим фосфатом. Высвобождение кальция из митохондрий происходит двумя путями. Один из путей накопления кальция (митохондрии клеток сердца, мозга, скелетных мышц, экзокринных и эндокринных желез) стимулируется натрием и, видимо, представляет собой обмен Са2+ на Na+; другой путь (митохондрии клеток почек, печени, легких) нечувствителен к натрию, механизм его неясен.
Морфологическим подтверждением транспорта кальция митохондриями является обнаружение в митохондриальном матриксе электронноплотных гранул диаметром 20-50 нм, которые, возможно, служат местом аккумуляции двухвалентных ионов. Увеличение размера, плотности и числа этих гранул обнаружено не только при обработке тканей высокими концентрациями Са2+, но и в интактных клетках тех тканей, которые вовлечены в активный транспорт кальция - остеокластах, остеобластах и др. Та же ситуация обнаружена и при гормонально-обусловленных гиперкальциемиях - кальцинозах. При некоторых болезнях (коронарная болезнь сердца), синдромах (хроническая почечная недостаточность) и патологических состояниях (отравления тиоацетатамидом, папаином, йодоформом и т.д.) клетки отвечают на повреждение появлением в митохондриальном матриксе многочисленных крупных плотных гранул кальция (см. рис. 16). При этом кальцификация митохондрий предшествует некрозу клетки и часто бывает обратимой.
Внутримитохондриальная кальцификация может быть связана как с избыточным притоком кальция в клетку вследствие первичного повреждения плазматической мембраны, так и с первичными нарушениями транспорта кальция митохондриями. При первичном повреждении плазматической мембраны избыточный приток кальция в клетку приводит к накоплению его в митохондриях, что «отнимает» энергию АТФ и повреждает саму систему генерации энергии - митохондрии. Первичные нарушения митохондриального транспорта кальция встречаются при заболеваниях скелетных мышц - миопатиях (болезнь Люфта, синдром Кернса-Сайра). При этих болезнях митохондрии, несмотря на высокий уровень эндогенного кальция, могут дополнительно накапливать значительные его количества. В таких случаях можно говорить о «болезнях» нарушенного митохондриального транспорта.
Лизосомы
Лизосомы не только «органы» внутриклеточного пищеварения, о чем говорит их название, но и «убийцы» клетки; они причастны как к фагоцитозу, так и аутофагии. Физиологическая и патологическая активность лизосом зависит в основном от двух факторов: состояния (стабилизации) мембран лизосом и активности их ферментов. Поэтому повреждения клетки, к которым могут быть причастны лизосомы, возникают либо при дестабилизации лизосомных мембран, позволяющей проявиться гидролазной активности
39
ферментов, либо при лизосомной ферментопатии, ведущей к накоплению в клетке ряда исходных или промежуточных продуктов обмена.
Дестабилизация мембран лизосом и патология клетки
К дестабилизации (лабилизации) мембран лизосом могут привести воздействия различных веществ и агентов -лабилизаторов мембран лизосом (например, так называемые провоспалительные гормоны, витамины A, D, К и др.). Выраженным повреждающим мембраны лизосом действием отличаются некоторые микотоксины, различные канцерогенные вещества, фосфолипазы, активаторы и продукты перекисного окисления, двуокись кремния. Дестабилизирующе на мембраны лизосом действуют гипоксия, нарушения кислотноосновного состояния, голодание и белковая недостаточность, изменения гормонального статуса, шок, травмы, обширные оперативные вмешательства. Антагонистами лабилизаторов мембран лизосом являются их стабилизаторы(например, так называемые противовоспалительные гормоны, хлороксин, фенерган, холестерол и др.).
В патологических условиях возникают конкурентные взаимоотношения между лабилизаторами и стабилизаторами лизосомных мембран, и, если они в пользу первых, проницаемость мембран становится достаточной для выхода гидролаз в цитоплазму и взаимодействия с субстратом, которым могут стать и субклеточные структуры. Часть клетки или вся клетка погибают. Тот же механизм дестабилизации мембран лизосом имеется при фагоцитозе, когда после контакта первичных лизосом с фагосомами образуются фаголизосомы (рис. 18) и цитолизосомы. Подобный механизм лежит и в основе клеточной аутофагии. Как видно, патология мембран лизосом может определять и патологию фагоцитоза.
40
