
МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«МАТИ – Российский государственный технологический университет имени К.Э. Циолковского»
(МАТИ)
Лабораторная работа : «Т2 : Определение отношения теплоемкости воздуха»
Выполнил студент группы 2АВС-2ДБ-270
Бессонов Илья Игоревич
Москва 2014
Схема экспериментальной установки :
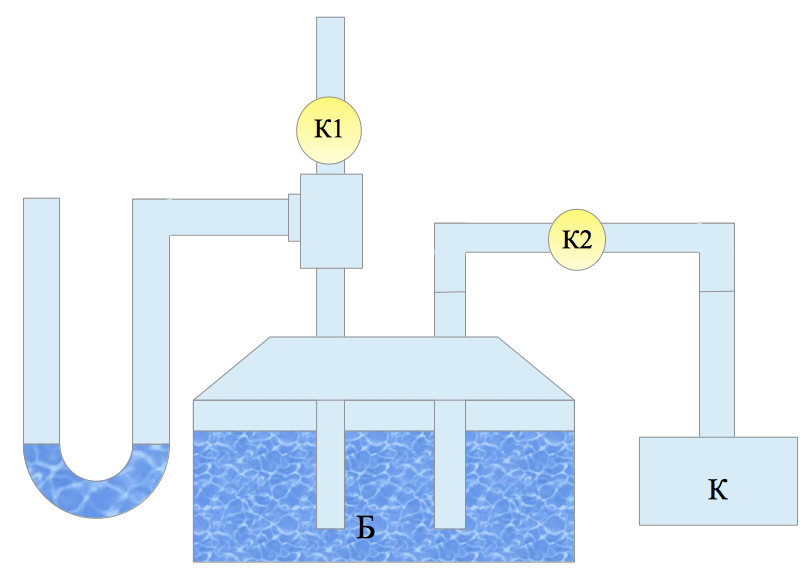
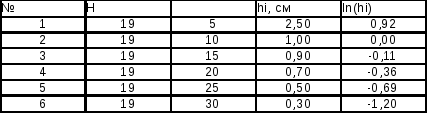
-
Найдем ln(hi)
-
По результатам измерений __ и ln(hi), найдем ln(h0) и абсолютную погрешность (полуширину доверительного интервала) ∆ln(h0). Величина h0 соответствует мгновенному (адиабатному) расширению воздуха. Согласно уравнению
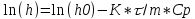 ,
график функции ln(h)=f(τ)
— прямая линия. Приближенно ln(h0) и
∆ln(h0) можно найти по графику:
,
график функции ln(h)=f(τ)
— прямая линия. Приближенно ln(h0) и
∆ln(h0) можно найти по графику:
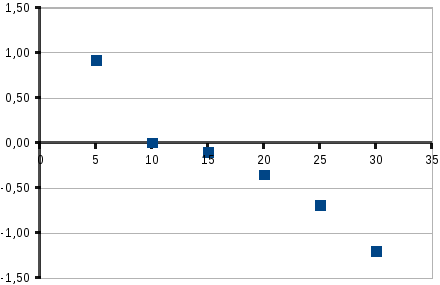




ln(h0)≈0,73
∆ln(h0) = ln(h1) — ln(h0) = 0,91-0,73 = 0,18.
3)
![]()
h0=2,07
∆h0=0,37
4)Найдем отношение теплоемкостей воздуха γ по формулам :
![]()
γ = 1,12
5)Определим абсолютную погрешность ∆H и вычислим абсолютную погрешность ∆γ c помощью формулы :
![]()
∆H = 0
![]()
Вопросы : 1)Теплоемкость — физическая величина, опред. Отношение бесконечно малого кол-ва теплоты полученного телом, к соответствующему приращению температуры.
2) Уравнение первого начала термодинамики dQ = dU + dA
3) Потому что при постоянном объёме газ только нагревается, а при постоянном давлении - ещё и совершает работу против внешней силы (равную произведению давления на изменение объёма) .
4)
5)
6)Процесс выпускания воздуха можно считать адиабатическим, потому что происходит быстрое изменение объема газа и т.к. обмен теплотой с окр.средой невелик в следствии быстроты протекания процесса.
7)Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
8)
9)Ур-е адиабатического процесса для ИГ имеет вид :
PV^k = const
T*p^(k-1) = const
TV^(k-1) = const
10)Политропный процесс — термодинамический процесс при котором удельная теплоемкость = const
11)Показатель политропы изменяется от (-бесконечность; + бесконечность).
(P=const) n=0;
T=const n=1;
V=const n±бесконечность;
dQ=const n=R;
12)P=const T=const
V=const P/T= const
T=const PV=const
13) Cp = Cv +R
14) (11)
15) Внутренняя энергия тела при адиабатическом процессе изменяется в результате работы тела.
16) Макросостояние - состояние тела, содержащего огромное количество частиц, характеризующееся с помощью макропроцессов. Микросостояние – состояние всех частиц, из которых состоит тело.
17) Статистический вес макросостояния – число рзличных микросостояний, соответствующих данному макросостоянию.
18) Равновесным называется макросостояние, которое не имеет тенденций к изменению с течением времени.
19) необратимым называется процесс, обратный которому маловероятен.
20) Квазистатический процесс в термодинамике - идеальный процесс, состоящий из неприрывно следующих друг за другом состояний равновесия.
21) Степени свободы тела – независимые величины, с помощью которых может быть задано положение тела, необходимы для полного описания движения механической системы.
22) i=2
23) Cv= iR/2
24) Ѡ=i/2 kT
25) Внутренняя энергия газа характеризует поступательное, вращательное и колебательное движение.
26) Связанная энергия - та часть внутренней энергии, которая не может быть превращена в работу.
27) Энтропия — мера необратимого рассеивания энергии, мера отклонения реального процесса от идеального. Энтропия – вероятностная статистическая величина. наиболее вероятным изменением энтропии является ее возрастание.
28) ∆S=∆Q/T
29) В адиабатическом процессе энтропия равна нулю
30) Можно считать массу неизменяемой.
