
- •1. Фотофизический этап фотосинтеза
- •2.2 Перенос электрона по электронно-транспортной цепи
- •2.3 Фотофосфорилирование
- •1.Макроэлементы.
- •2.Микроэлементы.
- •42.Покой у растений. Виды покоя, способы его нарушения.
- •43.Ферменты класса оксидоредуктаз: дегидрогеназы и оксидазы.
- •45.Понятие о росте и развитии растений, их различие и взаимосвязь.
- •46.Классификация ферментов. Ферменты класса гидролаз, изоферменты.
- •Классификация
- •47. Величины, характеризующие процесс транспирации.
- •48.Физиологическая роль макроэлементов в растениях.
- •49.Каротиноиды, их строение, функции.
- •50.Жаростойкость и засухоустойчивость растений.
- •51.Физиологические основы применения удобрений.
- •52.Днк как генетический материал клетки.
- •54.Диагностика дефицита питательных элементов.
- •56.Энергетический уровень различных путей окисления.
- •3.3 Фотосинтез по типу толстянковых (сам-метаболизм)
- •Белки, их строение и функции Интегрированный урок
- •Ход урока Роль белков в организме
- •Состав, строение, свойства белков
- •Химические свойства белков
- •Лабораторный опыт 1. Денатурация белков
- •Лабораторный опыт 2. Цветные качественные реакции белков
- •Функции белков
- •Синтез белков
- •Превращения белков в организме
Химические свойства белков
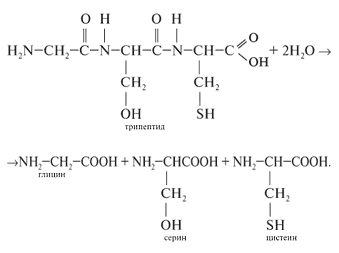
При нагревании белков и пептидов с растворами кислот, щелочей или при действии ферментов протекает гидролиз. Гидролиз белков сводится к расщеплению полипептидных связей:
Лабораторный опыт 1. Денатурация белков
Денатурация – нарушение природной структуры белка под действием нагревания и химических реагентов. а) Действие спирта на белок; б) действие солей хлорида натрия (концентрированный раствор) и ацетата свинца на белок; в) действие HNO3 (конц.); г) свертывание белков при кипячении.
Лабораторный опыт 2. Цветные качественные реакции белков
а) Биуретовая реакция; б) ксантопротеиновая реакция; в) взаимодействие белка с ацетатом свинца при нагревании.
Учительхимии. Данные опыта 1 показывают, что загрязнение природной среды солями тяжелых металлов приводит к отрицательным последствиям для живых организмов. Природные белки теряют присущие им специфические свойства, становятся нерастворимыми, денатурируют. При отравлении людей солями тяжелых металлов используют молоко, белки которого связывают ионы таких металлов. (Демонстрация фрагмента из 1-й части фильма «Белки, строение белковых молекул».)
Функции белков
Учитель биологии. Функции белков разнообразны.
1. Строительный материал – белки участвуют в образовании оболочки клетки, органоидов и мембран клетки. Из белков построены кровеносные сосуды, сухожилия, волосы. 2. Каталитическая роль – все клеточные катализаторы – белки (активные центры фермента). Структура активного центра фермента и структура субстрата точно соответствуют друг другу, как ключ и замок. 3. Двигательная функция – сократительные белки вызывают всякое движение. 4. Транспортная функция – белок крови гемоглобин присоединяет кислород и разносит его по всем тканям. 5. Защитная роль – выработка белковых тел и антител для обезвреживания чужеродных веществ. 6. Энергетическая функция – 1 г белка эквивалентен 17,6 кДж.
Содержание белков в различных тканях человека неодинаково. Так, мышцы содержат до 80% белка, селезенка, кровь, легкие – 72%, кожа – 63%, печень – 57%, мозг – 15%, жировая ткань, костная и ткань зубов – 14–28%. Белки – необходимые компоненты пищевых продуктов, они входят в состав лекарственных препаратов.
Синтез белков
Учитель биологии. Человек в течение длительного времени потреблял белки, выделенные главным образом из растений и животных. В последние десятилетия ведутся работы по искусственному получению белковых веществ. Половина земного шара находится в состоянии белкового голодания, а мировая нехватка пищевого белка составляет около 15 млн т в год при норме потребления белка в сутки взрослым человеком 115 г. (Демонстрация фрагмента 2-й части кинофильма «Белки, строение белковых молекул» – о сборке молекулы белка.)
Превращения белков в организме

Учительхимии. Выводы. Все белки являются полипептидами, но не всякий полипептид является белком. Каждый белок имеет свое специфическое строение.
Различают физические, химические и биологические свойства белков.
Физическими свойствами белков являются наличие молекулярной массы, двойное лучепреломление (изменение оптической характеристики раствора белка, находящегося в движении, по сравнению с раствором, находящимся в покое), обусловленное несферической формой белков, подвижность в электрическом поле, обусловленная зарядом молекул белка. Кроме этого для белков характерны оптические свойства, заключающиеся в способности вращать плоскость поляризации света, рассеивать световые лучи ввиду значительных размеров белковых частиц и поглощать ультрафиолетовые лучи.
Одним из характерных физических свойств белков являются способность адсорбировать на поверхности, а иногда и захватывать внутрь молекулы, низкомолекулярные органические соединения и ионы.
Химические свойства белков отличаются исключительным разнообразием, так как для белков характерны все реакции аминокислотных радикалов и характерна реакция гидролиза пептидных связей.
Имея значительное число кислотных и основных групп, белки проявляют амфотерные свойства. В отличие от свободных аминокислот кислотно-основные свойства белков обусловлены не α-амино- и α-карбокси-группами, занятыми в образовании пептидных связей, а заряженными радикалами аминокислотных остатков. Основные свойства белков обусловлены остатками аргинина, лизина и гистидина. Кислые свойства обусловлены остатками аспарагиновой и глутаминовой кислоты.
Кривые титрования белков достаточно сложны для интерпретации, так как в любом белке имеется слишком большое число титруемых групп, между ионизированными группами белка имеются электростатические взаимодействия, на рК каждой титруемой группы оказывают влияние рядом расположенные гидрофобные остатки и водородные связи. Наибольшее практическое применение имеет изоэлектрическая точка белка – значение рН, при котором суммарный заряд белка равен нулю. В изоэлектрической точке белок максимально инертен, не перемещается в электрическом поле и имеет наиболее тонкую гидратную оболочку.
Белки проявляют буферные свойства, но их буферная емкость незначительна. Исключение составляют белки, содержащие большое число остатков гистидина. Например, содержащийся в эритроцитах гемоглобин за счет очень высокого содержания остатков гистидина имеет значительную буферную емкость при рН около 7, что весьма важно для той роль, которую играют эритроциты в переносе кровью кислорода и углекислого газа.
Для белков характерна растворимость в воде, причем с физической точки зрения они образуют истинные молекулярные растворы. Однако для растворов белков характерны некоторые коллоидные свойства: эффект Тендаля (явление светорассеяния), неспособность проходить через полупроницаемые мембраны, высокая вязкость, образование гелей.
Растворимость белка сильно зависит от концентрации солей, то есть от ионной силы раствора. В дистиллированной воде белки чаще всего растворяются плохо, однако их растворимость возрастает по мере увеличения ионной силы. При этом все большее количество гидратированных неорганических ионов связывается с поверхностью белка и тем самым уменьшается степень его агрегации. При высокой ионной силе ионы солей забирают гидратную оболочку у молекул белка, что приводит к агрегации и выпадению белков в осадок (явление высаливания). Используя различие в растворимости, можно с помощью обычных солей разделить смесь белков.
К числу биологических свойств белков относят в первую очередь их каталитическую активность. Другое важное биологическое свойство белков – их гормональная активность, то есть способность воздействовать на целые группы реакций в организме. Некоторым белкам присущи токсические свойства, патогенная активность, защитные и рецепторные функции, ответственность за явления клеточной адгезии.
Еще одно своеобразное биологическое свойство белков – денатурация. Белки в их естественном состоянии носят название нативных. Денатурация – это разрушение пространственной структуры белков при действии денатурирующих агентов. Первичная структура белков при денатурации не нарушается, но теряется их биологическая активность, а также растворимость, электрофоретическая подвижность и некоторые другие реакции. Радикалы аминокислот, формирующие активный центр белка, при денатурации оказываются пространственно удаленными друг от друга, то есть разрушается специфический центр связывания белка с лигандом. Гидрофобные радикалы, обычно находящиеся в гидрофобном ядре глобулярных белков, при денатурации оказываются на поверхности молекулы, тем самым создаются условия для агрегации белков, которые выпадают в осадок.
Реагенты и условия, вызывающие денатурацию белков:
- температура выше 60оС – разрушение слабых связей в белке,
- кислоты и щелочи – изменение ионизации ионогенных групп, разрыв ионных и водородных связей,
- мочевина – разрушение внутримолекулярных водородных связей в резуль-тате образования водородных связей с мочевиной,
- спирт, фенол, хлорамин – разрушение гидрофобных и водородных связей,
- соли тяжелых металлов – образование нерастворимых солей белков с иона-ми тяжелых металлов.
При удалении денатурирующих агентов возможна ренативация, так как пептидная цепь стремится принять в растворе конформацию с наименьшей свободной энергией.
В условиях клетки белки могут самопроизвольно денатурировать, хотя и с меньшей скоростью, чем при высокой температуре. Самопроизвольная ренативация белков в клетке затруднена, так как из-за высокой концентрации существует большая вероятность агрегации частично денатурированных молекул.
В клетках имеются белки – молекулярные шапероны, которые обладают способностью связываться с частично денатурированными, находящимися в неустойчивом, склонном к агрегации состоянии белками и восстанавливать их нативную конформацию. Вначале эти белки были обнаружены как белки теплового шока, так как их синтез усиливался при стрессовых воздействиях на клетку, например, при повышении температуры. Шапероны классифицируются по массе субъединиц: hsp-60, hsp-70 и hsp-90. Каждый класс включает семейство родственных белков.
Молекулярные шапероны (hsp-70) высококонсервативный класс белков, находящийся во всех отделах клетки: цитоплазме, ядре, эндоплазматическом ретикулуме, митохондриях. На С-конце единственной полипептидной цепи hsp-70 имеет участок, который представляет собой бороздку, способную взаимодействовать с пептидами длиной 7-9 аминокис-лотных остатков, обогащенных гидрофобными радикалами. Такие участки в глобулярных белках встречаются примерно через каждые 16 аминокислот. Hsp-70 способны защищать белки от температурной инактивации и восста-навливать конформацию и активность частично денатурированных белков.
Шапероны-60 (hsp-60) участвуют в формировании третичной структуры белков. Hsp-60 функционируют в виде олигомерных белков, состоящих из 14 субъединиц. Hsp-60 образуют два кольца, каждое кольцо состоит из 7 субъединиц, соединенных друг с другом. Каждая субъединица состоит из трех доменов:
- апикальный домен имеет ряд гидрофобных аминокислотных остатков, обращенных внутрь полости, формируемой субъединицами;
- экваториальный домен обладает АТФазной активностью, необходим для высвобождения белка из шаперонинового комплекса;
- промежуточный домен соединяет апикальный и экваториальный домены.
Белок, имеющий на своей поверхности фрагменты, обогащенные гидрофобными аминокислотами, попадает в полость шаперонинового комплекса. В специфической среде этой полости в условиях изолированности от других молекул цитозоля клетки выбор возможных конформаций белка происходит до тех пор, пока не будет найдена энергетически более выгодная конформация. Шаперонзависимое формирование нативной конформации связано с расходованием значительного количества энергии, источником которой служит АТФ.
Аминокислоты
Любое соединение, которое содержит одновременно карбоксильную и аминогруппу, является аминокислотой . Однако, чаще этот термин применяется для обозначения карбоновых кислот, аминогруппа которых находится в a-положении к карбоксильной группе.

Аминокислоты, как правило, входят в состав полимеров - белков . В природе встречается свыше 70 аминокислот, но только 20 играют важную роль в живых организмах. Незаменимыми называются аминокислоты, которые не могут быть синтезированы организмом из веществ, поступающих с пищей, в количествах, достаточных для того, чтобы удовлетворить физиологические потребности организма. Незаменимые аминокислоты приводятся в табл. 1. Для больных фенилкетонурией незаменимой аминокислотой является такжетирозин (см. табл. 1).
Таблица 1
Незаменимые аминокислоты R-CHNH2 COOH
Название (сокращение) |
R |
изолейцин (ile, ileu) |
CH3 CH2 CH(CH)3 - |
лейцин (leu) |
(CH3 )2 CHCH2 - |
лизин (lys) |
NH2 CH2 CH2 CH2 CH2 - |
метионин (met) |
CH3 SCH2 CH2 - |
фенилаланин (phe) |
C6 H5 CH2 - |
треонин (thr) |
CH3 CH(OH)- |
триптофан (try) |
|
валин (val) |
(CH3 )2 CH- |
тирозин (tyr) |
|
Аминокислоты называют обычно как замещенные соответствующих карбоновых кислот, обозначая положение аминогруппы буквами греческого алфавита. Для простейших аминокислот обычно применяются тривиальные названия (глицин, аланин, изолейцин и т.д.). Изомерия аминокислот связана с расположением функциональных групп и со строением углеводородного скелета. Молекула аминокислоты моет содержать одну или несколько карбоксильных групп и в соответствии с этим аминокислоты различаются по основности. Также в молекуле аминокислоты может находиться разное количество аминогрупп.
СПОСОБЫ ПОЛУЧЕНИЯ АМИНОКИСЛОТ
1. Гидролизом белков можно получить около 25 аминокислот, но полученную смесь трудно разделить. Обычно одна или две кислоты получаются в значительно больших количествах, чем остальные, и эти кислоты удается выделить довольно легко – с помощью ионообменных смол.
2. Из галогензамещенных кислот. Один из наиболее распространенных методов синтеза a -аминокислот заключается в аммонолизе a-галогензамещенной кислоты, которую обычно получают по реакции Геля-Фольгарда-Зелинского:

Этот метод можно модифицировать, получая a-бромзамещенную кислоту через малоновый эфир:

Ввести аминогруппу в эфир a-галогензамещенной кислоты можно с помощью фталимида калия (синтез Габриэля ):

3. Из карбонильных соединений (синтез Штреккера ). Синтез a-аминокислот по Штреккеру состоит в реакции карбонильного соединения со смесью хлорида аммония и цианистого натрия (это усовершенствование метода предложено Н.Д. Зелинским и Г.Л. Стадниковым).

Реакции присоединения - отщепления с участием аммиака и карбонильного соединения дают имин, который реагирует с цианистым водородом, образуя a-аминонитрил. В результате его гидролиза образуется a-аминокислота.

Химические свойства аминокислот
Все a-аминокислоты, кроме глицина, содержат хиральный a-углеродный атом и могут встречаться в виде энантиомеров :

Было доказано, что почти все природные a-аминокислоты обладают одной и той же относительной конфигурацией при a-углеродном атоме. a-Углеродному атому (-)-серина была условно приписана L -конфигурация, а a-углеродному атому (+)-серина - D -конфигурация. При этом, если проекция a-аминокислоты по Фишеру написана так, что карбоксильная группа расположена сверху, а R - внизу, у L -аминокислоты аминогруппа будет находиться слева, а у D -аминокислоты - справа. Схема Фишера для определения конфигурации аминокислоты применима ко всем a-аминокислотам, обладающим хиральным a-углеродным атомом.

Из рисунка видно, что L -аминокислота может быть правовращающей (+) или левовращающей (-) в зависимости от природы радикала. Подавляющее большинство a-аминокислот, встречающихся в природе, относится к L -ряду. Их энантиоморфы , т.е. D -аминокислоты, синтезируются только микроорганизмами и называются «неприродными» аминокислотами .
Согласно номенклатуре (R,S), большинство «природных» или L-аминокислот имеет S-конфигурацию.

L-Изолейцин и L-треонин, содержащие по два хиральных центра в молекуле, могут быть любыми членами пары диастереомеров в зависимости от конфигурации при b-углеродном атоме. Ниже приводятся правильные абсолютные конфигурации этих аминокислот.

КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
Аминокислоты - амфотерные вещества, которые могут существовать в виде катионов или анионов. Это свойство объясняется наличием как кислотной (-СООН ), так и основной (- NH 2 ) группы в одной и той же молекуле. В очень кислых растворах NH 2 -группа кислоты протонируется и кислота становится катионом. В сильнощелочных растворах карбоксильная группа аминокислоты депротонируется и кислота превращается в анион.
В твердом состоянии аминокислоты существуют в виде цвиттер-ионов (биполярных ионов, внутренних солей ). В цвиттер-ионах протон переносится от карбоксильной группы к аминогруппе:

Если поместить аминокислоту в среду, обладающую проводимостью, и опустить туда пару электродов, то в кислых растворах аминокислота будет мигрировать к катоду, а в щелочных растворах - к аноду. При некотором значении рН, характерном для данной аминокислоты, она не будет передвигаться ни к аноду, ни к катоду, так как каждая молекула находится в виде цвиттер-иона (несет и положительный, и отрицательный заряд). Это значение рН называется изоэлектрической точкой (pI) данной аминокислоты.
РЕАКЦИИ АМИНОКИСЛОТ
Большинство реакций, в которые аминокислоты вступают в лабораторных условиях (in vitro ), свойственны всем аминам или карбоновым кислотам.
1. образование амидов по карбоксильной группе. При реакции карбонильной группы аминокислоты с аминогруппой амина параллельно протекает реакция поликонденсации аминокислоты, приводящей к образованию амидов. Чтобы предотвратить полимеризацию, аминогруппу кислоты блокируют с тем, чтобы в реакцию вступала только аминогруппа амина. С этой целью используют карбобензоксихлорид (карбобензилоксихлорид, бензилхлорформиат), трет -бутоксикарбоксазид и др. Для реакции с амином карбоксильную группу активируют, воздействуя на нее этилхлорформиатом. Защитную группу затем удаляют путем каталитического гидрогенолиза или действием холодного раствора бромистого водорода в уксусной кислоте.

2. образование амидов по аминогруппе. При ацилировании аминогруппы a-аминокислоты образуется амид.

Реакция лучше идет в основной среде, так как при этом обеспечивается высокая концентрация свободного амина.
3. образование сложных эфиров. Карбоксильная группа аминокислоты легко этерифицируется обычными методами. Например, метиловые эфиры получают, пропуская сухой газообразный хлористый водород через раствор аминокислоты в метаноле:

Аминокислоты способны к поликонденсации, в результате которой образуется полиамид. Полиамиды, состоящие из a-аминокислот, называются пептидами или полипептидами . Амидная связь в таких полимерах называется пептидной связью . Полипептиды с молекулярной массой не меньше 5000 называют белками . В состав белков входит около 25 различных аминокислот. При гидролизе данного белка могут образовываться все эти аминокислоты или некоторые из них в определенных пропорциях, характерных для отдельного белка.
Уникальная последовательность аминокислотных остатков в цепи, присущая данному белку, называется первичной структурой белка . Особенности скручивания цепей белковых молекул (взаимное расположение фрагментов в пространстве) называютсявторичной структурой белков . Полипептидные цепи белков могут соединяться между собой с образованием амидных, дисульфидных, водородных и иных связей за счет боковых цепей аминокислот. В результате этого происходит закручивание спирали в клубок. Эта особенность строения называется третичной структурой белка . Для проявления биологической активности некоторые белки должны сначала образовать макрокомплекс (олигопротеин ), состоящий из нескольких полноценных белковых субъединиц. Четвертичная структура определяет степень ассоциации таких мономеров в биологически активном материале.
Белки делятся на две большие группы - фибриллярные (отношение длины молекулы к ширине больше 10) и глобулярные(отношение меньше 10). К фибриллярным белкам относится коллаген , наиболее распространенный белок позвоночных; на его долю приходится почти 50% сухого веса хрящей и около 30% твердого вещества кости. В большинстве регуляторных систем растений и животных катализ осуществляется глобулярными белками, которые носят название ферментов .
71. Диагностика дефицита питательных элементов в растениях.
Для повышения продуктивности сельскохозяйственных посевов необходимо создать оптимальные условия питания растений и корректировать их в течение вегетации.
Диагностику питания растений подразделяют на почвенную и растительную. Почвенную диагностику проводят путем агрохимического анализа почвы и сопоставления полученных данных с установленными нормативами. Однако анализа почвы не всегда достаточно для определения обеспеченности растений минеральным питанием, так как питательные вещества могут не усваиваться растением. Поэтому наряду с почвенной проводят растительную диагностику -химический анализ растений, или определение нарушения питания по внешнему виду растений, т.е. визуальную диагностику.
Остановимся подробнее на визуальной диагностике. В ее основе лежат наблюдения за изменением окраски растений, появлением на листьях и стеблях пятен, полос, некрозов тканей, отклонениями в строении растений.
В чем состоит сложность визуальной диагностики ?
Сложность визуальной диагностики состоит в том, что очень сходные проявления могут иметь разные неблагоприятные воздействия. Например, очень похожими по внешнему виду могут быть признаки недостатка азота и воды, опрыскивание пестицидами может вызвать краевой ожог листьев или появление бурых пятен, свойственное недостатку калия или кальция. Нередко наблюдается проявление признаков недостатка или избытка не одного, а двух или нескольких элементов питания одновременно. Так, у картофеля на сильнокислых супесчаных почвах часто наблюдают совместное проявление признаков недостатка магния и вредного действия марганца. Кроме того, признаки голодания могут появляться, исчезать и снова возникать. Это зависит от погодных условий, проникновения корней в глубокие слои почвы и изменения потребностей растений в отдельных элементах питания в процессе их роста и развития.
Существенным недостатком листовой диагностики является появление внешних признаков лишь при значительном голодании в отношении того или иного элемента. Но надо иметь в виду, что признаки голодания обычно появляются сначала у одиночных растений и лишь постепенно распространяются на весь посев или насаждение. Поэтому систематический еженедельный внимательный осмотр растений позволяет исправить ситуацию с помощью подкормки.
При визуальной диагностике прежде всего следует установить, внешний вид каких частей растения нарушен. Элементы питания по их подвижности в растении делятся на две группы: реутилизируемые и нереутилизируемые.
Что называется реутилизацией элементов минерального питания?
Реутилизация - повторное использование элементов. При недостатке реутилизируемых элементов они оттекают из ранее образовавшихся частей растения в молодые, формирующиеся органы. К таким элементам относятся N, К, Р, Мд. Поэтому их недостаток прежде всего и ярче проявляется на нижних закончивших рост листьях. Недостаток остальных элементов (Са, S, Fe и всех микроэлементов), нереутилизируемых или слабо реутилизируемых, отражается на самых молодых растущих частях растения. Так, очень близкие по внешнему виду хлорозы при недостатке азота проявляются на листьях нижнего яруса, а при недостатке железа - на верхнем, более молодом ярусе. Побурение и отмирание тканей по краям листа (краевой ожог) при недостатке калия наблюдаются сначала на более старых листьях, а при недостатке кальция - на молодых.
72. Ретарданты, их действие на растение. Возможности практического использования ретардантов.
Ретарданты – это синтетические регуляторы роста растения, обладающие ингибирующими свойствами. Такие препараты способствуют замедлению роста стеблей в высоту и в целом влияют на физиологию и морфологию культур. Ретарданты нашли широкое применение на зерновых культурах, а также рапсе, винограде и др.
Действие ретардантов
Ретарданты являются ингибиторами биосинтеза гиббереллина, замедляющего рост стебля в высоту. Они подавляют растягивание клеток стеблей в период их роста, но усиливают их деление в поперечном направлении без ущерба для других основных физиологических процессов. За счет такого механизма высота растения уменьшается, что гарантирует повышение прочности растения и увеличение размеров колоса. Также действующие вещества регуляторов роста способствуют развитию корневой системы культуры, увеличению образования в листьях хлорофилла, благодаря чему окраска становится более насыщенной и темной. Все это позволяет сделать растение более устойчивым к воздействию неблагоприятных факторов окружающей среды.
Эффективность применения регуляторов роста
Основная задача, с которой помогают справиться регуляторы роста – это предотвратить полегание посевов, которое в свою очередь негативно сказывается на прохождении фаз колошения, цветения, налива зерна, а также уменьшает количество зерен в колосе, сокращает отток питательных веществ в зерна. Полегание посевов также затрудняет процесс выращивания культур, технологически ограничивая внесение удобрений, ухудшая качество урожая и усложняя его уборку.
Ретарданты делают растения более прочными и устойчивыми к воздействию неблагоприятных факторов внешней среды и, как следствие, к полеганию посевов. Благодаря уплотнению стебля снижается риск заражения пятнистостью и другими болезнями. Таким образом, регуляторы роста растений позволяют:
существенно уменьшить риск полегания посевов;
повысить урожайность;
вносить более высокие нормы азотных удобрений под планируемый урожай;
снизить риск возникновения листостебельных болезней и болезней колоса;
ускорить и облегчить уборку урожая.
73. Структура и функции устьичного аппарата растений. Суточный ход устьичных движений.
Строение и работа устьичного аппарата. Устьица растений, как уже было неоднократно сказано, выполняют две основные функции: осуществляют газообмен между внутренними тканями растений и внешней средой; обеспечивают транспирацию (испарение).
Устьице состоит из двух специализированных замыкающих клеток и щелевидного отверстия между ними – устьичной щели (рис. 46). К замыкающим клеткам примыкают так называемые побочные (околоустьичные) клетки. Под устьицем в мякоти листа расположена воздушная полость. В процессе эволюции у растений выработалось приспособление, регулирующее интенсивность испарения: устьица способны автоматически закрываться или открываться по мере необходимости. Изменение размера устьичной щели обусловлено тургорными явлениями.
 Рис.
46. Строение устьичного аппарата:
А – вид сверху; Б – поперечный разрез;
1 – замыкающие клетки; 2 – устьичная
щель; 3 – ядро замыкающей клетки; 4 –
хлоропласты; 5 – ядро клетки эпидермы;
6 – воздушная полость
Рис.
46. Строение устьичного аппарата:
А – вид сверху; Б – поперечный разрез;
1 – замыкающие клетки; 2 – устьичная
щель; 3 – ядро замыкающей клетки; 4 –
хлоропласты; 5 – ядро клетки эпидермы;
6 – воздушная полость
Замыкающие клетки устьица существенно отличаются от остальных клеток эпидермы. Они имеют очертания семян фасоли или боба, и их стенки неравномерно утолщены: те, что обращены друг к другу, значительно толще остальных и практически не растяжимы. В замыкающих клетках находится большое число хлоропластов, и активно идет фотосинтез. В процессе фотосинтеза в них образуются и накапливаются углеводы, что приводит к повышению осмотического потенциала. Вода из соседних клеток эпидермы устремляется в замыкающие клетки: их объем увеличивается, в них резко возрастает тургорное давление. При увеличении объема наружные тонкие стенки замыкающих клеток растягиваются, а утолщенные внутренние стенки становятся вогнутыми и раздвигаются. Устьица открываются. В ночное время в результате прекращения фотосинтеза концентрация веществ в клеточном соке этих клеток уменьшается, тургор падает и устьица закрываются. Устьичная щель закрывается также и при недостатке влаги, так как замыкающие клетки не способны в таких условиях поддерживать высокое тургорное давление.

Итак, мы убедились в том, что устьичные движения регулируются основными факторами внешней среды светом, температурой, содержанием влаги в почве, влажностью воздуха и концентрацией СОг в воздухе се эти переменные воздействуют на такие внутренние факторы, как содержание воды и концентрацияабсцизовой кислоты в листе. Кроме этого, имеют место также ритмические колебания отверстости устьиц, совершающиеся даже в отсутствие внешних воздействий. Эти ритмические колебания регулируются внутренним осциллятором —биологическими часами растения, о которых мы будем говорить в гл. 12. Рис. 6.15 иллю>стрирует суточный ход устьичных движений, регулируемый внутренними ритмами и внешними факторами вместе. Если открывание и закрывание устьиц вызываютсявнутренними факторами, то речь идет об автономных движениях. Хотя они, следовательно, и не относятся к настиям, мы о них все же коротко расскажем. Например, способность реагировать надействие внешних факторов сильно зависит от времени суток. Поэтому говорят о циркадных (имеющих примерно суточную периодичность) компонентах движений устьичных клеток. Это можно показать, если внешние условия остаются неизменными. Так, в частности, Musa a uminata — растение родом из тропиковВосточной Азии, относящееся к семейству банановых, — обнаруживает правильное чередование готовности минимально и максимально открывать устьичные щели . Указателем времени для поддержания этого ритма служит наступление темноты. После рассмотрения настий мы поговорим об автономных движениях подробнее.

74. С-4 растения, их физиологические особенности.
Ряд растений, происходящих из тропиков (например, кукуруза, сорго, сахарный тростник), имеют другой тип фиксации СО2, принципиально отличающийся от цикла Кальвина. Этот путь ассимиляции СО2 был назван С4-путём фотосинтеза или циклом Хетча-Слэка-Карпилова, по имени австралийских учёных: М. Хетча, К. Слэка и русского исследователя Ю.С. Карпилова, впервые описавших этот цикл (рис. 7), а растения с таким путём фотосинтеза называют С4-растениями.
С4-растения имеют особое анатомическое строение листьев. У них хорошо развита проводящая система, сосудистые пучки окружены крупными клетками паренхимы (клетки обкладки пучков). Листья этих растений содержат два разных типа хлоропластов: хлоропласты обычного вида - в клетках мезофилла и большое количество крупных хлоропластов, часто не имеющих гран, - в клетках, окружающих проводящие пучки (обкладка).
В мелких клетках мезофилла листа происходит первичное акцептирование СО2 по С4-пути, характерной особенностью которого является то, что СО2 присоединяется к фосфоенолпировиноградной кислоте (ФЕП) - трёхуглеродному соединению, содержащему макроэргическую связь. В результате этого карбоксилирования образуется четырёхуглеродная щавелевоуксусная кислота (ЩУК), что и позволило назвать этот путь С4-путь фотосинтеза.
Реакцию карбоксилирования катализирует фермент фосфоенолпируваткарбоксилаза (ФЕП-карбоксилаза), которая может работать при гораздо более низких концентрациях СО2, чем рибулозодифосфаткарбоксилаза в цикле Кальвина). Затем образующиеся четырёхуглеродные кислоты диффундируют из клеток мезофилла в клетки обкладки, где распадаются на пировиноградную кислоту (ПВК) и СО2 с образованием восстановленного НАДФ·Н2. Освобождающийся СО2 поступает в цикл Кальвина и присоединяется к рибулозодифосфату, а пировиноградная кислота (ПВК) возвращается в клетки мезофилла, где с участием АТФ превращается в ФЕП и цикл повторяется (рис. 7).
Таким образом, С4-путь является как бы дополнительным насосом (помпой), поставляющим добавочные порции СО2, повышает его концентрацию в растении, ибо концентрация СО2 в ассимиляционной ткани ниже, чем в воздухе является лимитирующим фактором в процессе фотосинтеза.
Растения С4-типа являются одними из наиболее продуктивных культур. Так, при оптимальных условиях, интенсивность фотосинтеза у кукурузы (С4-растение) в 2-2,5 раза выше, чем у пшеницы (С3-растение).
Хлоропласты разных типов клеток характеризуются и разным типом фосфорилирования. В клетках мезофилла в основном идёт нециклическое фосфорилирование и образуется НАДФ·Н, необходимый для цикла Кальвина, идущего в клетках обкладки. В хлоропластах клеток обкладки осуществляется циклическое фосфорилирование.

-
Клетка мезофилла
КС
Клетка обкладки
СО2
НАДФ·Н
НАДФ+
НАДФ·Н
![]() СО2 3-ФГК
СО2 3-ФГК
|
|
Яблочная к- |
РДФ |
Цикл |
ФЕП |
ЩУК |
|
||
та |
|
Кальвина |
||
|
|
|
АМФ+РРi |
АТФ+Рi |
|
|
|
ПВК |
Сахар, |
Сахароза |
C4 - путь |
крахмал |
||
|
|
|
Проводящийсосуд |
Рис.7. С4 - путь фотосинтеза (цикл Хэтча-Слека-Карпилова); КС – клеточная стенка.
К этому можно добавить, что положение клеток обкладки создаёт условия для передачи конечных продуктов фотосинтеза (в частности, сахарозы) непосредственно в ситовидные трубки флоэмы, по которым эти продукты могут затем транспортироваться в другие части растения.
С4-растения имеют ещё ряд преимуществ. У них почти отсутствует фотодыхание, растения же С3-типа характеризуются высокой интенсивностью этого процесса. Под фотодыханием понимают процесс поглощения О2 и выделения СО2 активируемый светом, при котором может "сжигаться" до 50% органических веществ, образующихся в процессе фотосинтеза. При этом не происходит синтез АТФ.
75. Особенности питания бобовых растений.
Бобовые растения играют, по-видимому, главную роль в связывании молекулярного азота в возделываемых почвах. Однако неправильно было бы думать, что все виды бобовых растений в равной степени обогащают почву. Общее увеличение количества азота в надземной массе и пожнивных остатках при культивировании люпина составляет 150 - 200 кг, клевера красного - 180 кг, люцерны - 300 кг, донника - 150 кг, зерновых бобовых - 50 - 60 кг азота в год на 1 га почвы. При этом прибыль азота в почве для всех перечисленных видов, за исключением зерновых бобовых, составляет примерно 50 - 70 кг на 1 га.
Бобовые растения, как известно, выносят с урожаем значительно больше калия, чем другие сельскохозяйственные культуры. Поэтому калийные и особенно фосфорно-калийные удобрения существенно повышают продуктивность азотфиксации бобовыми растениями.
Бобовые растения обогащают почву азотом и являются хорошими предшественниками для других культур. В урожае бобовых растений содержится больше азотистых веществ, и особенно белка, чем у злаковых культур.
Бобовые растения из травостоя по ряду причин выпадают. К числу причин, обусловливающих выпадение бобовых трав на лугах и пастбищах, относятся: недостаток в почве фосфора и калия, чрезмерное увлажнение, к которому более приспособлены злаковые травы и в этих условиях они вытесняют бобовые растения. Азотные удобрения стимулируют рост злаковых трав, которые при этом условии больше потребляют фосфора и калия, создавая тем самым относительный недостаток в этих элементах для бобовых растений, что приводит к вытеснению их из травостоя. Повышение дозы фосфора и калия снижает отрицательное влияние азотных удобрений на бобовые растения в смешанном травостое.
Влияние времени внесения навоза на поедаемостъ травы окотом, по П. И. Ромашеву. Влияние времени внесения навоза на поедаемостъ травы окотом, по П. И. Ромашеву.
Бобовые растения лучше развиваются на почвах с нейтральной или слабощелочной реакцией, исключение состав ляет клевер белый, который дает максимальный урожай при той же оптимальной реакции, что и злаковые травы.
Бобовые растения особенно чувствительны к повышенной кислотности почв.
Влияние нитрагина на урожай бобовых. Влияние нитрагина на урожай бобовых.
Бобовые растения обогащают почву азотом и являются хорошими предшественниками для других культур. В урожае бобовых растений содер жится больше азотистых веществ, и особенно белка, чем у злаковых культур.
Бобовые растения потребляют кальция и серы гораздо больше, чем другие сельскохозяйственные культуры, поэтому они особенно сильно отзываются на гипсование.
Бобовые растения при содействии бактерий, живущих на их корнях, могут пользоваться свободным азотом воздуха. Эту особенность азотного питания бобовых растений следует рассматривать как особую форму исторической приспособленности этих растений к питанию органическими формами азота.
Биологическая фиксация азота воздуха микроорганизмами, населяющими почву, и способность некоторых бактерий переводить азотсодержащие органические соединения в неорганические во многом облегчают задачу азотного питания растений. [c.44]
Получение высокого урожая определяется рядом факторов, среди которых ведущее место принадлежит интенсивности синтетических процессов в растении и нормальному корневому питанию. Последнее зависит от способности почвы удовлетворить потребность растений в доступных формах питательных веществ. Анализы растений в разные периоды вегетации на содержание в органах (стеблях, черешках, листьях), в их срезах или в соке растворимых минеральных форм питательных веществ служат показателем обеспеченности ими растений в конкретных условиях. Недостаток тех или иных элементов питания в почве тотчас же отразится на содержании их в органах и соке растений. Это положение послужило основой для разработки ряда простейших методов контроля питания растений в полевых условиях по химическому анализу на содержание элементов питания в соке или по микрореакциям на срезах растений. К их числу относятся метод диагностики азотного питания растений Давтяна, метод упрощенного химического анализа сока растений по Магницкому, метод определения нитратов, аммиака, фосфора и калия на срезах растений по Церлинг. [c.566]
Живот исчезнет за неделю!
Если каждый день пить стакан..
Лето! Худеем быстро!
Как похудеть без спорта и диет? Нужно взять простой...
Условия азотного питания оказывают большое влияние на рост и развитие растений. При недостатке азота рост их резко ухудшается. Особенно сильно сказывается недостаток азота на развитии листьев они бывают мелкие, имеют светло-зеленую окраску, преждевременно желтеют (рис. 35), стебли становятся тонкими и слабо ветвятся. Ухудшается также формирование и развитие репродуктивных органов и налив зерна. При нормальном азотном питании растений повышается синтез белковых веществ, усиливается и дольше сохраняется жизнедеятельность организма, ускоряется рост [c.186]
Основные научные работы посвящены изучению питания расте-н.пи и применению удобрений. Сформулировал (1916) теорию азотного питания растений, ставшую классической исследовал пути превращения азотсодержащих веществ в растениях, разъяснил роль аспарагина в растительном организме. Разработал научные основы фосфоритования почв. Дал физиологическую характеристику отечественных калийных солей. Апробировал различные виды азотных и фосфорных удобрений в основных земледельческих районах СССР. Изучал вопросы известкования кислых почв, гипсования солонцов, применения органических удобрений. Усовершенствовал методы изучения питания растений, анализа растений и почв. Автор классического руководства Агрохимия (3-е изд. 1934), [c.412]
Количество и состав основных продуктов фотосинтеза зависят от физиологического состояния растения и окружающей среды. В большинстве случаев преобладающая часть фиксированной углекислоты обнаруживается в виде углеводов (сахарозы и крахмала). Переход углерода в аминокислоты и белки отражает до некоторой степени условия азотного питания растения. При низком парциальном давлении углекислого газа основным продуктом фотосинтеза является гликолевая кислота. [c.282]
Частично элементы зольного и азотного питания растения поступают в него через листья, например аммиак и окислы серы из воздуха, соли, содержащиеся в дождевой воде, микроэлементы. Однако обычно таким [c.89]
По скорости разложения органические вещества кала и подстилки можно разделить на две группы. Первая из них, составляющая небольшую долю, включает сравнительно легко разлагающиеся соединения — сахара, крахмал, пентозаны, пектин, органические кислоты. Разложение их при доступе кислорода происходит очень быстро и сопровождается повышением температуры до 60—70°. Вторая группа включает клетчатку и другие медленнее разлагающиеся органические вещества. Скорость разложения навоза зависит от соотношения в нем этих двух групп органических соединений. Чем больше содержится веществ первой группы, тем быстрее идет разложение. Важно, чтобы распад безазотистых органических веществ навоза в основном происходил при его хранении, еще до внесения в почву. В противном случае возникает опасность сильного биологического поглощения азота микроорганизмами после внесения навоза в почву и ухудшаются в связи с этим условия азотного питания растений. [c.356]
Для повышения содержания белка в яровых зерновых культурах большое значение имеет азотное питание растений в период выхода в трубку, колошения и цветения. Азот, поступающий в растение в эти фазы, используется в основном для образования семян, в результате чего содержание азота в них повышается, и В период налива зерна синтез белков идет более интенсивно. [c.419]
Работами лаборатории азота НИУИФ (Ф. В. Турчин и др.) внесено много нового в изучение азотного питания растений с использованием изотопа [c.562]
Д м и т р п 1 Николаевич Прянишников (1865—1948) — академик, Герой Социалистического Труда, лауреат Ленинской и Государственных премий, основоположник и руководитель советской школы агрохимиков. Автор многочисленных научных трудов, в том числе по вопросам азотного питания растений. [c.403]
Так, без азотного питания растение развиваться не может. Азот увеличивает количество и улучшает качество урожая. Но при избытке в почве легко усваиваемого азота в растении накапливаются нитраты, что уменьшает биологическую полноценность пищи и кормов. Кормовые культуры, содержащие больше 0,25 % нитратов, вредны для животных, вызывают их заболевания, снижают продуктивность. Естественно, избыток нитратов в пище вреден и для человека.
АЗОТНОЕ ПИТАНИЕ РАСТЕНИЙ
Влияние уровня азотного питания растений сахарной свеклы на размеры клеток мезофилла листьев и число хлоропластов в этих клетках
Факторы внешней среды сильно влияют на соотношение направлений синтеза углеводных и неуглеводных продуктов. Хотя не ясны еще звенья в ферментативной цепи, на которые влияет тот или иной фактор, установлено, что усиление азотного питания растений повышает синтез аминокислот и белков уменьшение соотношения НАДФН/АТФ против нормы может затруднить синтез [c.37]
Применение связанного азота. В почвах содержание соединений азота, которые могут усваиваться растениями, очень мало и поэтому основным источником азотного питания растений является азот воздуха. Как уже указывалось, в природе имеются два пути связывания атмосферного азота и пополнения ресурсов азота почвы — электрический разряд и способность некоторых бактерий связывать азот. Однако этого недостаточно. Поэтому возникла практическая задача обеспечения растений азотным питанием для увеличения урожайности сельскохозяйственных культур путем внесения в почву соединений, содержащих азот, — азотных удобрений. [c.87]
Д.Н. Прянишников в 1916 году создал теорию азотного питания растений и сформулировал теоретические основы процессов фосфори-лирования, известкования и гипсования почв для улучшения их свойств.
Таким образом, зависимость эффективности воздействия кинетина от условий азотного питания растений оказалась неодинаковой в отношении отдельных физиологических признаков. Цветение было более заметно ускорено кинетином при сниженной дозе азота, вызвавшей запоздание цветения, содержание НК в корнях возрастало больше при сниженной дозе азота, тогда как в стеблях содержание РНК повышалось значительнее при высокой дозе. Для роста же растений (кроме корней) обильное снабжение азотом оказалось необходимым для активирования накопления сухого вещества под действием кинетина. Возможно, что для проявления активирующего действия кинетина обилие азота необходимо пото-
Эффективность зеленого удобрения. При правильной агротехнике люпин на песчаных почвах к моменту запашки дает урожай зеленой массы 30—40 т с 1 га, а на легкосуглинистых и суглинистых почвах — до 60—80 т с I га. Зеленая масса люпина содержит около 0,5% азота, т. е. примерно столько же, сколько и навоз. Следовательно, при запашке люпина в почву вносится от 150—200 до 300—400 кг азота, который в процессе разложения зеленого удобрения становится мощным источником азотного питания растений. Кроме того, корневые и пожнивные остатки люпина составляют более 2 т на 1 га.
Регулируя уровень азотного питания и соблюдая правильное соотношение основных элементов пищи в удобрениях с учетом биологических особенностей сельскохозяйственных растений, можно добиться значительного увеличения урожая. При нормальном азотном питании растений повышается
Одним из факторов, регулирующих пути усвоения СО при фотосинтезе, являются условия питания растений. Так, например,синтез белков, происходящий в хлоропластах на свету (стр. 47 ) в сильной стеиени зависит от уровня азотного питания растений (Осипова, 1953 Андреева, 1969). В хлоропластах растений, хорошо обеспеченных азотом, усиливается синтез не только структурных белков, но и белков ферментных систем, участвующих в реакциях восстановительного цикла углерода. Это, в частности, по
Главными неорганическими соединениями азота в почвах являются нитрат, аммоний и в редко встречающихся условиях нитрит. Поведение первых двух компонентов в почве совершенно различно. Если нитрат является легкоподвижным соединением, не сорбируется минералами почвы и остается в растворенном в воде состоянии, то аммоний легко хемосорбируется глинистыми минералами, хотя это не мешает ему в определенных условиях легко окисляться до нитрата. Такое различие в подвижности нитрата и аммония предопределяет источники азотного питания растений. С энергетических позиций аммонийная форма азота более предпочтительна, так как валентность азота в ней одинакова с валентностью азота в аминокислотах.
Д. Н. Прянишников доказывал, что для нашей страны более перспективно не травополье, а интенсивные плодосменные севообороты. Именно они пришли на смену трехполью зернового типа, господствовавшему на протяжении тысячи лет в Западной Европе. При трехполье треть земли пустовала (поздний пар), а две трети засевались зерновыми культурами. Бобовые не возделывали, что исключало возможность мобилизации азота воздуха с помощью клубеньковых бактерий и отрицательно сказывалось на азотном питании растений и круговороте азота в земледелии. В этом севообороте почти отсутствовали и пропашные, в том числе картофель и корнеплоды, что приводило к засоренности полей и постоянному недостатку кормов. На протяжении столетий крестьянское хозяйство (за исключением кулацкой верхушки) не могло вырваться из порочного круга, отмеченного известным русским агрономом ХУП в. А. Т. Болотовым, который писал ...без навоза земля не дает урожая, а навоза мало, так как мало скота,
Применяя метод хроматографии в исследованиях азотного питания растений, Ф. В. Турчин (1954) установил, что поступающий в растение аммиачный азот уже через 10—15 минут превращается в корнях в аминокислоты. В нормальных условиях роста и при концентрации аммиачного азота, не превышающей известные пределы, он полностью перерабатывается в корнях в аминокислоты и не доходит до надземных органов. При некотором избытке аммиачного азота в среде и недостаточном снабжении калием скорость поступления аммиака в растение заметно превышает скорость его использования на синтез аминокислот в таких случаях аммиак может накапливаться в растениях. Образование многих аминокислот в корнях подтверждено также Е. И. Ратнером и И. И. Колосовым (1954). Эти авторы четко установили, что корневая система обладает ясно выраженными синтетическими функциями и что указанные первичные превращения минерального азота в органические соединения осуществляются корнями и в строго стерильных условиях, та есть без помощи микроорганизмов.
Современные способы применения удобрений позволяют вносить азотные удобрения с учетом изложенных особенностей азотного питания растений в различные периоды их роста.
Азотобактерин содержит культуру свободноживуще-го микроба азотобактера (Azotoba ter). Практически азотобактерин не оказывает сущеста влияния на азотное питание растений, как предполагали до 1970-х гг. Вместе с тем в ряде случаев он действительно улучшает рост растений. Это объясняют способностью азотобактера 1) синтезировать комплекс биологически активных в-в-стимуляторов роста растений, напр, биотина, гетероауксина, пнридоксина 2) образовывать антимикробные в-ва, угнетающие развитие фитопатогенных грибов и бактерий - возбудителей корневой гнили растений. Действие азотобактерина, выпускаемого в виде сухого препарата и применяемого для обработки семян овощных культур и рассады, лучше всего может проявляться на нейтральных плодородных почвах, достаточно обеспеченных органическими в-вами и фосфором.
Поэтому в кислых почвах сильно ослаблена или вовсе прекращается фиксация азота воздуха, замедляется минерализация органического вещества, процесс нитрификации подавлен, в результате чего резко ухудшаются условия азотного питания растений. В кислых почвах подвижные формы фосфора связываются полуторными окислами с образованием нерастЕори-мых и малодоступных растениям фосфатов алюминия и железа..
За рубежом синтетический аммиак первоначально перерабатывали в малоконцентрированные удобрения — сульфат аммония и известково-аммиачную селитру, содержащие 21% азота, однако аммиачную селитру не применяли в сельском хозяйстве из-за ее взрывоопасности (известен взрыв в Оннау в 1921 г., когда нри разрыхлении с помощью взрывчатых веществ слежавшейся двойной соли сульфата—нитрата аммония произошла детонация с катастрофическими последствиями). Еще в 1903 г. академик Д. Н. Прянишников, внесший большой вклад в изучение азотного питания растений, называл аммиачную селитру удобрением будущего . В конце 20-х годов, когда в СССР только закладывался фундамент азотной промышленности и необходимо было установить ассортимент азотных удобрений, особое внимание было обращено на перспективность использования в сельском хозяйстве аммиачной селитры, единица азота в которой оказывалась наиболее дешевой. В результате глубокого изучения свойств, в том числе взрывоопасности, аммиачной селитры и особенно благодаря полевым опытам в различных зонах в основу отечественной азотной промышленности с самого начала ее развития была положена переработка аммиака в аммиачную селитру.
Таким образом, растения в почвенных условиях питаются неорга-иическими соединениями в виде ионов. Они могут поглощать и некоторые органические соединения (например, аминокислоты и др.), но ссГдержание этих соединений в почве очень невелико. Азотное питание растений осуществляется у бобовых и некоторых
НИТРАТНЫЕ УДОБРЕНИЯ (селитры). Азотные удобрения, содержащие азот в форме нитратов. К ним относятся натриевая, кальциевая и калийная селитры. Селитры аммиачная и кальциевоаммиачная являются аммиачно-нитратными удобрениями, так как они содержат азот одновременно в нитратной и аммиачной форме. Нитратные формы азота легко растворимы в воде, не поглощаются почвой, легко вымываются атмосферными осадками в нижние слои почвы и также легко в сухие периоды года выносятся с восходящими токами влаги в поверхностный слой почвы. Благодаря высокой подвижности в почве нитратный азот быстро усваивается растениями. Поэтому Н. у. весьма пригодны для подкормок, когда требуется быстрое усиление азотного питания растений. Высокая подвижность Н.у. ограничивает возможность их использования для основного осеннего внесения под яровые культуры, особенно на легких почвах, где возможны значительные потери Н. у. вследствие вымывания их осенними дождями и талыми водами.
Неиспользованные живым веществом запасы химически связанного азота под действием микроорганизмов непрерывно преобразовываются в формы, доступные для азотного питания растений. Так, фиксированный глинистыми минера.лами аммоний окисляется до нитратов. В определенных условиях при отсутствии свободного кислорода и наличии неиспользованного живым веществом нитрата может происходить обусловленное процессом денитрификации восстановление азота до мо.чекулярного с уходом последнего в атмосферу.
Частично элементы зольного и азотного питания растения поступают в него через листья, например аммиак и окислы серы из воздуха, соли, содержащиеся в дождевой воде, микроэлементы. Однако обычно таким путем потребности культур в питательных веществах не могут быть удовлетворены. Так, аммиака в 1 м воздуха содержится лишь около /50 мг. Количество окислов серы в воздухе бывает заметным в индустриальных районах при некотором минимуме сульфатной серы в почвах растения в состоянии усваивать и ее окислы из атмосферы. Однако только газообразными источниками серы нельзя обеспечить потребность в ней культуры (Олсен, 1957). Микроэлементы с осадками оседают на листья лишь в приморских областях.
При запашке всей зеленой массы бобовых культур почва обогащается азотом в количестве, обеспечивающем хорошее азотное питание растений, высеваемых иосле бобовых. Бобовые культуры (на зерно, сено или зеленый корм) оставляют азота в почве гораздо меньше, чем отдают с урожаем. Тем не иенее по любому бобовому растению азотное питание сельскохозяйственных культур обеспечено лучше, чем по небобовому предшественнику, если только не вносятся азотные удобрения.
Закономерности азотного питания растений, о которых выше шла речь, открыты и изучены выдающимся советским згченым Д. Н. Прянишниковым. Трудами Д. Н. Прянишникова разрешена одна из самых сложных проблем питания культурных растений. Вместе с тем исследования Д. Н. Прянишникова и его учеников подняли на новую ступень нашу отечественную науку о питании растений и применении удобрений — агрономическую химию, которая в течение многих лет занимает ведущее место в мире.
Для зерновых, овощных культур, корнеплодов и картофеля выпускают бактериальное удобрение— азотобактерин, которым обрабатывают посевной материал так же, как и нитрагином. Бактерии, содержащиеся в азотобактерине, живут не на корнях, а вблизи них. Они питаются органическим веществом, минеральные соли усваивают из почвы, азот — из воздуха. В дальнейшем азотом, усвоенным этими бактериями, пользуются растения. Азотобактер накопляет в почве азота во много раз меньше, чем клубеньковые бактерии, но все же несколько улучшает азотное питание растений. При использовании азотобактера необходимо помнить, что на кислых почвах он погибает, поэтому и обрабатывать семена азотобактерином на кислых почвах не имеет смысла. На таких почвах применение азотобактерина будет эффективно только при известкованхга почв.

