
- •Оглавление
- •Введение
- •Краткие указания к практическим занятиям Правила работы в лаборатории органической химии
- •Первая помощь при несчастных случаях в лаборатории
- •I. Методы выделения и очистки органических веществ
- •Опыт № 1. Перекристаллизация бензойной кислоты
- •Опыт №2. Возгонка (сублимация) бензойной кислоты
- •Опыт №4. Определение температуры плавления бензойной кислоты
- •Опыт №5. Разделение смеси веществ простой перегонкой
- •II. Качественный элементный анализ органических соединений
- •Опыт № 8. Обнаружение углерода и водорода
- •Опыт № 9. Обнаружение азота
- •Опыт № 10. Обнаружение галогенов (проба Бейльштейна)
- •Опыт № 11. Обнаружение серы
- •Опыт № 13. Получение и свойства этилена
- •Опыт №14. Получение и свойства бензола
- •IV. Галогенопроизводные углеводородов (галогеноуглеводороды)
- •Опыт № 15. Получение хлорэтана
- •V. Спирты. Простые эфиры
- •Опыт № 16. Обнаружение воды в спирте-ректификате
- •Опыт № 18. Окисление этилового спирта перманганатом калия
- •Опыт № 19. Получение простого (диэтилового) эфира
- •Опыт № 20. Получение сложного (уксусноэтилового) эфира
- •VI. Фенолы. Нафтолы
- •Опыт № 21. Получение фенолята натрия
- •Опыт № 24. Взаимодействие α- и β-нафтолов с хлоридом железа (III)
- •VII. Альдегиды и кетоны
- •Опыт № 25. Получение уксусного альдегида из этанола
- •Опыт № 26. Окисление альдегида. Образование серебряного зеркала
- •Опыт № 27. Реакция диспропорционирования формальдегида (реакция Канницаро)
- •Опыт № 28. Окисление формальдегида гидроксидом меди (II) в щелочной среде
- •Опыт № 29. Цветные реакции на альдегиды
- •Опыт № 30. Образование альдегидами и кетонами гидросульфитных производных
- •Опыт № 31. Йодоформная проба на ацетон
- •Опыт № 32. Окисление бензойного альдегида кислородом воздуха
- •VIII. Карбоновые кислоты и их производные
- •Опыт № 33. Получение уксусной кислоты из ацетата натрия
- •Опыт № 34. Получение и гидролиз ацетата железа (III)
- •Опыт № 35. Устойчивость уксусной кислоты к действию окислителей
- •Опыт № 36. Окисление муравьиной кислоты
- •Опыт № 37. Разложение муравьиной кислоты
- •Опыт № 38. Окисление олеиновой кислоты перманганатом калия (реакция Вагнера)
- •Опыт № 39. Разложение щавелевой кислоты при нагревании
- •Опыт № 40. Окисление щавелевой кислоты
- •IX. Гидроксикислоты
- •Опыт № 42. Разложение молочной кислоты при нагревании с концентрированной серной кислотой
- •Опыт № 43. Разложение молочной кислоты при нагревании с разбавленной серной кислотой
- •Опыт № 44. Окисление молочной кислоты в пировиноградную кислоту
- •Опыт № 45. Получение реактива Фелинга
- •Опыт № 46. Разложение лимонной кислоты при нагревании
- •Опыт № 47. Получение ацетилсалициловой кислоты (аспирин)
- •Опыт № 48. Доказательство отсутствия фенольного гидроксила в ацетилсалициловой кислоте (аспирине) и её гидролиз
- •Опыт № 49. Термическое декарбоксилирование салициловой кислоты
- •Опыт № 50. Взаимодействие салициловой и бензойной кислот с хлоридом железа (III)
- •Опыт № 52. Доказательство наличия гидроксильных групп в винной кислоте
- •Опыт № 53. Взаимодействие галловой кислоты и танина с хлоридом железа (III)
- •Опыт № 54. Обнаружение кислотных свойств ацетоуксусного эфира
- •Опыт № 55. Кетонное расщепление ацетоуксусного эфира
- •X. Углеводы
- •Опыт № 56. Реакция на обнаружение углеводов с -нафтолом (реакция Молиша)
- •Опыт № 57. Доказательство наличия гидроксильных групп в глюкозе
- •Опыт № 58. Восстановление гидроксида меди (II) глюкозой в присутствии щелочи (реакция Троммера)
- •Глюкоза глюконовая кислота
- •Опыт № 59. Взаимодействие глюкозы с реактивом Фелинга
- •Опыт № 60. Восстановление аммиачного раствора оксида серебра (реакция серебряного зеркала)
- •Опыт № 61. Реакция Селиванова на кетогексозы
- •Опыт № 62. Взаимодействие глюкозы со щелочным раствором глицерата меди (реактив Гайнеса)
- •Опыт № 63. Реакция фуксинсернистой кислоты с глюкозой и формальдегидом
- •Опыт № 64. Образование фурфурола и конденсация его с анилином (качественная реакция на пентозаны)
- •Опыт № 65. Доказательство наличия гидроксильных групп у сахарозы
- •Опыт № 66. Восстанавливающая способность дисахаридов
- •Опыт № 67. Инверсия сахарозы при гидролизе
- •Опыт № 68. Приготовление крахмального клейстера
- •Опыт № 69. Реакция крахмала с йодом
- •Опыт № 70. Отсутствие восстанавливающей способности у крахмала
- •XI. Азотсодержащие органические соединения
- •Нитросоединения
- •Опыт № 71. Получение нитрометана
- •Опыт № 72. Разложение мочевины при гидролизе
- •Опыт № 73. Взаимодействие мочевины с азотной кислотой
- •Опыт № 74. Взаимодействие мочевины с азотистой кислотой
- •Опыт № 75. Взаимодействие мочевины со щавелевой кислотой
- •Опыт № 76. Образование биурета
- •Опыт № 77. Определение кислотности аминоэтановой кислоты (глицина)
- •Опыт № 78. Получение медной соли глицина
- •Опыт № 79. Реакции аминокислот с нингидрином
- •Опыт № 80. Реакции аминокислот с формальдегидом
- •Опыт № 81. Реакции аминокислот с азотистой кислотой (дезаминирование)
- •Опыт № 82. Реакция глицина с хлоридом железа (III)
- •Заказ №
Опыт № 61. Реакция Селиванова на кетогексозы
Реактивы:
1% раствор фруктозы
Раствор резорцина в 20% соляной кислоте
Ход работы:
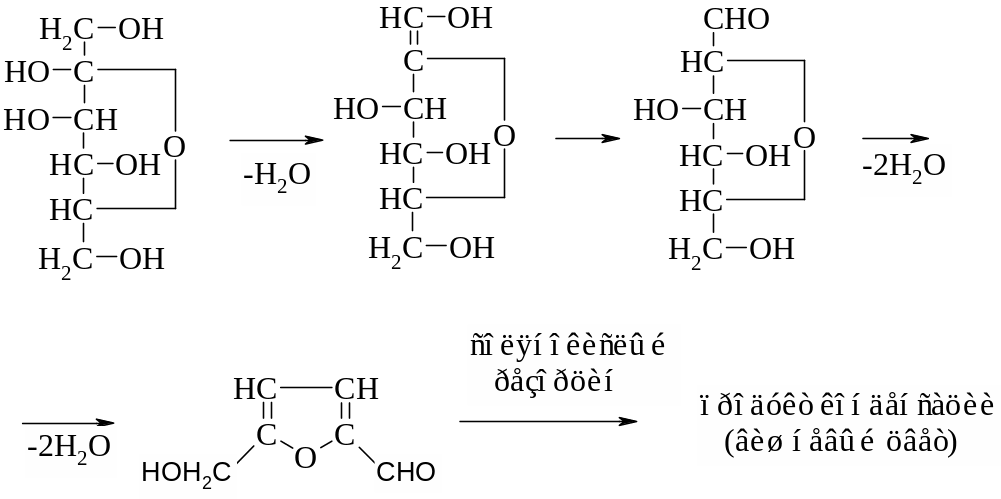
В пробирку берут 2 мл раствора фруктозы (1,1∙ 10-4 моль), приливают к нему 2 мл раствора резорцина в соляной кислоте. После этого содержимое пробирки осторожно нагревают на пламени горелки. Смесь приобретает вишнево-красное окрашивание, что указывает на присутствие кетозы (в данном случае – фруктозы).
Процесс проходит через образование из фруктозы оксиметилфурфурола, который под влиянием соляной кислоты конденсируется с резорцином и дает окрашенные продукты.
Альдозы с реактивом Селиванова реагируют медленно и дают слабую бледно-розовую окраску.
Опыт № 62. Взаимодействие глюкозы со щелочным раствором глицерата меди (реактив Гайнеса)
Реактивы:
Глицерин
1% раствор глюкозы
10% раствор гидроксида натрия
5% раствор сульфата меди
Ход работы:
В пробирку наливают 1 мл 5% раствора сульфата меди (3,2∙10-4 моль), добавляют 0,5 мл 10% раствора гидроксида натрия (1,25∙10-3 моль). К образовавшемуся осадку по каплям приливают глицерин до образования прозрачного синего раствора. К полученному раствору глицерата меди добавляют 1 мл 1% раствора (5,5∙10-5 моль) глюкозы. Держа пробирку в наклонном положении, нагревают до кипения только верхнюю часть пробирки (нижняя часть пробирки должна оставаться холодной для контроля). В верхней части пробирки образуется осадок красного цвета – оксид меди (I) Сu2О. Преимущество метода определения глюкозы реактивом Гейнеса перед реактивом Троммера заключается в его быстроте.
Опыт № 63. Реакция фуксинсернистой кислоты с глюкозой и формальдегидом
Реактивы:
Фуксинсернистая кислота
10% раствор формальдегида
10% раствор глюкозы
Ход работы:
В одну пробирку наливают 2 мл 10% раствора формальдегида, а в другую – 2 мл 10% раствора глюкозы. Затем в первую и во вторую пробирки добавляют по 1 мл бесцветной фуксинсернистой кислоты. В пробирке с формальдегидом через некоторое время окраска раствора меняется, а в пробирке с глюкозой изменения окрашивания не произошло. Раствор глюкозы не окрасился из-за таутомерных превращений, характерных для моносахаридов: альдегидная группа при растворении в воде вступает во взаимодействие со спиртовым гидроксилом, образуя циклическую полуацетальную форму.
Опыт № 64. Образование фурфурола и конденсация его с анилином (качественная реакция на пентозаны)
Реактивы:
Древесные опилки
20% раствор соляной кислоты
Уксусная кислота
Анилин
Фильтровальная бумага (полоски)
Ход работы:
В пробирку насыпают древесные опилки высотой 2 см и наливают 2 мл разбавленной соляной кислоты. Полоску фильтровальной бумаги, смоченную уксусной кислотой и анилином, помещают в пробирку так, чтобы свободный конец бумаги находился снаружи. Содержимое пробирки нагревают до кипения. Через некоторое время фильтровальная бумага окрашивается в красный цвет. При этом содержащиеся в древесине пентозаны в кислой среде гидролизуются:
H+
(С5Н8О4)n + n H2O n C5H10O5
пентозаны пентозы
при нагревании, под действием кислоты пентозы теряют три молекулы воды и превращаются в фурфурол:
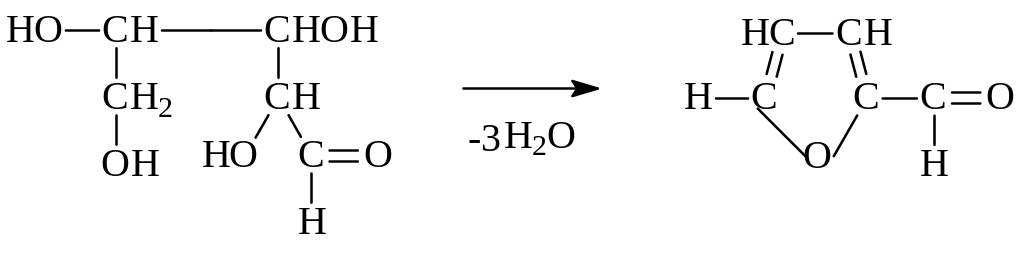
фурфурол с анилином дает продукты конденсации красного цвета.
Ди- и полисахариды
Опыт № 65. Доказательство наличия гидроксильных групп у сахарозы
Реактивы:
1% раствор сахарозы
10% раствор гидроксида натрия
5% раствор сульфата меди
Ход работы:
В пробирку наливают 1 мл 5% раствора сульфата меди (3,2∙10-4 моль), добавляют 0,5 мл 10% раствора гидроксида натрия (1,25∙10-3 моль). К образовавшемуся осадку по каплям приливают 2 мл 1%-ного раствора сахарозы (5,85∙10-5 моль). Полученную смесь встряхивают и получают прозрачный раствор сахарата меди синего цвета.
