
- •Лекция 4
- •Особенности растворения анодов в условиях гальванического нанесения покрытий и оксидирования
- •Тоэ Лекция 5,6
- •2. Катодные процессы
- •2.1. Особенности катодных процессов при размерной эхо
- •3.2.3. Рост кристаллических образований
- •2.2.2.4. Формирование поликристаллических осадков
- •2.2.2.4.1. Последовательность формирования поликристаллических осадков
- •2.2.2.4.2. Крупно- и мелкокристаллические осадки
- •2.2.2.4.3. Блестящие осадки
- •3.2.5. Влияние параллельной реакции выделения водорода на электроосаждение металлов
- •3.2.5.1. Основные закономерности выделения водорода
- •2.2.2.5.2. Катодный выход по току Катодный выход по току для электроотрицательных металлов зависит от
- •Тоэ Лекция 7, 8
- •2.4.3. Влияние рН прикатодного слоя
- •2.4.4. Влияние образующихся пузырьков водорода
- •2.5. Кристаллическая структура электроосаждённых металлов
- •2.5.1. Микроструктура
- •2.5.2. Структура границ зёрен
- •2.5.3. Текстура
- •2.5.4. Связь структуры электроосаждённых металлов с их свойствами
- •2.5.5. Внутренние напряжения в электроосаждённых металлах
- •Тоэ (меньше нормы) Лекция 9
- •2.6. Электроосаждение сплавов
- •Тоэ Лекция 10,11
- •3.1.2. Рассеивающая и кроющая способность электролита. Первичное и вторичное распределение тока
- •3.1.4. Влияние различных факторов на распределение тока и металла
- •3.1.4.1. Влияние профиля электродов. Критерий электрохимического подобия.
- •3.1.4.2. Влияние поляризуемости электродов и электропроводности растворов
- •3.1.4.3. Влияние выхода по току на распределение тока по поверхности электрода
- •3.1.4.4. Влияние условий электролиза на распределение тока на поверхности электрода
- •3.1.5. Искусственные приёмы для получения равномерных покрытий
- •3.1.6. Методы исследования рассеивающей способности электролитов
- •Ячейка представляет собой прямоугольный сосуд – ванну с катодом из тонкой ленты, согнутой в двух местах под углом в 60°. По её обеим сторонам на одинаковом расстоянии расположены два плоских анода.
- •3.2.1.2. Микрораспределение металла на микрорельефе поверхности
- •3.2.1.3. Изменение микрорельефа поверхности при равномерном микрораспределении скорости осаждения
- •3.2.1.4. Влияние особенностей электрокристаллизации на формирование микрорельефа поверхности
- •3.2.2. Природа микрорассеивающей и выравнивающей способности электролита
- •3.2.2.1. Влияние диффузии
- •3.2.2.2. Влияние выравнивающих агентов
- •3.2.2.3. Влияние нестационарных режимов электролиза
- •3.2.3. Методы исследования микрораспределения и оценки выравнивающей и микрорассеивающей способности электролита
- •3.2.3.1. Оценка выравнивающей и микрорассеивающей способности по толщине слоя
- •3.2.3.2. Выравнивающая способность электролита
- •4. Основы теории электроэрозионной обработки металлов
- •4.1. История развития процесса
- •4.2. Общее описание процесса
- •4.3. Стадии протекания электроэрозионного процесса
- •4.4. Основные закономерности процесса ээо
- •В первом приближении энергию аи можно рассчитывать по средним значениям силы тока и напряжения:
- •4.5. Тепловые процессы на электродах
- •4.6. Формы и размер лунок
- •4.6. Особенности протекания процесса в воздушной среде
- •4.7. Структура поверхностного слоя после электроэрозионной обработки
- •"Теоретические основы электрообработки поверхности изделий"
3.2.5. Влияние параллельной реакции выделения водорода на электроосаждение металлов
3.2.5.1. Основные закономерности выделения водорода
Электроосаждение большинства металлов и сплавов из водных растворов сопровождается параллельным протеканием реакции выделения водорода. В зависимости от рН раствора на электроде происходит разряд либо ионов гидроксония, либо молекул воды.
Суммарные электродные реакции имеют вид:
2H3O+ + 2e = H2 + 2H2O
2H2O + 2e = H2 + 2OH¯
Первая из этих реакций протекает в кислых растворах, вторая – в нейтральных и щелочных. Равновесный потенциал реакции:
Ер = -0,059 рН [B]
Рассмотрим два случая. Первый - пусть потенциал электрода под током при выделении металла положительнее равновесного потенциала водородного электрода. В этом случае параллельная реакция выделения водорода не протекает. Катодный выход по току для таких металлов близок к 100%. Так, например, реакция выделения водорода не протекает при электроосаждении меди из кислых сульфатных растворов, а также серебра и золота из электролитов, содержащих комплексные ионы. Это связано с тем, что при обычно используемых плотностях тока осаждения потенциал катода не достигает равновесного потенциала водородного электрода.
Второй случай – пусть потенциал электрода под током при выделении металла отрицательнее равновесного потенциала водородного электрода. В этом случае металлы осаждаются с параллельной реакцией выделения водорода. Причём катодный выход металла по току зависит здесь от перенапряжения выделения водорода на осаждающемся металле.
Перенапряжение выделения водорода зависит от природы металла, состава и рН электролита. Зависимость перенапряжения выделения водорода от плотности тока в достаточно концентрированных растворах и в отсутствии поверхностно-активных ионов и молекул подчиняется уравнению Тафеля:
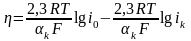
αk – коэффициент переноса катодной реакции; iк – плотность катодного тока.
Первый член в правой части определяет значение перенапряжения при единичной плотности тока (например 1 А/см2). Он зависит от тока обмена (i0) реакции «ионы гидроксония – молекулярный водород». Ток обмена сильно зависит от природы металла и уменьшается в ряду Pd (палладий), Pt, Fe, Au, Ag, Ni, Сu, Tl (таллий), Sn, Pb, Hg. Это соответствует возрастанию перенапряжения выделения водорода в той же последовательности. Величина 2,3RT/αкF слабо зависит от природы металла и для большинства металлов составляет 90-140 мВ. То есть на такое значение происходит увеличение перенапряжения выделения водорода (или сдвиг потенциала под током происходит в отрицательную сторону) при возрастании катодной плотности тока в 10 раз.
2.2.2.5.2. Катодный выход по току Катодный выход по току для электроотрицательных металлов зависит от
значений равновесных потенциалов реакции «металл-ионы металла»;
от перенапряжения выделения водорода на осаждённом металле, зависящем от природы металла, рН и состава раствора;
наличия ПАВ;
температуры электролита.
Выход по току металла определяется соотношением между скоростью его осаждения и скоростью выделения водорода. Пусть. Например, при сдвиге потенциала в отрицательную сторону скорость осаждения металла возрастает быстрее, чем скорость выделения водорода. Тогда выход по току будет увеличиваться при повышении плотности тока. В противном случае выход по току падает с повышением плотности тока.
Аналогичные рассуждения используются и при интерпретации влияния температуры, рН и состава раствора на выход металла по току.
На чистых металлах перенапряжение выделения водорода слабо зависит от структуры образующегося осадка и монотонно возрастает с увеличением плотности тока. При электроосаждении сплавов, напротив, перенапряжение выделения водорода зависит от их состава. Поскольку при каждом потенциале образуются сплавы различного состава, на них перенапряжение выделения водорода может изменяться не монотонно. Это может приводить к сложному характеру зависимости выхода по току от плотности тока. Это особенно характерно для сплавов, одновременно состоящих из металлов с высоким и низким перенапряжением выделения водорода, например Zn-Fe, Zn-Ni и другие.
