
Задача 41.
Прямая или обратная реакция будет протекать при стандартных условиях в системе: СН4(газ) + О2 ... Вычислите изменение изобарно-изотермического потенциала при протекании реакции и на основании этого подсчета дайте ответ.
Ответ:
Предыдущий расчет
CH4(г) + 2O 2(г) = CO2(г) + 2H2О(г).
Выписываем из справочника стандартные значения изобарно-изотермического потенциала при 25 °С :
|
CO2(г) |
H2O(г) |
CH4(г) |
О2(г) |
G0, кДж/моль |
-394,38 |
–228,61 |
–50,79 |
0 |
По следствию из закона Гесса определяем H0 химической реакции

G0 = (2 G 0 (H2О(г)) + G 0 (CO2(г)) – (G 0 (CH4(г)) + 2 G 0 (О2(г)) =
= (2· (–228,61) + (-394,38) –(–50,79 +0) = –800,81 кДж
Т.к. ΔG0 < 0, то реакция протекает в прямом направлении.
Расчет
ΔG по требованию преподавателя
по требованию преподавателя
Для реакции CH4 (г) + 2 O2(г) = CO2(г) + 2 H2O(г)
Значения стандартных энтальпий образования и стандартных энтропий при 25 °С (данные справочника) :
|
Н2О (г) |
CO2(г) |
CH4 (г) |
O2 (г) |
H0, кДж/моль |
-241,84 |
-393,51 |
– 74,85 |
0 |
S0, Дж/моль∙К |
188,74 |
213,6 |
186,19 |
205,03 |
1) Определяем H0298, химической реакции исходя из следствия из закона Гесса

Hх.р. = (2H0 (Н2О (г) + H0(СО2 (г)) – ( (H0 (CH4 (г)) + 2H0 (O2 (г)))=
= (2· (–241,84) + (– 393,51)) – ((– 74,85) + 0) = –877,19 +74,85=
= –802,34 кДж/моль
2) Для определения S0 вновь воспользуемся следствием из закона Гесса:
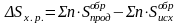
Sx.p. = (2 S0 (Н2О(г)) + S0 (СО2 (г))) – ((S0(CH4(г)) + 2S0 (O2(г))=
= (2· 188,74+ 213,6) – (186,19+ 2·205,03) =591,08 – 596,25 = –5,17 Дж/моль ·К
3) Изменение изобарно-изотермического потенциала определяем по формуле:
ΔGf = H0 - Т S0
ΔGf = –802,34 ·103– 298 (–5,17) = –800799,3Дж/моль = –800,8 кДж
Т.к. ΔG < 0, то реакция протекает в прямом направлении
Можете сравнить полученное значение с предыдущим расчетом.
Задача 11.
Вычислите молярную массу эквивалента и эквивалент угольной кислоты в реакциях: а) Н2СО3 + Mg(OH)2 = MgCO3 + 2Н2O; б) 2Н2СО3 + СаСО3 = Са(НСО3)2 + Н2O: в) Н2СО3 + 2КОН = К2СО3 + 2H2O.
С данными замечаниями согласен
Ответ:
а) H2CO3+Mg(OH)2=MgCO3+2H2O
В ходе реакции кислота образует две новые связи, поэтому
z = 2; fэ= 1/z = 1/2; Mэ = M·f = 62 ·1/2 = 31 г/моль
Эквивалент кислоты равен 1 поделенной на количество атомов водорода, отданных кислотой в ходе реакции. Значит, здесь эквивалент Н2СО3 равен 1/2.
б) 2H2CO3+CaCO3=Ca(HCO3)2+H2O
Одна молекула кислоты отдает один атом водорода в ходе реакции.
z = 1; fэ= 1/z = 1; Mэ = M·f = 62 ·1 = 31 г/моль
в) Н2СО3 + 2КОН = К2СО3 + 2H2O
1 моль Н2СО3 реагирует с 2 моль КОН, поэтому, эквивалент Н2СО3 равен 1/2, тогда
z = 2; fэ= 1/z = ½ ; Mэ = M·f = 62 ·1/2 = 31 г/моль
