
- •Часть I. Растворы
- •I. Общая характеристика растворов
- •II. О теориях растворов
- •III. Коллигативные свойства растворов
- •III.1. Закон Рауля. Лабораторная работа №1. Влияние концентрации малолетучей примеси на давление насыщенного пара над раствором на основе летучего растворителя
- •III.2. Осмос. Лабораторная работа №2.
- •2. Выполнение эксперимента
- •5. Запись термограмм охлаждения
- •6. Устранение возможной метастабильной модификации галлия
- •16. Оформите работу. Сделайте выводы.
- •Программирование криотермостата на достижение необходимой температуры
2. Выполнение эксперимента
Собирают прибор как показано на рис. 4. Для этого:
1. Эксикатор заполняют дистиллированной водой, трубку с фильтром закрепляют на штативе так, чтобы фильтр был погружен в воду на 3-5 см.
2. В верхнюю часть закрепленной трубки (ее диаметр должен быть предварительно измерен с достаточной точностью) аккуратно вводят 20 – 40 мл 0,01 М водного раствора сахарозы (объем раствора должен быть известен точно!).

Рис. 4. Схема установки для определения осмотического давления.
Обозначения: 1 – эксикатор, 2 – воронка Шотта (точнее, то, что от нее осталось после срезания широкой части по фильтр), 3 – фильтр Шотта, 4 – стеклянная или кварцевая трубка, 5 – раствор глюкозы (стрелочкой показано направление его движения при осмосе), 6 – дистиллированная вода, 7 – штатив с держателем и лапкой.
3. Необходимый объем раствора подбирается таким образом, чтобы заполнить широкую часть системы около фильтра и место стыка трубки и воронки Шотта. Далее наблюдают за явлением осмоса.
4. Для этого через каждые сутки фиксируют высоту водяного столба раствора относительно уровня воды в эксикаторе. После этого трубку вынимают из штатива и переворачивают так, чтобы фильтр оказался сверху. Процедуру такого перемешивания повторяют 2-3 раза. После этого трубку снова закрепляют в штативе в прежнем положении. Примерно через неделю показания должны стабилизироваться около определенного значения.
5. Теперь необходимо узнать, какое количество воды разбавило раствор сахарозы (рассчитывают по известной формуле V’ = 3,14r2h’, где h’ – прирост уровня жидкости в трубке, r – радиус этой трубки, V’ – искомый объем). Это позволяет найти концентрацию раствора сахарозы в трубке к моменту установления равновесия. Далее проводят необходимые вычисления и сравнивают, насколько экспериментальные данные отличаются от значений, полученных при использовании осмотического закона Вант-Гоффа.
Экспериментальная часть (продолжение). Лабораторная работа №3. “Химический сад”
Основной задачей предлагаемой работы является качественное наблюдение осмотических явлений. Несмотря на невозможность извлечения количественной информации данная работа дает яркое и наглядное представление об обсуждаемом здесь явлении.
Оборудование и реактивы: 2 химических стакана на 200 мл, ложечка железная химическая, поликристаллические реактивы: кристаллогидраты хлоридов (можно – любых других водорастворимых солей) меди (2+), кобальта, никеля, железа (3+), марганца (2+), неодима (3+), силикат натрия – 10% (по массе) раствор, желтая кровяная соль K4[Fe(CN)6] – 10% раствор.
Ход выполнения работы
В один из цилиндров наливают раствор силиката натрия (можно взять силикатный клей, разведенный дистиллированной водой ~в 3 раза. В другой сосуд наливают раствор желтой кровяной соли (гесацианоферрата (2+) калия). В каждый из цилиндров вносят по 2-3 г указанных солей d-металлов (соли предварительно НЕ перемешивают). Через 5-10 мин фиксируют первые изменения в цилиндрах. В последующем наблюдения ведут через каждые 10-15 минут до конца занятия. Последний раз цилиндры рассматривают на следующем занятии (т.е. ч/з 1-2 недели). Данный эксперимент не требует постоянного наблюдения и может выполняться одновременно с другими работами.
При оформлении работы следует ответить на следующие вопросы:
1. Чем вызван рост объектов разного цвета в цилиндрах?
2. Как записать реакции формирования полупроницаемой перегородки?
3. В случае какой из солей d-элемента отмечался наиболее интенсивный рост объекта? Почему? Каковы Ваши предположения?
4. Почему нельзя брать более концентрированные растворы силиката натрия и желтой кровяной соли?
III.3. Понижение температуры первичной кристаллизации растворителя и повышение температуры закипания раствора при введении примеси. Лабораторная работа №4. Криоскопическое определение молярной массы неизвестного металла и построение эвтектической T‑x диаграммы бинарной системы с помощью ДТА
Остановимся на следующих хорошо известных из жизни фактах:
1. Морская вода начинает замерзать при температурах, заметно меньших 0 С. При такой кристаллизации выделяющаяся твердая фаза представляет собой практически чистый лед (недаром полярники часто добывают воду, полученную при растапливании части льдины, образовавшейся при замерзании поверхности моря или океана).
2. Для борьбы c обледенением дорог зимой их часто посыпают растворимыми в воде веществами: солями, мочевиной и т.д. При этом часть льда “плавится” с образованием раствора, который может находиться в контакте с оставшимся льдом сколь угодно долго. Заметим, что жидкий раствор и твердый растворитель могут сосуществовать не при единственной температуре (как для чистых веществ), а в интервале температур. Например, лужицы раствора соли в контакте со льдом можно наблюдать и при ‑ 5, и при ‑ 10 С. При этом чем меньшая температура удерживается, тем меньшее количество льда превращается в жидкий раствор при одном и том же количестве используемой соли.
Рассмотрим более подробно такие фазовые превращения в растворах, которые связаны с кристаллизацией/плавлением. Ограничимся только такими случаями, когда примесь B очень хорошо растворима в жидком растворителе A, но в твердом (закристаллизовавшемся) растворителе растворимость этой примеси ничтожно мала. Для простоты будем также считать, что вещества A и B не дают между собой никаких соединений. Такая ситуация является очень распространенной: известно, что огромное количество веществ хорошо растворяется в жидкой воде, однако лишь очень немногие из них заметно растворимы в кристаллах льда.
(!) Конечно же, имеются и другие варианты физико-химического взаимодействия между произвольно выбранными веществами A и B, рассмотрение которых выходит за рамки данной работы.
Примем, что рассматриваемые фазовые превращения происходят в контакте с насыщенным паром растворителя, а летучесть примеси пренебрежимо мала. Температурная зависимость давления насыщенного пара над твердым и жидким растворителем A определяется кривыми (ab) и (bc) соответственно (рис. 5 а). Давление пара над жидкими растворами с возрастающими концентрациями примеси B xB1, xB2, xB3 описывается кривыми bc, bc, bc. Чем больше концентрация примеси в растворе, тем ниже расположена соответствующая ветвь экспоненты (вспомнить закон Рауля!). Точки пересечения кривых (b, b, b, b) соответствуют ситуации, когда давление паров над закристаллизованным растворителем и над раствором совпадают, т.е. в этих условиях жидкая и твердая фазы могут сосуществовать (совместно с паром). Из рис. 5 видно, что более концентрированный раствор имеет меньшую температуру фазового превращения
![]() . (III.3.1)
. (III.3.1)
В
(III.3.1)
![]() обозначает компонент A,
находящийся в твердой фазе жидкий
раствор,
обозначает компонент A,
находящийся в твердой фазе жидкий
раствор,
![]() – этот
же компонент в жидком растворе.
– этот
же компонент в жидком растворе.
а)

б)
Рис. 5. К обоснованию понижения температуры кристаллизации растворов при увеличении концентрации примеси в разбавленных растворах. Пояснения в тексте.
Почему растворы кристаллизуются, как правило, не при фиксированной температуре, а в интервале температур?
Это связано с тем, что в ходе кристаллизации из раствора удаляется один из компонентов (для относительно разбавленных растворов – растворитель). При этом концентрация раствора непрерывно изменяется, и, соответственно, изменяется и температура превращения (III.3.1). Кривая на рис. 5 б показывает, как связана температура этого превращения с концентрацией примеси xB.
До какой минимальной температуры можно охладить раствор, сохраняя при этом жидкую фазу?
Для ответа на этот вопрос вначале заметим, что концентрированные растворы ведут себя при охлаждении по-другому: из таких растворов при понижении температуры выделяется примесь (например, соль), а раствор обогащается растворителем (рис. 6).
 Обе
кривые первичной кристаллизации можно
нанести на один график. Для этого
развернем рисунок 5 б
на 90
против часовой стрелки и совместим с
рис. 6 На получившемся рис. 7 видно,
что эти кривые пересекаются в некоторой
точке с координатами (Te,
xe),
называемой эвтектической
(от
греческого “эутектос”
‑
легко плавящийся).
Обе
кривые первичной кристаллизации можно
нанести на один график. Для этого
развернем рисунок 5 б
на 90
против часовой стрелки и совместим с
рис. 6 На получившемся рис. 7 видно,
что эти кривые пересекаются в некоторой
точке с координатами (Te,
xe),
называемой эвтектической
(от
греческого “эутектос”
‑
легко плавящийся).
Рис. 6. Зависимость температуры первичной кристаллизации (T) от концентрации примеси вещества B. Область концентрированных растворов B в A.
При медленном отводе тепла жидкий раствор с концентрацией xe кристаллизуется при фиксированной температуре – так же, как и чистое вещество. Однако при кристаллизации такого раствора выделяется не одна, а две твердые фазы – в виде тонкой механической смеси. Соответственно, при температуре Te сосуществуют, сколь угодно долго, не две, а три конденсированных фазы, связанные фазовым равновесием
![]() (III.3.2)
(III.3.2)
где L – жидкий раствор, S и S ‑ две различные фазы; в нашем случае – фазы, состоящие из почти чистых компонентов A и B соответственно. Например, в эвтектической точке системы H2O ‑ NaCl (‑ 21C) сосуществуют соль, жидкий соляной раствор и лед. Представленный ниже рисунок является т.н. T-x фазовой диаграммой системы A-B.
 Рис. 7.
T-x
фазовая диаграмма эвтектического типа
системы A-B.
Рис. 7.
T-x
фазовая диаграмма эвтектического типа
системы A-B.
Особенностью T-x диаграммы является то, что любая точка этого графика (а не только точки на линиях) имеет определенный физический смысл. Например, все точки, расположенные выше линий первичной кристаллизации соответствуют жидкой фазе (обозначение L).
Кривые первичной кристаллизации – т.н. линии ликвидуса – описываются т.н. уравнениями Шредера, которые в приближении идеальных растворов выглядят как (III.3.3) и (III.3.4).
 ; (III.3.3)
; (III.3.3)
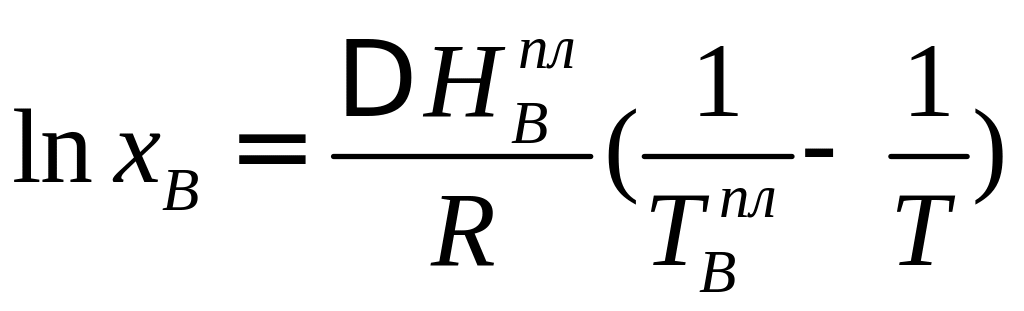 (III.3.4)
(III.3.4)
В
уравнениях (III.3.3)
и (III.3.4),
![]() -
энтальпии плавления компонентов A
и B
(равны соответствующим теплотам, взятым
с обратным знаком), R
– газовая постоянная,
-
энтальпии плавления компонентов A
и B
(равны соответствующим теплотам, взятым
с обратным знаком), R
– газовая постоянная,
![]() - температуры плавления веществ A
и B,
T
– температура первичной кристаллизации,
xB
– концентрация примеси, выраженная в
молярных долях.
- температуры плавления веществ A
и B,
T
– температура первичной кристаллизации,
xB
– концентрация примеси, выраженная в
молярных долях.
Выражение (III.3.3) записано для первичной кристаллизации вещества A, выражение (III.3.4) – для кристаллизации B. Совместное решение (III.3.3) и (III.3.4.) позволяет получить координаты эвтектической точки (Te, xe).
КРИОСКОПИЯ
Особый интерес представляет анализ (III.3.3) в случае очень разбавленных растворов. Используя разложение логарифма в ряд, левую часть (III.3.3) можно преобразовать как
![]() (III.3.5)
(III.3.5)
Для разбавленных растворов (xB0) ограничимся первым членом:
![]() ; (III.3.6)
; (III.3.6)
а молярную долю xB выразим через массы веществ A и B:
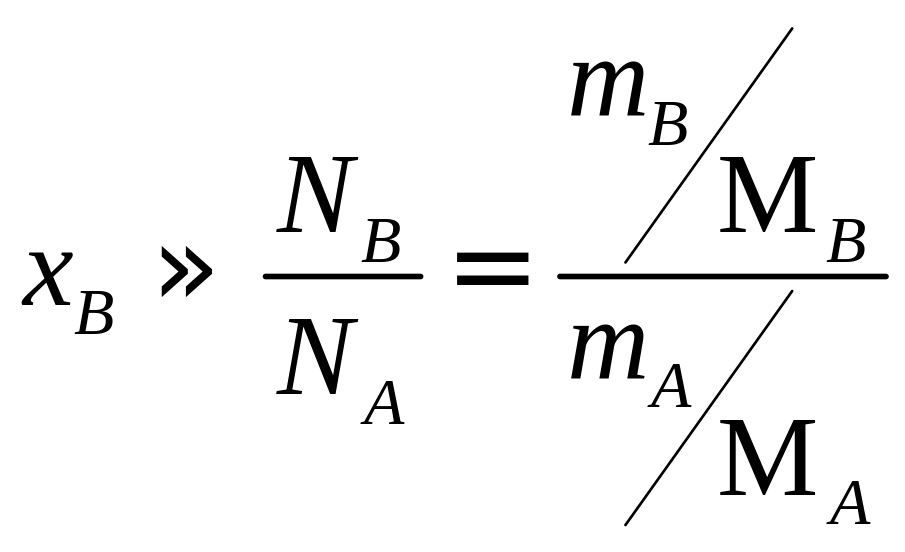 (III.3.7)
(III.3.7)
Правая часть (III.3.3) может быть упрощена:
 (III.3.8)
(III.3.8)
После приравнивания правых частей (III.3.7) и (III.3.8) и произведения замены
![]()
получаем
(III.3.9)
 (III.3.10)
(III.3.10)
Из (III.3.8) видно, что природа растворяемого вещества B– примеси – не влияет на температуру первичной кристаллизации растворителя. Имеет значение только количество взятого вещества (mB/MB).. Это позволяет говорить о том, что рассматриваемый эффект отражает коллигативные свойства разбавленных растворов.
Напротив, величина Tкр явно зависит от природы растворителя, которая проявляется в таких индивидуальных характеристиках, как температура и энтальпия плавления (TAпл и HAпл соответственно). Нетрудно видеть, что эффект понижения температуры первичной кристаллизации растворителя будет более сильно выражен в том случае, если:
- используемый растворитель плавится при относительно высокой температуре,
- на разрушение кристаллической структуры растворителя тратится относительно малая энергия.
– величина молярной массы растворителя достаточно велика.
Приведенные характеристики дают возможность предположить, что вода является не слишком удачным растворителем для наблюдения эффекта понижения температуры кристаллизации (ответьте, почему) в противоположность тяжелым органическим веществам.
На практике имеет значение обратная задача: нахождение молярной массы исследуемого вещества, вводимого в раствор в виде примеси по определяемому экспериментально эффекту понижения температуры первичной кристаллизации растворителя. Такой метод называется криоскопическим (от греческих слов - “крио” – лед, замораживать и “скопео” – измерять). Выражение (III.3.10) можно переписать, выразив молярную массу примеси MB. Для уменьшения громоздкости выражения константы, относящиеся к природе растворителя, часто объединяют в одну постоянную величину, которая носит название криоскопической константы:
 (III.3.11)
(III.3.11)
Тогда (III.3.8) преобразуется к виду
 (III.3.12)
(III.3.12)
Именно выражение (III.3.12) используется в одном из заданий настоящей лабораторной работы, которое связано с определением молярной массы неизвестного металла криоскопическим методом. Таким образом, измерение величины Tкр является основной экспериментальной задачей работы.
Метод дифференциального термического анализа (ДТА)
Величину Tкр находят в настоящей работе с помощью дифференциально-термического анализа (ДТА). Принципиально метод ДТА основан на сравнении температуры образца с температурой вещества сравнения (эталона) в процессе изменения температуры с определенной скоростью. Температуры исследуемого образца и эталона должны быть одинаковыми (или почти одинаковыми) до начала фазового превращения, происходящего в образце. При прохождении этих превращений температура образца либо отстает (эндотермический процесс), либо опережает (экзотермический процесс) температуру эталона. На рис. 8 схематически показаны два способа регистрации результатов ДТА. Если образец нагревается с постоянной скоростью и его температура изменяется непрерывно с помощью термопары, то зависимость температуры от времени линейна до начала эндотермического эффекта (рис. 8 а). Далее вплоть до завершения превращения температура плавления либо остается постоянной до окончания превращения (плавление индивидуального вещества или эвтектической смеси, перестройка кристаллической структуры и т.д.), либо продолжает возрастать, но с нарастающим отставанием от температуры эталонного вещества. После завершения превращения температура резко возрастает и вновь становится близкой температуре эталонного вещества. Таким образом, термический эффект проявляется как горизонтальный, либо слабонаклонный участок зависимости T=f(), заканчивающийся почти вертикальным изломом (рис. 8 а).
Однако на графике зависимости температуры образца от времени (называемом “простой” записью) трудно обнаружить процессы, сопровождающиеся небольшими выделениями тепла, т.к. время их протекания невелико. Следовательно, невелики и отклонения от линии T=f() для эталонного сосуда. Все это приводит к тому, что такой вариант термического анализа в настоящее время самостоятельно не используют.
Другой способ состоит в том, что измеряют или вычисляют разность температур T между исследуемым и эталонным сосудами (рис. 8 б). На начальном этапе эксперимента – до тех пор, пока в веществе не начались фазовые превращения – величина T близка к нулю. С началом таких превращений температура исследуемого вещества начинает “отставать” от температуры эталона и возникает некоторая разница температур. На практике строят зависимость T от температуры исследуемого сосуда. Такой способ (называемый “дифференциальной” записью) позволяет значительно увеличить точность определения температуры фазового превращения.
(!) При расшифровке результатов за температуру эффекта обычно принимают начало пика (рис. 8 б). Исключение представляет собой определение температуры полного плавления вещества (линии ликвидуса). Для определения такой температуры находят минимум пика (если пик имеет несколько минимумов, то находят минимум, относящийся к наибольшей температуре). Отметим, что аналогичная методика может применяться и к исследованиям, проводящимся в режиме охлаждения.

Рис. 8. Типичный вид термограммы нагревания индия. “Простая” (a) и “дифференциальные” виды записи термограммы (б). Скорость нагревания v = 0,47 C/мин.
Экспериментальная часть. Лабораторная работа № 4
Основными задачами настоящей работы являются криоскопическое определение молярной массы неизвестного металла и построение T-x диаграммы бинарной системы методом ДТА. В настоящей работе исследуется фазовая диаграмма системы Ga-Me, где Me – относительно легкоплавкий металл (In, Sn, Cd). В качестве растворителя используется галлий, низкая температура плавления которого позволяет проводить исследования при помощи несложного оборудования.
Оборудование и реактивы:
компьютер,
криотермостат (ТЖ-ТС-01),
7 запаянных стеклянных сосудов Степанова, заполненных сплавами галлия с индием со следующим содержанием индия: 0%, 1%, 2%, 3%, 7%, 10%, 15%;
один запаянный стеклянный сосуд Степанова с реперным веществом,
восьмиканальный измеритель температур (УКТ-38),
8 термопар, подключенных к измерителю УКТ-38,
держатель для сосудов Степанова..
Все сосуды Степанова со сплавами определенных составов должны быть приготовлены заранее
Ход выполнения работы:
Эксперимент
1. Подготовка образцов. Установить в гнезда держателя реперный сосуд Степанова (с металлическим свинцом) и 7 выданных преподавателем сосудов со сплавами. Записать соответствие между маркировкой сосуда и маркировкой гнезда. Вставить термопары в сосуды Степанова так, чтобы королек сплава проводов термопар максимально входил в отверстие сосуда. Записать соответствие каждой термопары и сосуда Степанова.
Внимание! Просьба ответственно отнестись к этой рутинной процедуре. Даже одна допущенная на этом этапе ошибка может привести к необходимости переделывать всю работу.
2. С криотермостата снять крышку и аккуратно погрузить держатель с сосудами в рабочую жидкость синего цвета (тосол). Следить, чтобы термопары не выскользнули из сосудов и оставались внутри углублений сосудов.
3. Подготовка компьютера к работе. Включить компьютер. Убедиться, что операционная система Windows загрузилась.
4-6. Наблюдение кристаллизации сплавов при переохлаждении и устранение метастабильных состояний
Галлий и сплавы на его основе часто переохлаждаются (т.е. остаются жидкими при температурах, заметно меньших температур плавления). Однако для выполнения основных задач в работе изначально необходимо иметь сплавы в твердом состоянии. Для кристаллизации указанных сплавов необходимо сильное охлаждение – до 25 С. Однако при таких температурах галлий может закристаллизоваться с образованием метастабильной модификации – т.н. -Ga. Появление этой модификации может исказить получаемые данные. Однако -Ga можно превратить в стабильную форму -Ga при выдерживании в течение нескольких минут сплавов при 10 С.
4. Программирование криотермостата на охлаждение до 25 С. Включите выключатель (красного цвета) на управляющей головке криотермостата ТЖ-ТС-01. На панели должно загореться сообщение «Start» после чего прибор перейдет в режим достижения введенной температуры. Нажмите кнопку «» (правая нижняя в ряду управляющих кнопок прибора) и, пользуясь стрелками «» и «», задать температуру 45 С, (В дальнейшем, мы выключим его при достижении -25±1С. Такой способ позволит ускорить выполнение работы, поскольку при приближении температуры к заданной термостат автоматически замедляет изменение температуры). Снова нажмите на кнопку «». Эта процедура даст прибору задание на установление указанной температуры в приборе. Если указанная температура уже выставлена на индикаторе, сразу нажмите кнопку «». (Здесь и далее: в случае, если заданного Вами изменения температуры не происходит, попробуйте выключить и включить прибор).
