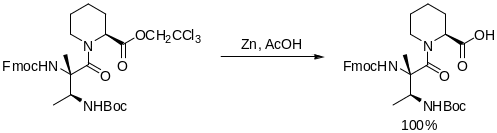- •Курс Лекций «Современные проблемы органической химии»
- •Защита гидроксильной группы
- •Сложные эфиры
- •Силиловые эфиры
- •Триметилсилиловые эфиры tms
- •Триэтилсилиловые эфиры tes
- •Третбутилдиметилсилиловые эфиры tbs
- •Третбутилдифенилсилиловые эфиры tbdps
- •Триизопропилсилиловые эфиры tips I-Pr3Si
- •Защитные группы для азота
- •Защиты карбосильных групп.
- •Метиловые эфиры.
- •Трет-бутиловые эфиры.
- •Аллиловые эфиры
- •Силиловые эфиры
Метиловые эфиры.
Получение.
Реакция с дазометаном. Последний получают реакицей N-метил-N-нитрозо-nтолуолсульфамида с КОН и исползуют в эфирном растворе. Диазометан летуч, токсичен, взрывоопасен. Но несмотря на это, метод используется в случае небольших загрузок. Диазометан в растворе желтый, и при встеплении в реакцию раствор обесцвечивается. В последнее время используют периметилимидазометан.
Этерификация кислот в метаноле в присутсвии 2 экв Me3SiCl используется для этрификации аминокислот.
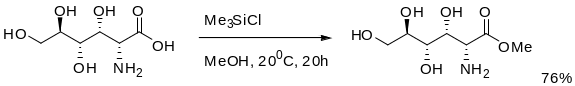
В начале генерируется триметилсилиловый эфир, который in situ превращается в меттиловый эфир.
Na, K, CsCOMe и тетраалкиламмониевык соли карбоновых кислот и метилиодид в ДМФА.

Использование N,N’-диалкил-О-метилизомочевин.
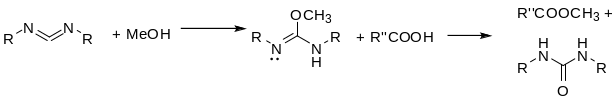
Этот тип реакции позволяет осущетсвить этерификацию кислоты в присутствии незащищенных ОН-групп.
Снятие метильных защитных групп.
Обычный метод – гидролиз, катализируемый гиороксилами металлов или карбонатами в метанле или ТГФ, - ограничивается настабильностью субстратов в основных условиях.
Следующий пример иллюстрирует селективный гидролиз сложноэфирной группы.
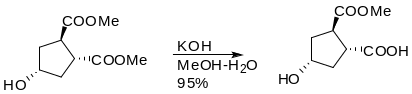
Карбоксилат анион является плохой уходящей группой, однако галогенид, тиолят или уианид анионы, чью нуклеофильность модно повысить, исопльзуя диполярные апротонные расворители, атакуют метиловые, этиловые и бензиловые эфиры при обычных температурах. Метиловые эфиры в 70 раз быстрее расщепляются по сравнению с соответствующими этиловыми эфирами, что можно использовать для селективного расщепления.
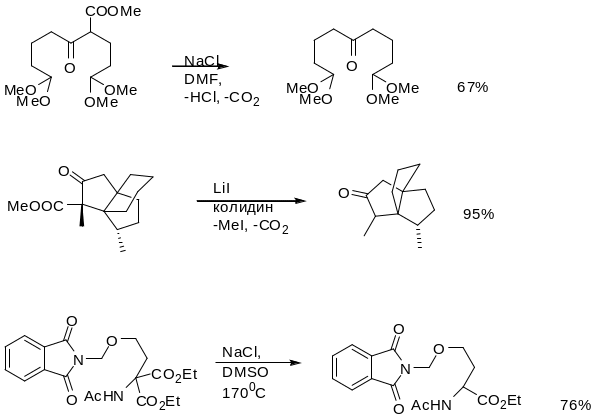
Понизить температуру расщепления метиловых эфиров можно, используя высокую нуклеофильность тиолят аниона в диполярных растворителях или используя тиоэфиры в присутствии кислот Льюиса.
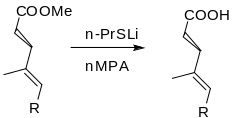
При этом ОМе, фенольные и спиртовые, s,s-диацетальная и OSiMe2But защита сохраняются.
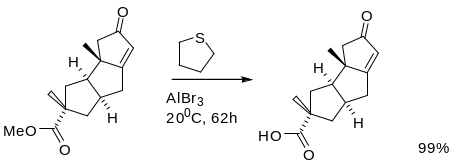
Трет-бутиловые эфиры.
О-третбутилтрихлорацетимидат получают с выходом в 70% из нитрила и t-BuOK (см. карюосоединения).
![]()
Имидат реагирует с кислотой в присутствии каталитичесиких количеств BF3 при 20°С в системе циклогексан-CH2Cl2.
Аналгичная реакция имеет место при использовании N,N’-диизопропил-О-третбутилизомочевиныю Присутствие гидроксильных групп не мешает протеканию реакции.
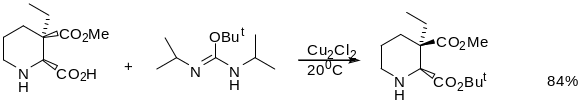
Классический метод, о котором уже говориось раньше, представляет собой использование изо-бутилена в присутствии сильной кислоты.
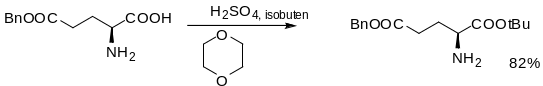
Более мягкий метод – это реакция Ямагуши: использование 2,4,6-трихлорбензоилхлорида и триэтиламина. Образуются смешанные ангидриды, которые реагируют с t-BuOH в присутствии DMAP.
Расщепление. Третбутиловые слжные эфиры очень лабильны в кислых условиях и могут селективно расщепляться в присутствии первичных алкиловых эфиров. С другой стороны первичные алкиловые эфиры в водной щёлочи гидролизуются легче, чем трет-бутиловые эфиры. Из-за стерическх препядствий трет бутиловые эфиры более стабильны к действию нуклеофилов, чем первичные.
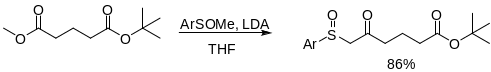
Третбутиловые эфиры легко расщепляются в триторуксусной кислоте водном или дихлорметановом растворе при 20 с потерей избутелена.
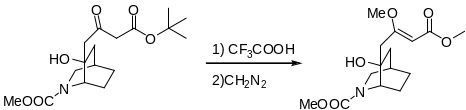
Могут быть использованы и муравьиная и п-толуолсульфокислота в кипящем бензоле.
Может быть использована уксусная в кипящем изпропаноле (мягкие условия. Этот метод используется в синтезе винкамина алкалода индольного ряда.).

MOM |
MEM |
BOM |
MTM |
SEM |
CH3OCH2 |
CH3CH2CH2OCH2 |
PhCH2OCH2 |
CH3SCH2 |
CH3SiOCH2CH2OCH2 |
Получение Реакции солей карбоовых кислот с ROCH2Cl.
![]()
В отсутствии кислот, образующиеся ацетали сложных эфиров показывают реакционную способность типичную для алкиловых эфиров.

МТМ метилтиометиловые эфиры получают реакцией триэтиламмониевых солей карбоновых кислот с хлрдиметилсульфонием хлоридом или калиевой соли кислоты с MeSCH2Cl в присутствии NaI и 18-краун-6. ((CH3)2SCl2)
Расщепление ацетали сложных эфиров чувствительны к мягким слабым водным кислотам в ТГФ, Мягким кислотам Льюиса типа MgBr2 в эфире при 20 С расщепляет МТМ эфиры. МЕМ расщепляют хуже.
Расщепление 48% HF в MeCN при -10 С не затрагивает третбутоксикарбонил (Boc) и бензилоксикарбоил (Cbz) защитных групп BOM можно снять каталитическим гидрированием.
2,2,2-трихлорэтилвые эфиры.
Получение этерификация карбоновых кислот или кароксильной группы с трихлорэтанолом в присутствии дициклогексилкарбодиимида и диметиламинопиридна. Это самый мягкий метод. Традиционный состоит во взаимодействии хлорандрида кислоты с трихлорэтанолом в присутствии пиридина.
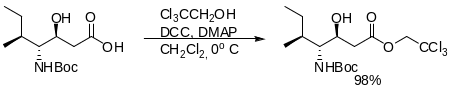
Расщепление Впервые эта защитная группа была использована Вудвордом в синтезе цефлоспорина С. Затем она стала ипользоваться в пептидном синтезе в синтезе антибиотика Lavendomicyn. Она легко удаляется обработкой Zn в AcOH. Возможен метод обработки каталитических количеств Se в присутствии NaBH4 в ДМФА при 40-50 С.