
- •Курс Лекций «Современные проблемы органической химии»
- •Защита гидроксильной группы
- •Сложные эфиры
- •Силиловые эфиры
- •Триметилсилиловые эфиры tms
- •Триэтилсилиловые эфиры tes
- •Третбутилдиметилсилиловые эфиры tbs
- •Третбутилдифенилсилиловые эфиры tbdps
- •Триизопропилсилиловые эфиры tips I-Pr3Si
- •Защитные группы для азота
- •Защиты карбосильных групп.
- •Метиловые эфиры.
- •Трет-бутиловые эфиры.
- •Аллиловые эфиры
- •Силиловые эфиры
Триметилсилиловые эфиры tms
Me3SiO группа отщепляется в очень мягких условиях АсОН или К2СО3 в МеОН. Скорость гидролиза зависит как от стерических, так и от электронных эффектов. Увеличение стирики уменьшает скорость гидролиза. Электроноакцепторные функции в алкогольной части увеличивают скорость.
Получение. Для триметилсилилирования используют большое количество реагентов, большинство из которых являются коммерческими.
Дешевый Me3SiCl (TMSCl) и более активный CF3SO2OSiMe3 (TMSOTf) силилируют гидроксильные группы в присутствии оснований (пиридин, Et3N, i-Pr2NЕt, имидазол). Соли аминов гидрохлориды отфильтровывают; для трифлата нужна водная обработка. В качестве растворителей могут быть использованы CH2Cl2, MeCN, ТГФ, ДМФА (абсолютные).
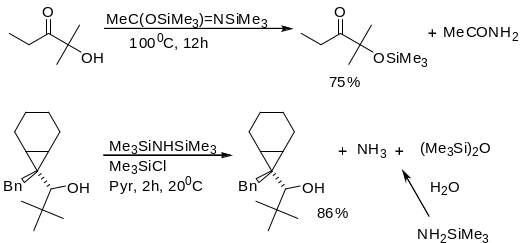
В случае альдегидов и кетонов TMSOTf превращает их в силиловые эфиры енолов.
![]()
Трифлат может расщеплять эпоксиды.

Когда присутствие солей или водная обработка нежелательны триметилсилилирование может быть осуществлено:
N,O-бис(триметилсилилацетамид)
![]() ,
гексаметилдисилазан (HMDS)
,
гексаметилдисилазан (HMDS)
катализируемый Me3SiCl, 1-триметилсилилимидазол (TMSIM).
Триэтилсилиловые эфиры tes
Et3Si группа более стабильна, чем метильная при колоночной хроматографии и к действию окислителей, восстановителей и металлоорганических соединений.
TES в 10-100 раз более стабильна к гидролизу и нуклеофильной атаке, чем Me3Si, но менее стабильна, чем t-BuMe2Si (TBS).
TES группу избирательно можно отщепить действием НОАс в водном ТГФ, 2% HF или HF в пиридине.
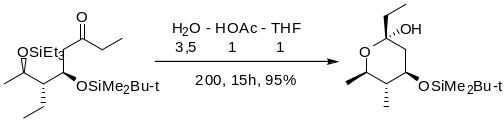
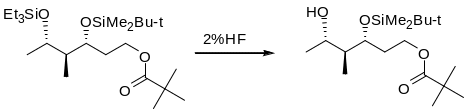
Введение. Ввести TES группу можно Et3SiCl в присутствии имидазола. Триэтилсилилтрифлат в пиридине или 2,6-лутидине используется для защиты β-ОН группы альдегидов, кетонов, сложных эфиров.
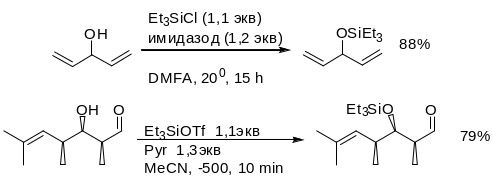
Третбутилдиметилсилиловые эфиры tbs
Самая популярная из групп. Стала использоваться только в 1972 году.
TBS стабильна при хроматографии, при ниже 00С к действию сильных не протонных оснований типа н-алкилLi, реагенты Гриньяра, еноляты и металлированные сульфоны. Однако t-BuLi депротонирует SiMe группу в ТГФ около –100С, что можно использовать для препаративных целей. TBS лобильна в мягких кислых условиях и в присутствии кислот Льюиса. Устойчива к действию LiAlH4, но расщепляется DIBAlH (Bu2AlH) при 200С.
Получение. Стерические препятствия значительно уменьшают скорость силилирования с t-BuMe2SiCl и для увеличения скорости лучше добавлять имидазол в качестве активатора и использовать диполярный апротонный растворитель ДМФА. Первичная спиртовая группа реагирует намного быстрее, чем вторичная, а третичная вообще инертна.

Стерически трудные вторичные и третичные спирты силилируются трет-бутилдиметилсилилтрифлатом (TBSOTf) в присутствии 2,6-лутидина.

При этом силилирование может сопровождаться реакцией пересилилирования.

Снятие защиты. АсОН при 200С SiMe2Bu-t удаляется легче, чем SiPh2Bu-t или SiPr3.
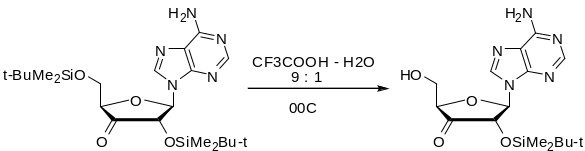
2,5-бис-О-(третбутилдиметилсилил)-3’-кетоадепозин
Снимается менее стерически трудная группа. Снятие защиты не лимитируется только кислыми реагентами: фторид анион в основных условиях также эффективен. Наиболее популярен для этих целей тетра-н-бутиламоний фторид (TBAF). Бензилтриметиламмоний фторид также может использоваться для этих целей.
TBAF стоит очень дорого. Из-за высокой основности может вызвать нежелательные реакции β-элиминирования или образование енолятов.
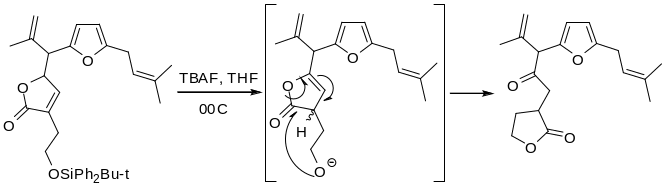
В зависимости от условий фенольные и спиртовые SiMe2Bu-t группы могут сниматься селективно.
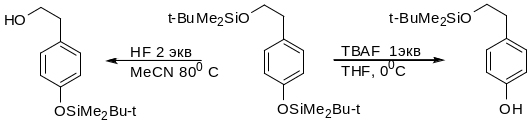
Фторид аммония в кипящем метаноле – экономическая альтернатива TBAF. SiMe2Bu-t группу можно снять каталитическим гидрогенолизом.
