
- •Фазовые состояния углеводородных систем
- •1. Виды фазовых превращений.
- •2. Схемы фазовых превращений углеводородов
- •1. Схемы фазовых превращений однокомпонентных систем
- •2. Схема фазовых превращений двух- и многокомпонентных систем.
- •1. Способы изображения состава бинарных систем.
- •2. Способы изображения состава трёхкомпонентных систем.
- •3. Поведение бинарных и многокомпонентных систем в критической области
- •4. Критическая температура и критическое давление многокомпонентных углеводородных смесей.
- •12 Метан — бензол; 13 — метан — нонан; 14 — метан — толуол; 15 — метан — декан;
- •5. Условия залегания углеводородов в газовых, газоконденсатных и газонефтяных залежах
- •6. Влияние строения углеводородов, давления и температуры на фазовые превращения газоконденсатных систем.
- •7. Влагосодержание природных газов и газоконденсатных систем. Влияние воды на фазовые превращения углеводородов.
- •8. Фазовое состояние системы нефть – газ при различных давлениях и температурах.
- •9. Оценка типа газовых залежей. Прогнозирование нефтяной оторочки по составу пластового газа.
3. Поведение бинарных и многокомпонентных систем в критической области
Типовые
изотермы многокомпонентных углеводородных
смесей вблизи критической области
показаны на рис. 5. Как уже упоминалось,
основной признак критической
точки — одинаковые свойства газовой и
жидкой фаз, т. е. она
находится в точке соединения кривых
начала конденсации и парообразования
(в точке
).
Из этого рисунка следует, что в
критической точке давление и температура
не наибольшие, при которых еще возможно
одновременное существование обеих фаз.
Действительно, если давление несколько
меньше
![]() ,
но больше, чем критическое
,
но больше, чем критическое
![]() ,
в системе появляется газовая фаза,
находящаяся в равновесии с жидкой. Это
относится ко всей области
,
в системе появляется газовая фаза,
находящаяся в равновесии с жидкой. Это
относится ко всей области
![]() .
Точно также в области
.
Точно также в области
![]() существуют одновременно две фазы
несмотря на то, что при этом температура
в системе выше критической
существуют одновременно две фазы
несмотря на то, что при этом температура
в системе выше критической
![]() .
Наибольшее давление (
на рис. 5), при котором жидкость и пар
могут существовать в равновесии, принято
называть криконденбар.
Наивысшая температура (
.
Наибольшее давление (
на рис. 5), при котором жидкость и пар
могут существовать в равновесии, принято
называть криконденбар.
Наивысшая температура (![]() на рис. 5), при которой жидкость и пар
существуют в равновесии, называется
крикондентерм.
на рис. 5), при которой жидкость и пар
существуют в равновесии, называется
крикондентерм.

Рис. 5. Типовые изотермы многокомпонентных углеводородных смесей вблизи
критической области.
1 — кривая точек парообразования; 2 — кривая точек конденсации.
В области
выше критической с изменением температуры
и давления в многокомпонентной системе
происходят необычные фазовые превращения.
Чтобы убедиться в этом, рассмотрим
изобарическое расширение насыщенной
газом жидкости по линии
![]() (рис. 5) вследствие повышения температуры
от
(рис. 5) вследствие повышения температуры
от
![]() до
до
![]() .
В точке
с увеличением температуры жидкость
закипает. По мере увеличения температуры
вначале объем газовой фазы увеличивается.
Однако с дальнейшим повышением температуры
объем газовой фазы, достигнув максимума,
очевидно, вновь начинает уменьшаться,
так как в точке
,
так же как и в точке
,
лежащей на кривой начала парообразования,
содержание паровой фазы в системе равно
нулю.
.
В точке
с увеличением температуры жидкость
закипает. По мере увеличения температуры
вначале объем газовой фазы увеличивается.
Однако с дальнейшим повышением температуры
объем газовой фазы, достигнув максимума,
очевидно, вновь начинает уменьшаться,
так как в точке
,
так же как и в точке
,
лежащей на кривой начала парообразования,
содержание паровой фазы в системе равно
нулю.
Необычные
процессы испарения и конденсации
возможны также и при температурах выше
критических - в области
.
Например, при изотермическом расширении
от точки
![]() до
до
![]() ,
расположенных на линии точек начала
конденсации, система проходит двухфазную
область. Причем количество конденсата
в ней вначале увеличивается. После
достижения максимума жидкая фаза далее
в точке М исчезает. Аналогичные
явления в области выше критических
и
наблюдаются не только при изотермическом
или изобарическом расширении и сжатии
смеси, но также и при осуществлении
процесса по любой другой кривой.
,
расположенных на линии точек начала
конденсации, система проходит двухфазную
область. Причем количество конденсата
в ней вначале увеличивается. После
достижения максимума жидкая фаза далее
в точке М исчезает. Аналогичные
явления в области выше критических
и
наблюдаются не только при изотермическом
или изобарическом расширении и сжатии
смеси, но также и при осуществлении
процесса по любой другой кривой.
Рассмотренные необычные процессы фазовых превращений двух и многокомпонентных систем в области выше критической называются процессами обратного или ретроградного испарения и конденсации.

Рис. 6. Различные виды фазовых диаграмм.
1 — кривая точек парообразования; 2 — кривая точек конденсации.
Фазовая
диаграмма, приведенная на рис. 5, типична
для многих систем. Однако условия
возникновения ретроградных явлений и
вид
![]() – диаграммы (
– диаграммы (![]() - удельный объем,
- давление и
- абсолютная температура) в области
критических точек могут быть в зависимости
от состава углеводородных смесей
другими. Так, например, на рис. 6 показаны
фазовые диаграммы в координатах
- удельный объем,
- давление и
- абсолютная температура) в области
критических точек могут быть в зависимости
от состава углеводородных смесей
другими. Так, например, на рис. 6 показаны
фазовые диаграммы в координатах
![]() (давление - температура), построенные
для других условий возникновения
ретроградных явлений. Диаграмма (рис.
6, а) аналогична зависимости
(давление - температура), построенные
для других условий возникновения
ретроградных явлений. Диаграмма (рис.
6, а) аналогична зависимости
![]() ,
приведенной на рис. 5. Здесь в области
,
приведенной на рис. 5. Здесь в области
![]() возникают процессы обратной
изотермической конденсации, а в области
возникают процессы обратной
изотермической конденсации, а в области
![]() - процессы обратного изобарического
испарения.
- процессы обратного изобарического
испарения.
Если критическая
область характеризуется диаграммой
(рис. 6, б), где критическая точка
существует при давлении и температуре
ниже максимальных
и
,
лежащих на кривой парообразования, то
изотермическое обратное испарение
происходит в области
![]() ,
а изобарическое ретроградное испарение
- в области
,
а изобарическое ретроградное испарение
- в области
![]() .
.
Обычно критическая точка находится справа от максимального давления, при котором могут одновременно сосуществовать жидкая и газовая фазы, когда в углеводородной смеси массовая концентрация гептана и более тяжелых фракций высокая, а метана низкая (см. рис. 4, б).
Ретроградные
явления характеризуются диаграммой
вида (рис. 6, в),
когда максимальное давление
находится на кривой точек конденсации,
а критическое давление — между
и давлением, соответствующим
крикондентерме
.
Изотермическая ретроградная конденсация
возникает тогда по любой вертикальной
линии в области
![]() .
В области
.
В области
![]() могут происходить явления обратной
изобарической конденсации. Такие
диаграммы характерны для
жирных и конденсатных газов.
могут происходить явления обратной
изобарической конденсации. Такие
диаграммы характерны для
жирных и конденсатных газов.
Из рис. 5 и 6 следует, что изотермические ретроградные явления происходят только при температурах выше критической и ниже максимальной двухфазной температуры (крикондентермы). Изобарические процессы испарения и конденсации наблюдаются между критическим и максимальным двухфазным давлением (криконденбарой).
Ретроградные процессы испарения и конденсации сопровождаются непрерывным изменением состава и объемного соотношения жидкой и паровой фаз. Например, по диаграмме (рис. 7), соответствующей фазовой диаграмме, приведенной на рис. 6, в, можно проследить за течением процессов обратного испарения и конденсации.

Рис. 7. Фазовая диаграмма вблизи критической точки.
1 - кривая точек парообразования; 2 - кривая точек конденсации.
На рис. 7 нанесены дополнительные кривые,
характеризующие количество (в процентах)
углеводородов в системе, находящихся
в жидком состоянии при различных
давлениях и температурах. По изотерме
(допустим,
![]() )
от давления начала конденсации до
области более высоких давлений можно
проследить за характером ретроградного
процесса. При давлении, соответствующем
точке
)
от давления начала конденсации до
области более высоких давлений можно
проследить за характером ретроградного
процесса. При давлении, соответствующем
точке
![]() ,
молекулы приблизятся друг к другу
достаточно, чтобы силы притяжения начали
действовать между тяжелыми молекулами;
образуется жидкая фаза, состоящая в
основном из тяжелых
углеводородов. Этот процесс будет
происходить до давления
,
молекулы приблизятся друг к другу
достаточно, чтобы силы притяжения начали
действовать между тяжелыми молекулами;
образуется жидкая фаза, состоящая в
основном из тяжелых
углеводородов. Этот процесс будет
происходить до давления
![]() .
При этом давлении выделяется
максимальное количество жидкой фазы и
называется оно давлением
максимальной конденсации. С
дальнейшим повышением давления притяжение
между легкими молекулами, оставшимися
в газе, до этого слабое станет более
эффективным из-за большей близости
молекул. С этого момента молекулы
сконденсировавшихся углеводородов
начинают вновь втягиваться в паровую
фазу. С увеличением давления выше
взаимодействие молекул в жидкости также
несколько уменьшается вследствие
растворения в ней легких углеводородов.
Относительная плотность газовой фазы
увеличивается, и компоненты жидкой фазы
начинают все более и более растворяться
в плотной газовой фазе до тех пор, пока
не закончится процесс ретроградного
испарения. Из сказанного следует, что
процесс ретроградного
испарения можно упрощенно рассматривать
как процесс растворения тяжелых
компонентов в плотной паровой фазе
подобно тому, как тяжелые фракции нефти
растворяются в легком бензине.
.
При этом давлении выделяется
максимальное количество жидкой фазы и
называется оно давлением
максимальной конденсации. С
дальнейшим повышением давления притяжение
между легкими молекулами, оставшимися
в газе, до этого слабое станет более
эффективным из-за большей близости
молекул. С этого момента молекулы
сконденсировавшихся углеводородов
начинают вновь втягиваться в паровую
фазу. С увеличением давления выше
взаимодействие молекул в жидкости также
несколько уменьшается вследствие
растворения в ней легких углеводородов.
Относительная плотность газовой фазы
увеличивается, и компоненты жидкой фазы
начинают все более и более растворяться
в плотной газовой фазе до тех пор, пока
не закончится процесс ретроградного
испарения. Из сказанного следует, что
процесс ретроградного
испарения можно упрощенно рассматривать
как процесс растворения тяжелых
компонентов в плотной паровой фазе
подобно тому, как тяжелые фракции нефти
растворяются в легком бензине.
Описанные явления обратной конденсации часто встречаются в природных условиях. Залежи, которым свойственны ретроградные явления, называются газоконденсатными.
Экспериментальное определение критических параметров углеводородных смесей
Критические параметры (давление, температура, плотность) многокомпонентных углеводородных смесей относятся к числу основных, характеризующих их объёмное и фазовое поведение. По значениям критических давления и температуры углеводородной смеси можно судить о фазовом состоянии её при различных давлениях и температурах. Исследование газожидкостных систем в критических областях, определение критических давлений и температур данной углеводородной системы дает примерное представление о том, в какой области давлений и температур эта система может существовать как жидкость или как газ, или же как двухфазная газожидкостная система. Для практических целей важно знать положение критической точки на пограничной кривой пластовой смеси. В зависимости от того, находится критическая точка выше температуры пласта или ниже, месторождение считается нефтяным или газоконденсатным. Соответственно метод разработки месторождения будет различным.
Критические параметры даже простейших бинарных смесей метана с более тяжёлыми углеводородами изменяются в широком диапазоне в зависимости от состава. При изменении количественного соотношения компонентов критические точки различных смесей индивидуальных углеводородов образуют кривую, которую принято называть огибающей критических точек системы или критической кривой. На рис. 4.7 приведены кривые геометрического места критических точек для бинарных систем, составленных из нормальных парафиновых углеводородов, заимствованные из [21]. Из диаграммы ясно видно, что критическое давление для смеси может быть выше критического давления для каждого из индивидуальных компонентов.
Критические параметры пока не могут быть найдены на основе строго обоснованных термодинамических соотношений, и их определяют или экспериментально, или на основе эмпирических корреляций. Имеется достаточное количество экспериментальных данных о критических параметрах лишь простых компонентов, по которым можно построить огибающие кривые критических точек этих простых систем. Для сложных многокомпонентных смесей построение таких огибающих осложняется из-за недостатка данных о значениях критических параметров чрезвычайно широкого многообразия смесей, которые встречаются на практике.
Особенное значение представляет экспериментальный метод определения критических параметров углеводородных смесей по характеру изменения скачка изохорной теплоёмкости и производной давления по температуре. Причем особо следует отметить, что предлагаемый метод позволяет локализовать критическую точку смеси как в свободном объёме, так и в любой пористой среде.

Рис. 4.7. Геометрические места точек критической области у бинарных систем нормальных парафинов [2].
1
– метан; 2 – этан; 3 – пропан; 4 -
![]() -бутан;
5 -
-пентан;
6 -
-гексан;
7 -
-гептан;
8 -
-
декан.
-бутан;
5 -
-пентан;
6 -
-гексан;
7 -
-гептан;
8 -
-
декан.
Ранее
я уже говорил при описании конструкции
экспериментального адиабатического
комплекса о высокой точности измерения
основных параметров смеси, в том числе
давления и температуры. Достижение
особо высокой точности измерения было
не самоцелью. Именно благодаря высокой
точности впервые была получена возможность
корректно
измерять термодинамические производные,
включая изохорную
![]() и изобарную
и изобарную
![]() теплоёмкости, изохорную
термодинамическую производную давления
по температуре
теплоёмкости, изохорную
термодинамическую производную давления
по температуре
![]() и другие термодинамические производные.
и другие термодинамические производные.
При
температуре перехода из одного фазового
состояния в другое (например, из
двухфазного состояния в однофазное)
теплоёмкость испытывает аномальное
поведение (скачок), а в зависимости
давления от температуры наблюдается
излом (в производной также будет скачок).
Критической
точке соответствует такое состояние
вещества, при котором исчезает различие
между жидкостью и равновесным с ней
паром. Такое состояние вещества называется
критическим.
По мере приближения к критической точке
происходит уменьшение величины скачка
в зависимости термодинамической
производной
![]() и изохорной теплоёмкости от температуры
(«зарезание»). Необходимо отметить, что
в отличие от смесей, для чистых веществ
в критической точке зависимость изохорной
теплоёмкости от температуры носит
сингулярный характер, а в зависимости
от температуры, также как и в смесях,
скачок зануляется
и изохорной теплоёмкости от температуры
(«зарезание»). Необходимо отметить, что
в отличие от смесей, для чистых веществ
в критической точке зависимость изохорной
теплоёмкости от температуры носит
сингулярный характер, а в зависимости
от температуры, также как и в смесях,
скачок зануляется
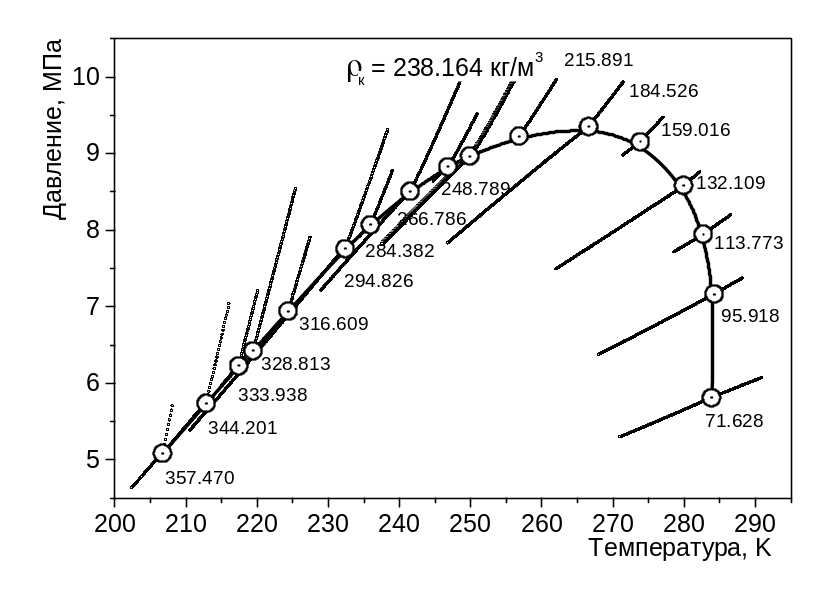
Рис.
4.8а. Зависимость давления бинарной
углеводородной смеси в околокритической
области от температуры на ряде изохор
в диапазоне плотностей 71,6 – 357,47 кг/м3
(критическая температура
![]() = 249,89 К, критическое давление
= 249,89 К, критическое давление
![]() = 8,97 МПа, критическая плотность
= 8,97 МПа, критическая плотность
![]() = 238,16 кг/м3).
По Степановой Г.С.:
= 264,1 К, с учётом поправки
=254,9
К
= 238,16 кг/м3).
По Степановой Г.С.:
= 264,1 К, с учётом поправки
=254,9
К
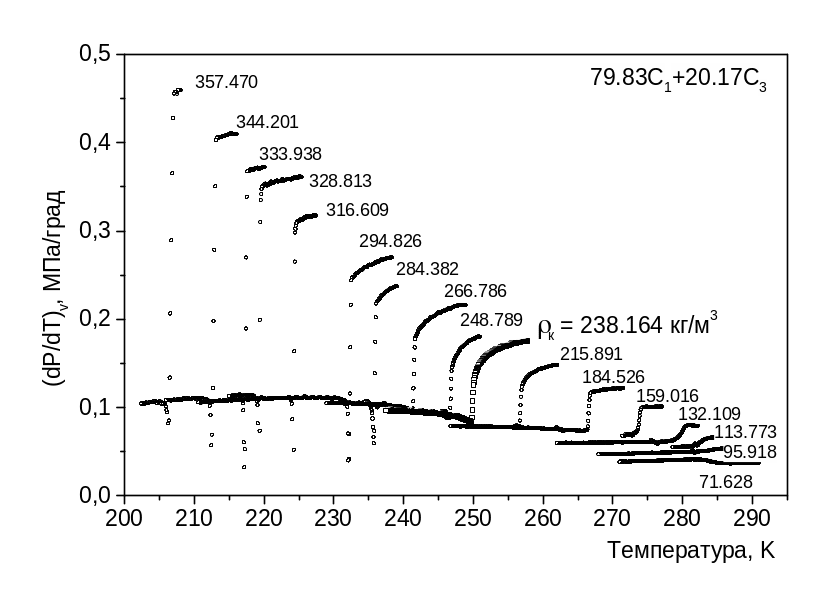
Рис. 4.8б. Зависимость термодинамической производной бинарной углеводородной смеси в околокритической области от температуры на ряде изохор в диапазоне плотностей 71,6 – 357,47 кг/м3 (критическая температура = 249,89 К, критическое давление = 8,97 МПа, критическая плотность = 238,16 кг/м3). По Степановой Г.С.: = 264,1 К, с учётом поправки =254,9 К.


Рис.
4.9. Зависимость термодинамической
производной
(а) и изохорной
теплоёмкости
![]() (б)
трёхкомпонентной углеводородной смеси
в околокритической области от температуры
на ряде изохор в диапазоне плотностей
232,06 – 303,18 кг/м3
(критическая температура
= 260,89 К, критическое давление
= 11,76 МПа, критическая плотность
= 282,45 кг/м3).
(б)
трёхкомпонентной углеводородной смеси
в околокритической области от температуры
на ряде изохор в диапазоне плотностей
232,06 – 303,18 кг/м3
(критическая температура
= 260,89 К, критическое давление
= 11,76 МПа, критическая плотность
= 282,45 кг/м3).
Особый характер изменения скачка изохорной теплоёмкости и производной давления по температуре в околокритической области углеводородной смеси иллюстрируют рис.4.8 (а, б) и , 4.9 (а, б). На рис. 4.8 (а) показаны пограничная кривая жидкость – пар и зависимость давления бинарной углеводородной смеси (смесь 7 в табл. 3.1) от температуры при постоянной плотности в свободном объёме. Для этой же смеси и на тех же изохорах, что на рис. 4.8 (а), на рис. 4.8 (б) показана зависимость от температуры. На рис. 4.8 (б) отчётливо видно, что по мере приближения к критической точке происходит уменьшение величины скачка в зависимости термодинамической производной от температуры.
На рис. 4.9 показаны зависимость (а) и изохорной теплоёмкости - (б) трёхкомпонентной углеводородной смеси 2 (табл.3.1) от температуры в свободном объёме. Скачок в зависимостях и от температуры соответствует фазовому переходу из двухфазной области (жидкость – пар) - в однофазную (газ).
Особый
характер изменения скачка изохорной
теплоёмкости и производной
давления по температуре в
околокритической области углеводородной
смеси, позволяет корректно локализовать
критическую точку.На рис. 4.10 представлены
зависимости величины скачка -
![]() метана и трёхкомпонентной смеси 2 (табл.
3.1) от плотности. Как видно из рисунков,
с уменьшением плотности по мере
приближения к критической точке
происходит уменьшение величины скачка
термодинамической производной
.
В критической точке величина скачка
зануляется. При дальнейшем уменьшении
плотности для чистых компонентов (в
нашем случае для метана) величина скачка
продолжает уменьшаться, принимая
отрицательные значения. Для смеси двух
и более углеводородных компонентов
величина скачка сначала возрастает, а
потом монотонно убывает, достигая
нулевого значения в крикондетерме. При
дальнейшем уменьшении плотности величина
скачка продолжает уменьшаться, принимая
отрицательные значения.
метана и трёхкомпонентной смеси 2 (табл.
3.1) от плотности. Как видно из рисунков,
с уменьшением плотности по мере
приближения к критической точке
происходит уменьшение величины скачка
термодинамической производной
.
В критической точке величина скачка
зануляется. При дальнейшем уменьшении
плотности для чистых компонентов (в
нашем случае для метана) величина скачка
продолжает уменьшаться, принимая
отрицательные значения. Для смеси двух
и более углеводородных компонентов
величина скачка сначала возрастает, а
потом монотонно убывает, достигая
нулевого значения в крикондетерме. При
дальнейшем уменьшении плотности величина
скачка продолжает уменьшаться, принимая
отрицательные значения.

Рис. 4.10. Зависимость метана и трёхкомпонентной смеси от плотности
На рис.4.11 показана зависимость трёхкомпонентной углеводородной смеси (смесь 1, в табл. 3.2) в свободном объёме от температуры. Критические параметры углеводородных смесей, зависимости термодинамических производных которых и изохорной теплоёмкости представлены на рис. 4.8, 4.9 и 4.11, даны ниже:
- бинарная (смесь 7 в табл. 3.1): критическое давление - 8,97 МПа, критическая температура – 249,90 К, критическая плотность – 238,16 кг/м3;
- трёхкомпонентная (смесь 2, табл. 3.1): критическое давление - 11,757 МПа, критическая температура – 260,89 К, критическая плотность – 282,45 кг/м3;
- трёхкомпонентная (смесь 1, табл. 3.2): критическое давление - 35,152 МПа, критическая
температура – 282,97 К, критическая плотность – 452.80 кг/м3.
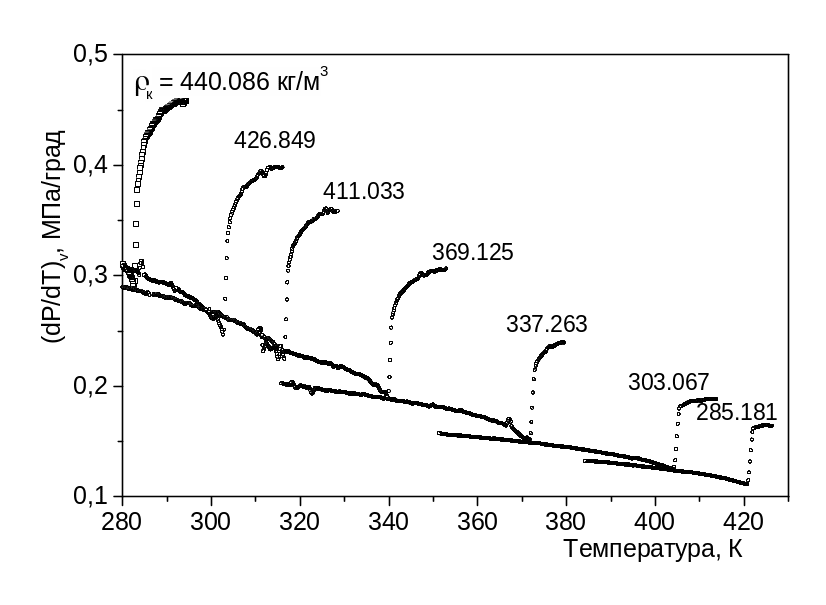
Рис. 4.11. Зависимость трехкомпонентной углеводородной смеси в околокритической области.
